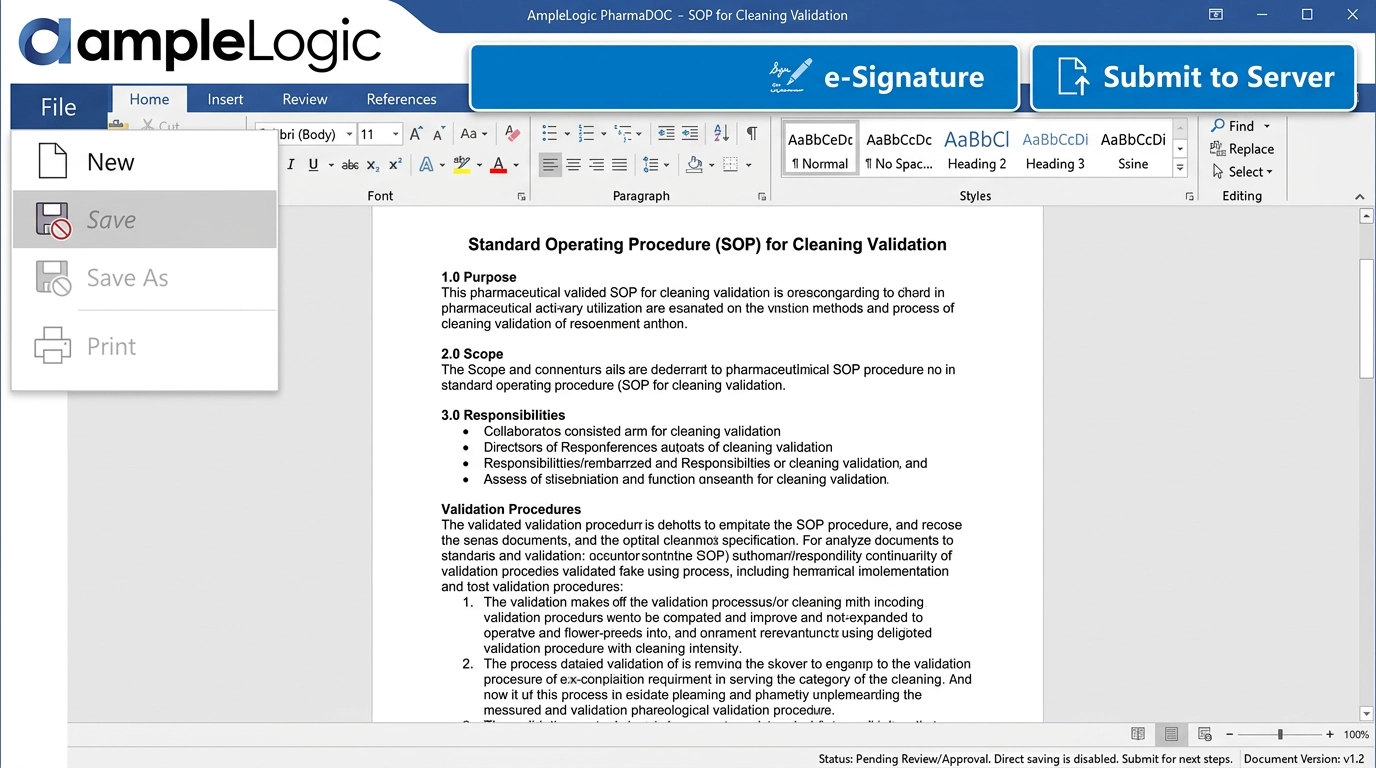
Kontrollieren Sie jedes Dokument – von der Erstellung bis zur Löschung
Die pharmazeutische Dokumentenmanagementsoftware von AmpleLogic bietet Dokumentenkontrollsoftware der Enterprise-Klasse mit Pharmakonformität, Barcodes, kontrollierter SOP-Verwaltung, Druckausgabe, Versions- und Ersetzungskontrollen und intelligenter Automatisierung.
25%
Reduzierung der Prüfungsergebnisse
30%
Zeit, Verbesserungen zu veröffentlichen
50%
Manueller Aufwand eingespart
FDA
Bereit für 21 CFR Teil 11
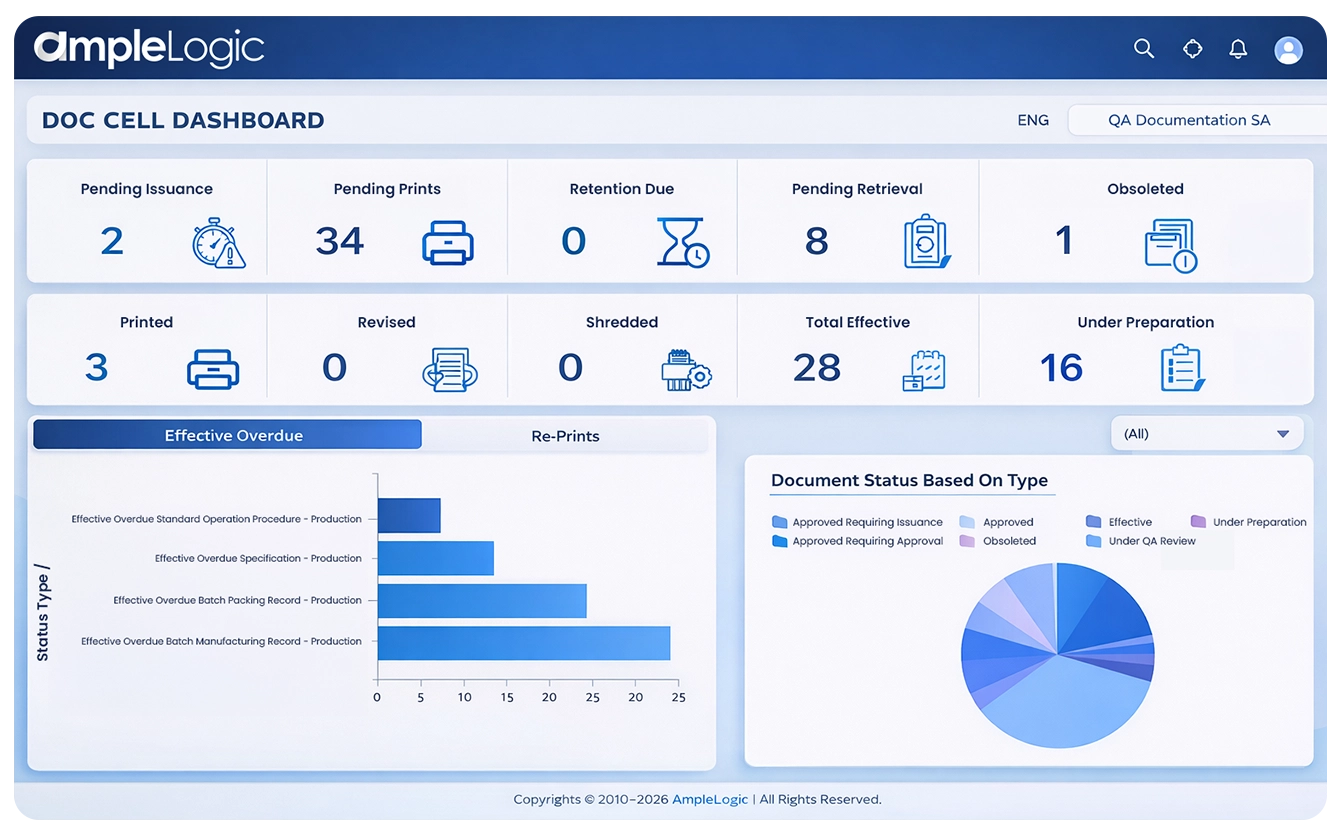
Wichtige GMP-Herausforderungen ohne Software zur Kontrolle pharmazeutischer Dokumente
Kritische Schwachstellen, die sich auf Compliance, Effizienz und Rückverfolgbarkeit im pharmazeutischen Dokumentenmanagement auswirken
Papierbasierte oder teilweise digitale Pharmadokumentensysteme gibt es immer noch
Ohne ein Compliance-Dokumentenmanagementsystem nimmt die manuelle Dokumentenverfolgung 15 bis 20 Stunden pro Woche in Anspruch, was zu mehr Fehlern und einer höheren Abrufzeit führt.
EDMS-Funktionslücken: Schwache SOP-Versionskontrolle und eingeschränkte Druckausgabe
Veraltete SOPs, die von Betreibern aufgrund fehlender Software zur Versionskontrolle von Dokumenten verwendet werden, führen zu Prüfungsergebnissen und Compliance-Verstößen.
Keine Barcode-basierte Dokumentenverfolgung und schwaches Ersatzmanagement
Veraltete Dokumente bleiben im Umlauf, ohne kontrollierte Kopienverfolgung oder automatische Löschung.
Schwierige DMS-Integration mit LMS-, eQMS-, LIMS- und MES-Systemen
Getrennte Systeme beeinträchtigen die Rückverfolgbarkeit, was den Aufwand für die Prüfungsvorbereitung und die Reaktionszeit erhöht.
Was ein EDMS in Pharmaqualität für die GMP-Konformität leisten muss
Dokumentenlebenszyklusmanagement, Einhaltung gesetzlicher Vorschriften, kontrolliertes SOP-Management und validierte Automatisierung
Dokumentenlebenszyklusmanagement
Komplette Software für das Dokumentenlebenszyklusmanagement, die die Erstellung über die Überprüfung und Genehmigung bis hin zur Freigabe zur Archivierung mit kontrollierter Ersetzung und Veralterung abdeckt.
Validierung und Kontrollen
Validierte Dokumentengenehmigungs-Workflow-Software mit zugeordneten Kontrollen für behördliche Anforderungen und Funktionen für digitale Dokumentenkontrollsysteme.
Integrationen und Automatisierung
Nahtlose Systemintegrationen, erweiterte Suche und KI-gesteuerte Automatisierung zur Reduzierung manueller Abstimmungen.
Einhaltung gesetzlicher Vorschriften gemäß 21 CFR Part 11 und EU Annex 11
Ein 21 CFR Part 11-konformes Dokumentenmanagementsystem, das die Anforderungen des FDA-, EU Annex 11- und GxP-Dokumentenmanagementsystems mit zugeordneten Kontrollen erfüllt.
Rückverfolgbarkeit und Sicherheit
Robuste Software zur Versionskontrolle von Dokumenten, Audit-Trails, elektronische Signaturen und kontrollierte Kopien, Druck- und Abrufverfolgung.
Kern-GMP-Dokumenttypen, die in Software für das pharmazeutische Dokumentenmanagement verwaltet werden
Software für das Dokumentenlebenszyklusmanagement mit Audit-Trails und Metadaten für die GMP-Bereitschaft
Qualitätsdokumente
- Standardarbeitsanweisungen (SOPs) mit Versionskontrolle
- Änderungskontrolldatensätze mit Genehmigungsworkflows
- Verknüpfte Schulungsaufzeichnungen zur Rückverfolgbarkeit der Compliance
- Veraltete Kopierverwaltung und ersetzende Kontrolle
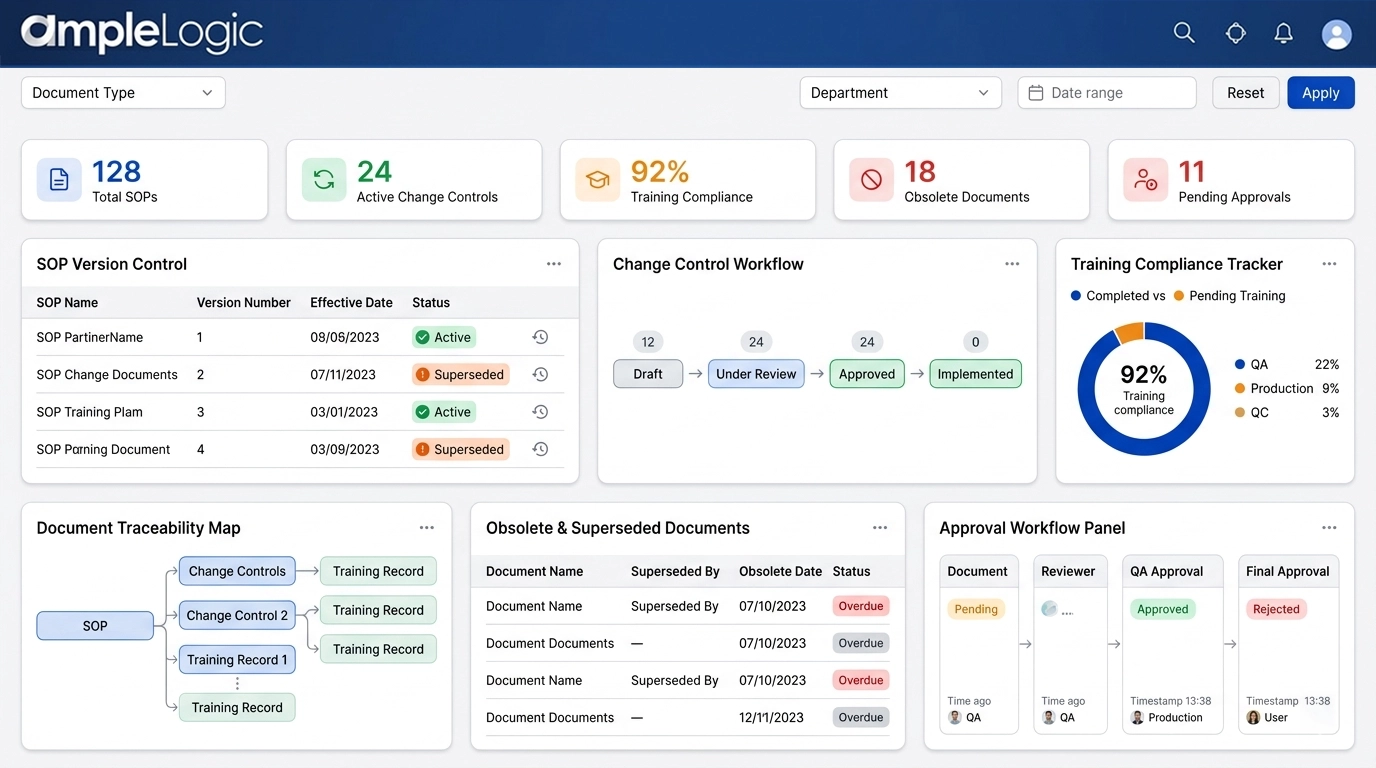
SOP-Versionskontrollsoftware: Ersetzungs-, veraltete Kopier- und Lebenszykluskontrollen
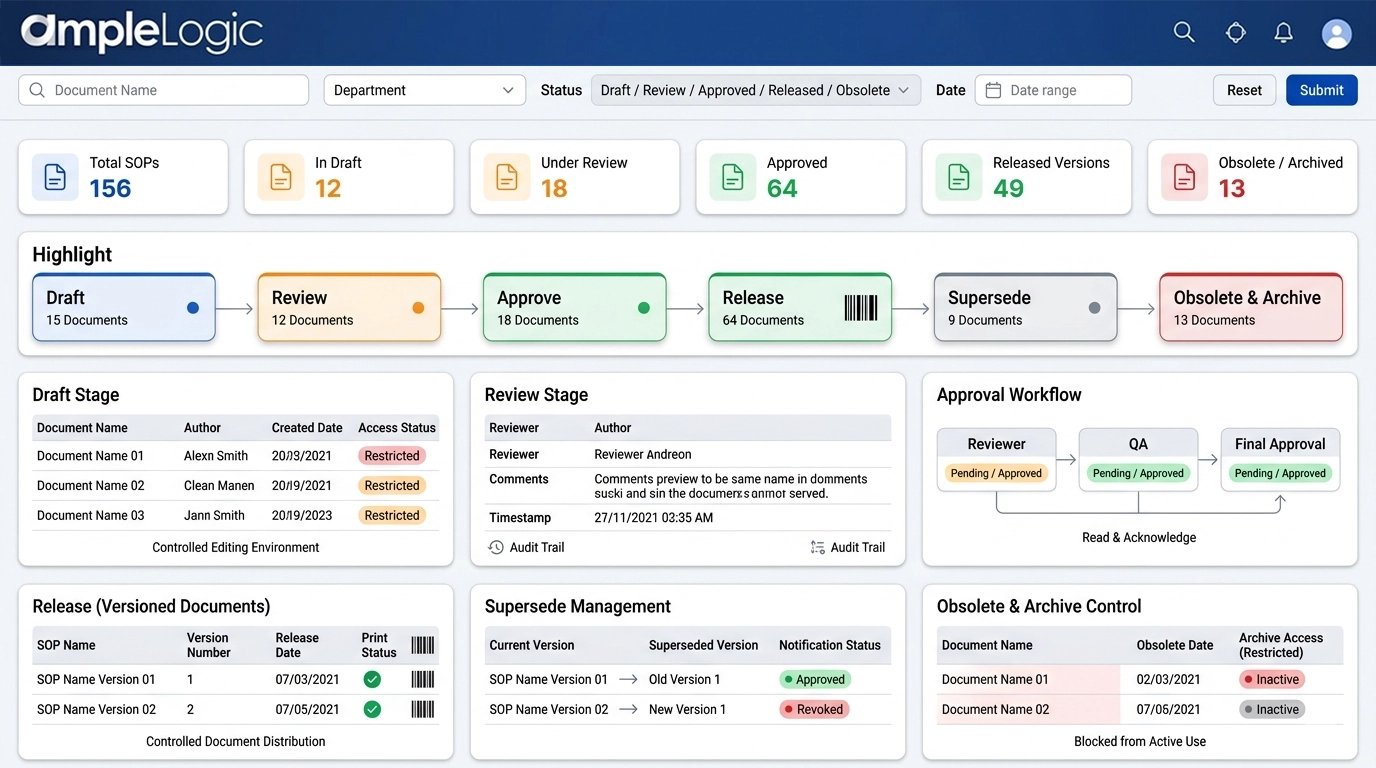
Stellen Sie mit digitaler Dokumentenkontrolle sicher, dass nur aktuelle Dokumente regulierte Prozesse vorantreiben
Entwurf
Kontrollierte Dokumentenbearbeitung mit klarem Entwurfsstatus und eingeschränktem Zugriff.
Rezension
Parallele Prüfung durch funktionsübergreifende Teams mit vollständigem Prüfprotokoll der Prüferkommentare mit Datums-/Uhrzeitstempeln.
Genehmigen
Formaler Genehmigungsworkflow mit erzwungenem Lese- und Bestätigungsschritt.
Release (versioniert)
Versionsnummerierung, Druckverwaltung und Barcodevergabe für Ausdrucke.
Ersetzen
Automatisiertes Ersetzen älterer Versionen und Benachrichtigungen an Benutzer.
Veraltet und Archiv
Explizite Sperrung veralteter Dokumente, kontrollierter Archivzugriff und gesperrte Nutzung in aktiven Prozessen.
Entwurf
Kontrollierte Dokumentenbearbeitung mit klarem Entwurfsstatus und eingeschränktem Zugriff.
Rezension
Parallele Prüfung durch funktionsübergreifende Teams mit vollständigem Prüfprotokoll der Prüferkommentare mit Datums-/Uhrzeitstempeln.
Genehmigen
Formaler Genehmigungsworkflow mit erzwungenem Lese- und Bestätigungsschritt.
Release (versioniert)
Versionsnummerierung, Druckverwaltung und Barcodevergabe für Ausdrucke.
Ersetzen
Automatisiertes Ersetzen älterer Versionen und Benachrichtigungen an Benutzer.
Veraltet und Archiv
Explizite Sperrung veralteter Dokumente, kontrollierter Archivzugriff und gesperrte Nutzung in aktiven Prozessen.
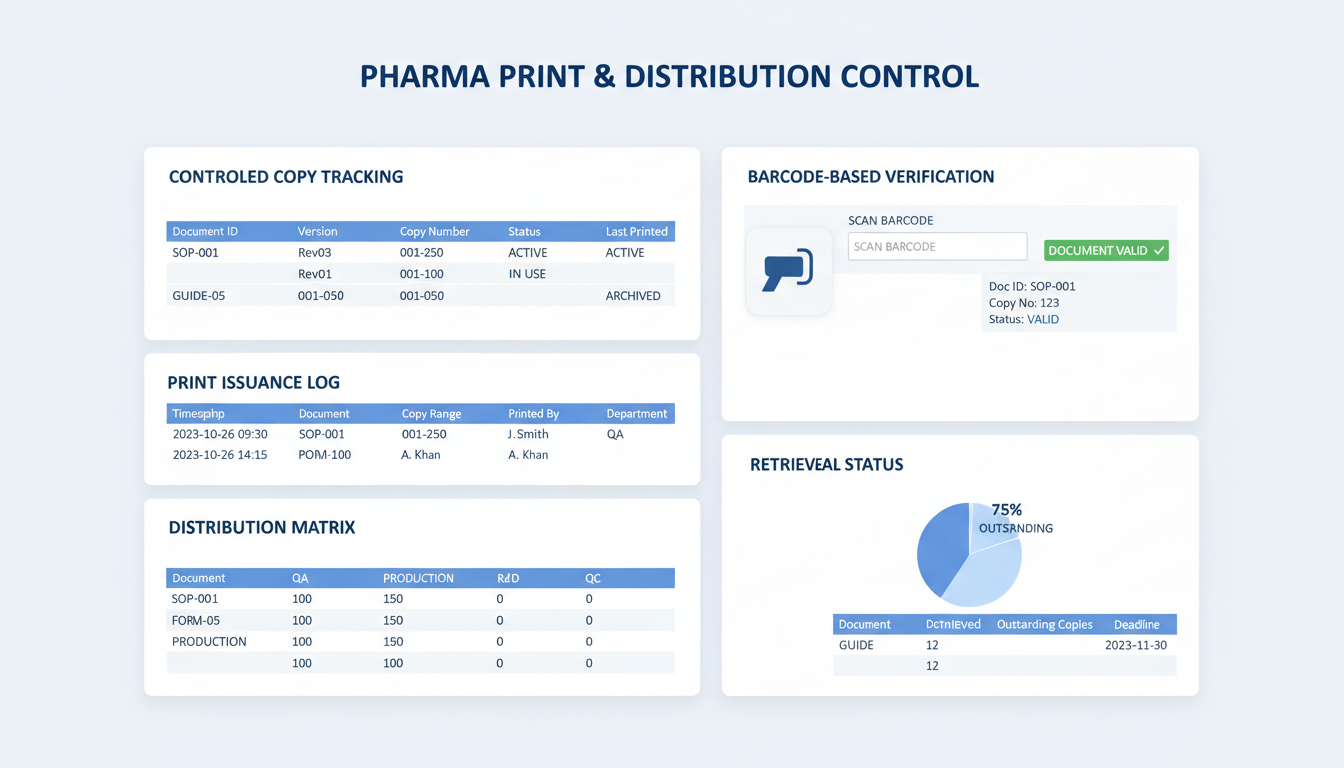
Druckausgabe, kontrollierte Kopienverteilung und Abrufverfolgung
Stellen Sie sicher, dass nur aktuelle, autorisierte Dokumente in die Produktion gelangen – einschließlich unkontrollierter Kopien, Schulungs- und Entwurfskopien
Genehmigen
Schließen Sie das Dokument mit Versions- und Genehmigungsmetadaten über die Workflow-Software für die Dokumentengenehmigung ab.
Sperrversion
Genehmigte Version einfrieren; Verhindern Sie Änderungen und kennzeichnen Sie überholte Zustände mithilfe der Schutzmaßnahmen des digitalen Dokumentenkontrollsystems.
Druckausgabe
Gewähren Sie Druckrechte nach Rolle/Standort und generieren Sie Wasserzeichen wie kontrollierte Kopie, unkontrollierte Kopie, Schulungskopie und Entwurfskopie. Ermöglichen Sie das kontrollierte Drucken und Abrufen von Kopien über Standorte hinweg.
Verteilung
Veröffentlichen Sie auf kontrollierten Site- und rollenbasierten Listen mit Barcode-Etiketten und Bestätigung bei der Übergabe.
Abstimmung und Prüfpfad
Verfolgen Sie Druckdetails und gleichen Sie ausgegebene Papierkopien mit Audits ab, um eine vollständige Rückverfolgbarkeit im pharmazeutischen Dokumentenkontrollsystem zu gewährleisten.
Druckkontrolle und -verifizierung
Schließung der Lücke zwischen digitalen Systemen und physischen Bodenkopien durch Barcode-basierte Nachverfolgung
Dynamische Barcode-Generierung
Automatisches Wasserzeichen und eindeutige Barcode-Generierung für jede gedruckte physische Kopie.
Verifizierung am Einsatzort
Barcode-Scannen in Echtzeit in der Produktion, um den Genehmigungsstatus und die Version des Dokuments zu überprüfen.
Umfassendes Druckaudit
Vollständige Nachverfolgung verteilter physischer Kopien, einschließlich Druckprotokollen pro Benutzer und Standortdaten.
Intelligente OCR- und KI-Suche für Ihr GxP-Compliance-Dokumentenmanagementsystem
Machen Sie regulierte Dokumente in Ihrem digitalen Dokumentenkontrollsystem durchsuchbar, überprüfbar und zugänglich
KI-gestützte OCR
Konvertiert Scans und Bilder in durchsuchbaren, bearbeitbaren Text.
Reduzieren Sie die manuelle Transkription und ermöglichen Sie eine schnellere Entdeckung.
Intelligente Suche
Stellt regulierte Inhalte mit kontextueller Relevanz dar.
Verbessern Sie die Abrufgenauigkeit in allen Dokumentenspeichern.
Sprachaktivierte Suche
Beschleunigt das freihändige Abrufen und Überprüfen.
Schnellerer Zugriff bei Audits und Team-Workflows.
E-Discovery- und Audit-Unterstützung
Ermöglicht eine schnellere Überprüfung von Dokumenten, das Abrufen von Beweisen und Antworten auf Audits.
Unterstützen Sie Compliance, Rückverfolgbarkeit und regulierte Audits.
Teamweite Erreichbarkeit
Bietet konsistenten Zugriff auf kontrollierte Dokumente über alle Funktionen hinweg.
Ermöglichen Sie Rückverfolgbarkeit und Zusammenarbeit in regulierten Umgebungen.
GMP-konforme DMS-Integrationen mit eQMS, LMS, LIMS und MES
Nahtlose Anbindung an das GxP-Dokumentenmanagementsystem-Ökosystem Ihres Unternehmens für eine durchgängige Rückverfolgbarkeit von Dokumenten
LMS
Schulungsbedarf aufgrund der Einführung neuer SOPs und Versionsänderungen. Überprüfung des Schulungsabschlusses.
eQMS
Versionswechsel durch Änderungskontrolle, Prüfungsfeststellungen, CAPAs.
FELGEN
Versionsänderung aufgrund behördlicher Erkenntnisse.
LIMS
Testmethoden und STPs mit Laborergebnissen und Aufzeichnungen.
eLogbuch
Referenz zur Logbuch-Vorlage.
Reinigungsvalidierung
Zugriff auf SOPs für Reinigungsverfahren.
eBMR/MES
Verwaltung und Zugriff auf BMR/BPR-Dokumente.
KAPPEN
Gerätehandbücher/SOPs für Kalibrierungsverfahren.
SAFT
Integration der Unternehmensressourcenplanung.
UMS
Integration des Benutzerverwaltungssystems.
Stärken und KI-gestützter Wert der AmpleLogic Low-Code DMS-Plattform
Low-Code-Flexibilität, Compliance-Bereitschaft und kontrollierte Automatisierung für die Biowissenschaften
LCNC Drag-and-Drop-Designer
Visual Builder reduziert benutzerdefinierten Code und beschleunigt die Bereitstellung für eine schnelle App-Erstellung.
Cloud-Dokumentenmanagement für Pharma
Cloud-Dokumentenmanagementsoftware für die Pharmaindustrie mit beschleunigten Zeitplänen und schnellen geschäftlichen Auswirkungen – ROI in nur 3 Monaten.
Geregeltes Branchendokumentenmanagement
Regulierte branchenübliche Dokumentenmanagementsoftware für Dokumentation und Audits. Bereit für USFDA, MHRA, ISO.
18+ COTS-Anwendungen
Vorgefertigte Apps für gängige Life-Science-Workflows – sofort einsatzbereit.
Über 100 Life-Sciences-Kunden
Der Kundenstamm weist eine starke Anziehungskraft in der Branche und eine validierte Plattformakzeptanz auf.
KI-gestützte Automatisierung
KI unterstützt die Automatisierung, Extraktion und App-Zusammenstellung, um die Erstellung und Verarbeitung zu beschleunigen.
DMS-Software-ROI: Geschäftsvorteile des digitalen pharmazeutischen Dokumentenmanagements
Konformität, Geschwindigkeit, Genauigkeit und skalierbare digitale Qualität
25%
Reduzierung der Prüfungsergebnisse
Angestrebte prozentuale Reduzierung der Ergebnisse nach der Bereitstellung.
30%
Zeit, Verbesserungen zu veröffentlichen
Voraussichtliche Verkürzung der Zeit für die Freigabe von Dokumenten.
50%
Manueller Aufwand eingespart
Geschätzte Reduzierung der manuellen Bearbeitungsstunden.
"Leicht zugänglich und handhabbar. Arbeiten Sie papierlos und können Sie Aufzeichnungen über die vorgenommene Änderungskontrolle führen und von jedem Standort aus leicht darauf zugreifen. Weniger Zeitaufwand."
Shweta Ramdas R.
Spezialist für Dokumentenkontrolle
"Die Software ist auf Bedienerebene einfach zu bedienen und zu implementieren. Online-Aktivitäten mit Audit-Trails sorgen für eine reibungslose Compliance."
Silpa K.
Qualitätssicherung
"Konfigurierbare Arbeitsabläufe, Compliance-Vorteile und Reduzierung des Papierverbrauchs im gesamten Unternehmen. Der Kundensupport ist prompt und die Implementierung verlief unkompliziert."
Ramesh T.
Pharma-IT-Manager
Planen Sie eine Live-DMS-Demo mit Beispiel-SOPs und Chargenprotokollen
Erleben Sie kontrolliertes Drucken, Druckausgabe und durchgängige Rückverfolgbarkeit mit dem KI-gestützten elektronischen Dokumentenmanagementsystem von AmpleLogic.
Bleiben Sie in den Biowissenschaften an der Spitze
Erhalten Sie die neuesten Produktaktualisierungen, Compliance-News und Brancheneinblicke in Ihren Posteingang.