Führen Sie intelligentere QC-Labore mit KI-gestütztem LIMS durch
Enterprise LIMS-Plattform und cloudbasiertes Laborinformationsmanagementsystem für Pharma, Biotechnologie und regulierte Biowissenschaften – bietet Labor-Workflow-Automatisierung, Instrumentenintegration und Einhaltung gesetzlicher Vorschriften mit eingebetteter KI, ISO 17025, Low-Code/No-Code-Bereitstellung und dem einzigen integrierten digitalen GxP-Ökosystem der Branche.
20%
Schnellere Abwicklung
25%
Mehr Samples/Shift
100%
Datenintegrität
Fast
3–6 Monate Bereitstellung
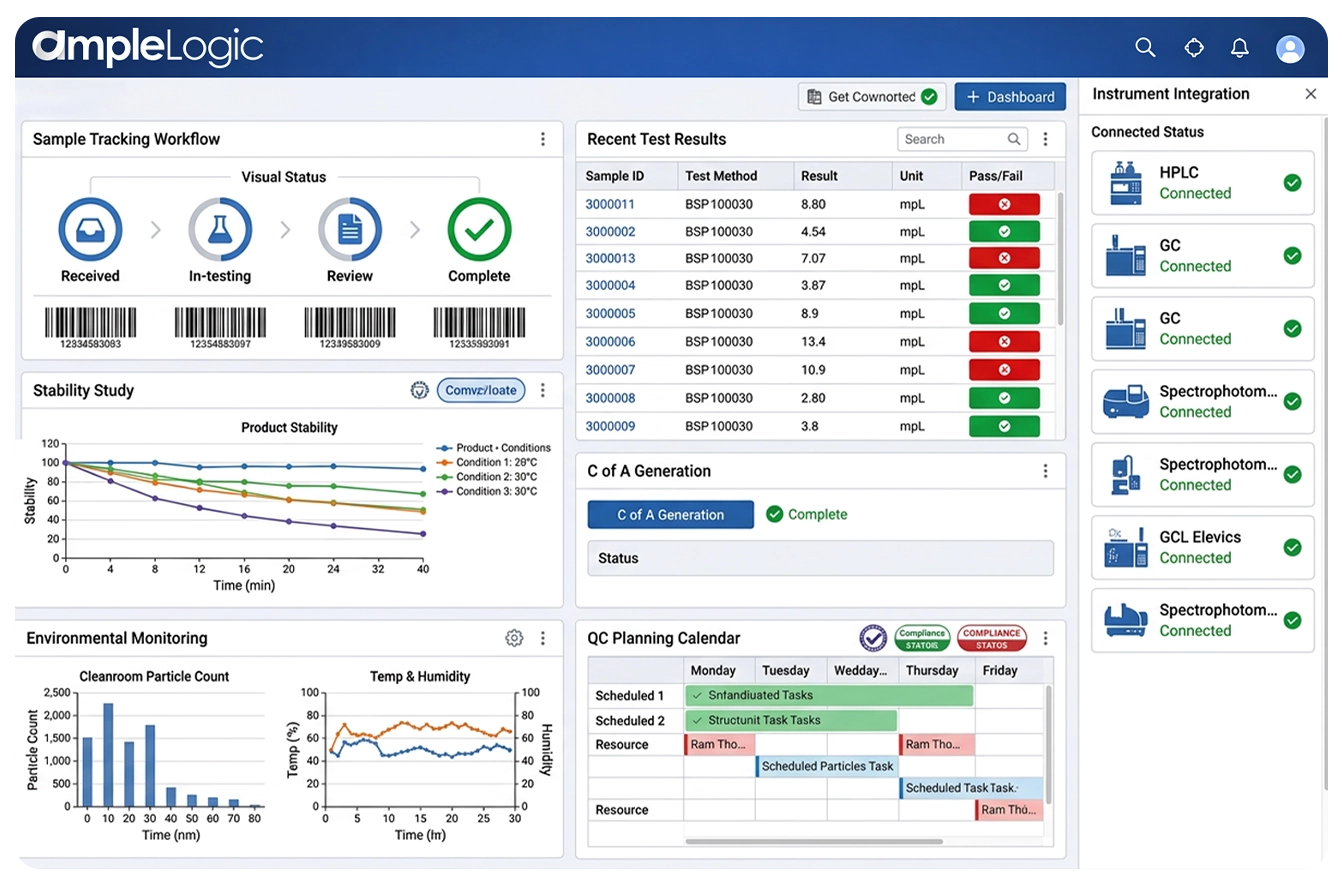
Vernetztes Laborökosystem: Einheitliche LIMS-Digitalplattform
AmpleLogic LIMS schafft eine einzige Quelle der Wahrheit für den Laborbetrieb – es eliminiert Datensilos, reduziert Übertragungsfehler und ermöglicht Echtzeittransparenz im gesamten Unternehmen als einheitliche Cloud-LIMS- und wissenschaftliche Datenverwaltungsplattform.
Analyseinstrumente
HPLC-, GC-, LC-MS-, ICP-OES-, UV-Vis-, Auflösungs- und Partikelanalysatoren, verbunden über validierte bidirektionale Schnittstellen
ERP-Systeme
Nahtlose Integration mit SAP, Oracle und NetSuite für Chargenfreigabe, Lagerbestand und Materialverwaltung
Fertigungsausführung
Echtzeit-Datenaustausch mit MES und eBMR für prozessbegleitende Tests, Chargenprotokolle und Produktionsplanung
Qualitätsmanagement
Bidirektionale Integration mit eQMS für Abweichungsauslösung, CAPA-Management und OOS-Untersuchungen
Chromatographie-Datensysteme
Vorgefertigte Konnektoren für Empower, Chromeleon, OpenLab und MassLynx mit automatisiertem Ergebnisimport
Dokumentenmanagement
Mit DMS synchronisierte SOPs, Analysemethoden und Spezifikationen für versionierten QC-Laborbetrieb
LIMS speziell für GxP-regulierte Labore entwickelt
Musterregistrierung
Automatisierte Probenanmeldung mit Barcode-/RFID-Scannen, Registrierung auf Chargenebene aus ERP/MES und konfigurierbare Probenpläne mit vordefinierten Testaufgaben
Probenverfolgung
Echtzeit-Chain-of-Custody mit Standortverfolgung, Speicherverwaltung, Halte-/Freigabestatus und automatischen Benachrichtigungen bei Annäherung an SLA-Fristen
Testausführung
Vorlagengesteuerte Ausführung analytischer Methoden mit Gerätedatenerfassung, Überprüfung der Systemeignung und Inline-Berechnungen mit konfigurierbaren Rundungsregeln
Ergebnisvalidierung
Automatisierte OOS/OOT-Erkennung, regelbasierte Pass/Fail-Bewertung, mehrstufige Prüf- und Genehmigungsworkflows mit elektronischen Signaturen
Analysezertifikat
Automatisch generierter COA/ROA mit konfigurierbaren Vorlagen, Aggregation auf Chargenebene, kundenspezifischen Formaten und digitaler Verteilung
Regulatorische Berichterstattung
Inspektionsfertige Datenexporte, Berichte zu Stabilitätstrends, statistische Analysepakete und formatierte Ausgaben für behördliche Einreichungen für FDA/EMA-Einreichungen
Musterregistrierung
Automatisierte Probenanmeldung mit Barcode-/RFID-Scannen, Registrierung auf Chargenebene aus ERP/MES und konfigurierbare Probenpläne mit vordefinierten Testaufgaben
Probenverfolgung
Echtzeit-Chain-of-Custody mit Standortverfolgung, Speicherverwaltung, Halte-/Freigabestatus und automatischen Benachrichtigungen bei Annäherung an SLA-Fristen
Testausführung
Vorlagengesteuerte Ausführung analytischer Methoden mit Gerätedatenerfassung, Überprüfung der Systemeignung und Inline-Berechnungen mit konfigurierbaren Rundungsregeln
Ergebnisvalidierung
Automatisierte OOS/OOT-Erkennung, regelbasierte Pass/Fail-Bewertung, mehrstufige Prüf- und Genehmigungsworkflows mit elektronischen Signaturen
Analysezertifikat
Automatisch generierter COA/ROA mit konfigurierbaren Vorlagen, Aggregation auf Chargenebene, kundenspezifischen Formaten und digitaler Verteilung
Regulatorische Berichterstattung
Inspektionsfertige Datenexporte, Berichte zu Stabilitätstrends, statistische Analysepakete und formatierte Ausgaben für behördliche Einreichungen für FDA/EMA-Einreichungen
Aktuelle LIMS-Softwarelandschaft
Den aktuellen Stand der Laborinformatiksoftware und LIMS-Plattformen in der Pharmaindustrie verstehen
Die meisten Labore verfügen bereits über ein LIMS
Weit verbreitete Basissystempräsenz
Bestehende LIMS sind stark angepasst und schwer zu aktualisieren
Maßgeschneiderte Integrationen sorgen für Reibungsverluste bei Upgrades
Hohe Wartungs- und Validierungskosten
Laufende Ausgaben für Wartung und behördliche Neuvalidierung
Es existieren mehrere Punktlösungen nebeneinander
Fragmentiertes Toolset erhöht den Integrationsaufwand
Prioritäten des QC-Laborleiters: Validierung und Gesamtbetriebskosten
Reduzieren Sie den Aufwand für die LIMS-Validierung + Konsolidieren Sie Einzellösungen, um die Gesamtbetriebskosten (TCO) langfristig zu senken.
Wichtigste Herausforderungen bei bestehender LIMS-Software
Fragmentierte Arbeitsabläufe, manuelle Prozesse und Compliance-Risiken
Konzentriert sich hauptsächlich auf die Probenverfolgung
Beschränkt die Sicht über den Ein- und Ausgang der Probe hinaus
- Beschränkt die End-to-End-Sichtbarkeit
- Erhöht manuelle Übergaben
- Erhöht das Compliance-Risiko
- Führt zu langsameren Produktveröffentlichungen
Stabilität und EMS werden außerhalb von LIMS behandelt
Fragmentierte Abläufe erhöhen die Komplexität und das Risiko
- Erstellt eine fragmentierte Betriebskontrolle
- Beschränkt den Geltungsbereich
- Erschwert die Validierung
- Antriebe müssen Ersatz prüfen
Tabellenkalkulationsabhängigkeit
Manuelle Prozesse untergraben Compliance und Effizienz
- Verursacht manuelle Statusaktualisierungen
- Schwächt Trending und Audit Trails
- Erhöht die Fehlerquote
- Macht Führungskräfte auf informelle Berichterstattung angewiesen
Schlechte Benutzererfahrung
Ältere Systeme verlangsamen die Einführung und Arbeitsabläufe
- Reduziert die Akzeptanz
- Verlangsamt tägliche Arbeitsabläufe
- Treibt Anpassungsherausforderungen voran
- Hebt Bedarf an Integrationsverbesserungen hervor
Herausforderungen bei der Instrumentenintegration
Instrumentensilos
HPLC-, GC-, LC-MS- und Mikrosysteme arbeiten getrennt
Manuelle Datenübertragung aus CDS
Chromatographie-Datensysteme erfordern manuelle Eingabeschritte
Risiken der Datenintegrität
Audit-Trail-Lücken und potenzielle Compliance-Verstöße
Komplexer Validierungsaufwand
Jede Verbindung erfordert umfangreiche Systemeignungstests
Priorisieren Sie validierte Konnektoren
Vorgefertigte, qualifizierte Instrumentenintegrationen reduzieren das Risiko
Priorisieren Sie die Audit-Trail-Unterstützung
Vollständige Rückverfolgbarkeit vom Instrument bis zum Bericht
Priorisieren Sie die Minimierung manueller Übergaben
Automatisieren Sie die Datenerfassung, um Fehler und Zykluszeiten zu reduzieren
Kernfunktionen der LIMS-Software
Speziell entwickelte pharmazeutische LIMS-Softwarefunktionen für das moderne Laborbetriebsmanagement
Beispiel-Lifecycle-Management
Probenverfolgungssoftware für Unternehmen, die ein durchgängiges Probenlebenszyklusmanagement von der Registrierung über die Analyse, Berichterstattung und Entsorgung bietet
Test- und Methodenausführung
Definieren und führen Sie Analyseverfahren mit vollständiger Rückverfolgbarkeit aus
Gerätekonnektivität
Instrumentenintegrationssoftware für nahtlose Konnektivität mit QC-Laborinstrumenten, Chromatographie-Datensystemen und LIMS ELN-Integration
Barcode- und RFID-Handhabung
Automatisierte Probenidentifizierung und Nachverfolgung des QC-Laborbestandsmanagements
Qualitätskontroll-Workflows
Integrierte QC-Prüfungen, Genehmigungen und Compliance-Überprüfungen auf der gesamten digitalen Laborplattform
Elektronische Signaturen und Audit Trails
FDA-konforme Laborsoftware mit vollständigen 21 CFR Part 11-, GxP-konformen LIMS- und ISO 17025-konformen LIMS-Anforderungen
Anpassbare Berichterstattung
Laboranalyseplattform mit flexiblem COA, ROA, Laborleistungsanalysen und behördlicher Berichtserstellung
Intuitive Dashboards
Echtzeit-Dashboards für das Laborbetriebsmanagement mit KPIs, wissenschaftlichen Datenanalysen und Laborleistungsanalysen
Erweiterte LIMS-Module für Pharmalabore
Speziell entwickelte LIMS-Lösungen für spezialisierte Laborbetriebe
Erweitertes Stabilitätsmanagement
ICH-konforme Software zur Verwaltung von Stabilitätsstudien für Pharma und Biotechnologie
AmpleLogic Advanced Stability Management ist ein speziell entwickeltes Managementsystem für Stabilitätstests zur Verwaltung des gesamten Lebenszyklus von Stabilitätsstudien – von der Erstellung des Stabilitätsprotokolls und der Planung der Probenentnahme über die Verwaltung der Kammerlagerung, die Testdurchführung, die Stabilitätstrendanalyse bis hin zur behördlichen Berichterstattung.
Hauptmerkmale
Erstellung eines Stabilitätsprotokolls
Definieren Sie ICH Q1A-konforme Stabilitätsprotokolle mit konfigurierbaren Studiendesigns, Lagerbedingungen, Akzeptanzkriterien und automatisierten Probenahmeplänen
Stabilitätsprobenplanung
Automatisierte Probenentnahmeplanung mit kalenderbasierten Erinnerungen, dynamischer Neuplanung und vollständigen Prüfprotokollen
Kammer- und Umweltüberwachung
Überwachen Sie Stabilitätslagerbedingungen wie Temperatur und Luftfeuchtigkeit in Stabilitätskammern und Lagerhäusern
Testausführung und Datenerfassung
Führen Sie analytische Tests innerhalb desselben LIMS-Workflows mit direkter Geräteintegration und vollständiger Rückverfolgbarkeit durch
Stabilitätstrendanalyse und Berichterstattung
Automatisierte statistische Trendanalyse mit Anpassung der Abbaukurve, Kontrolldiagrammen und aufsichtsrechtlich geeigneten Stabilitätsberichten
KI-gestützte Haltbarkeitsbestimmung
Durch maschinelles Lernen gesteuerte Haltbarkeitsprognose mit Konfidenzintervallen, frühen Warnmeldungen zum Ablaufrisiko und beschleunigter Stabilitätsvorhersage
Ablaufbestimmung und Verwaltung des Datums für erneute Tests
Systematische Ablaufbestimmung basierend auf Stabilitätstrenddaten, Berechnung des Wiederholungstestdatums und automatisierte Unterstützung für Etikettenansprüche
Einhaltung der ICH Q1A-Vorschriften
Integrierte Ausrichtung an den ICH Q1A-Q1F-Stabilitätsrichtlinien für pharmazeutische und biotechnologische Stabilitätsprogramme
Einhaltung der FDA-Stabilitätsanforderungen
Vorkonfigurierte Arbeitsabläufe erfüllen die Stabilitätsanforderungen der FDA, einschließlich 21 CFR Part 211.166
GMP-Stabilitätsprogramm-Management
Umfassende GMP-Stabilitätsprogramme mit fortlaufenden Stabilitätsverpflichtungen und Überwachung nach der Zulassung
Stabilitätstrendanalyse und Haltbarkeitsvorhersage
KI analysiert Stabilitätstestergebnisse, um Produktverschlechterungstendenzen zu erkennen und die Haltbarkeit des Produkts abzuschätzen
Hauptvorteile
Beschleunigen Sie die Durchführung von Stabilitätsstudien mit automatisierter Planung und Protokollverwaltung
Reduzieren Sie die Zeit zur Bestimmung der Haltbarkeit um 40 % mit KI-gesteuerter Trendanalyse
Stellen Sie die vollständige Einhaltung gesetzlicher Vorschriften mit ICH Q1A-, FDA- und GMP-ausgerichteten Arbeitsabläufen sicher
Vermeiden Sie verpasste Probenentnahmen mit der automatisierten Probenentnahmeplanung
Zentralisieren Sie die Kammerlagerverwaltung mit Echtzeit-Umgebungsüberwachung
11 KI-Funktionen verändern pharmazeutische LIMS-Abläufe
Von der KI-gestützten Referenzstandardüberprüfung und virtuellen QC-Laborassistenten bis hin zu vorausschauender Wartung und OCR-Dokumentenverarbeitung – AmpleLogic LIMS integriert intelligente Automatisierung in jeden Laborarbeitsablauf
Überprüfung des KI-Referenzstandardkatalogs für Pharmalabore
KI verifiziert automatisch den Referenzstandardkatalog und vergleicht ihn mit derzeit im Labor verwendeten Standards. Dabei werden aktualisierte, abgelaufene, versionierte und neu verfügbare Standards identifiziert, um die Einhaltung gesetzlicher Vorschriften sicherzustellen.
- Gewährleistet die korrekte Verwendung des Referenzstandards
- Verhindert veraltete Standardnutzung
- Automatisierte Katalogaktualisierungen und Versionsverfolgung
KI-Laborassistent (LIMS-MAN): Virtueller LIMS-Trainer
Intelligenter virtueller Assistent integriert in die LIMS-Plattform. Benutzer interagieren mit Abfragen in natürlicher Sprache wie „Wie ist der Status von Charge B12345?“ oder „Testergebnisse für Produkt X anzeigen“ – Labordaten sofort abrufen und als virtueller Trainer für neue Benutzer fungieren.
- Schnellerer Zugriff auf Laborinformationen
- Reduzierte Schulungszeit für neue Benutzer
- Vereinfachte LIMS-Navigation und Entscheidungsfindung
KI-gesteuerte automatisierte Arbeitsblattvorbereitung für QC-Labore
KI analysiert STP-Daten (Standard Test Procedure) – einschließlich Testparameter, Berechnungsformeln, erforderliche Reagenzien, Gerätedetails und Akzeptanzkriterien –, um dynamisch gebrauchsfertige digitale Arbeitsblätter für Analysten zu generieren.
- Automatische Generierung von Testarbeitsblättern aus STP-Daten
- Intelligentes Auffüllen von Berechnungsfeldern
- Beseitigung von Übertragungsfehlern
KI-Ressourcenoptimierungs-Engine für den Laborbetrieb
Der KI-gestützte Ressourcenoptimierer analysiert historische Testdaten und prognostiziert zukünftige Laboranforderungen – indem er die erforderlichen Reagenzien, Referenzstandards, Verbrauchsmaterialien und Gerätenutzungszeit für kommende Chargen schätzt.
- Genaue Beschaffungsplanung und Bestandsverwaltung
- Weniger Reagenzienmangel und Abfall
- Optimierte Instrumentennutzung und Kostenreduzierung
Automatisierte KI-Ergebnisüberprüfung und Trendanalyse (virtueller Prüfer)
Der KI-gesteuerte virtuelle Prüfer analysiert kontinuierlich analytische Daten – er erkennt Fehler während der Analyse, überprüft automatisch Audit-Trails, identifiziert abnormale Trends, Datenintegritätsprobleme, OOT-Ergebnisse und markiert Abweichungen von der Analysemethode.
- Schnellere Ergebnisüberprüfung mit KI-gesteuerten Erkenntnissen
- Frühzeitige Erkennung von Qualitätsproblemen und OOT-Trends
- Reduzierter Arbeitsaufwand für manuelle Überprüfungen
KI-basierte Chromatogrammauswertung für HPLC, GC und UPLC
KI wertet Chromatogramme von HPLC-, GC- und UPLC-Geräten aus und bewertet automatisch Peakflächen, Retentionszeiten, Peaksymmetrie, Auflösung und Standardabweichungen. Benachrichtigt Analysten sofort, wenn Abweichungen von Standardmustern festgestellt werden.
- Automatisierte chromatographische Datenüberprüfung
- Erkennung abnormaler Spitzen und Integrationsprobleme
- Automatisierung der prozessbegleitenden Überprüfung von Mustersätzen
KI-gesteuerte Stabilitätsvorhersage und Haltbarkeitsvorhersage
Algorithmen für maschinelles Lernen analysieren historische Stabilitätsstudiendaten, um zukünftiges Produktverhalten vorherzusagen – und schätzen die Haltbarkeit, Abbautrends, Stabilitätsschwankungswahrscheinlichkeiten und das Risiko von Spezifikationsfehlern ein.
- Frühzeitige Erkennung potenzieller Stabilitätsprobleme
- Datengesteuerte Haltbarkeitsvorhersagen mit Konfidenzintervallen
- Verbesserte regulatorische Dokumentation für Stabilitätsprogramme
Vorhersage von KI-Instrumentenausfällen und vorausschauende Wartung
KI überwacht kontinuierlich die Leistungsdaten der Instrumente – Kalibrierungsaufzeichnungen, Nutzungsstunden, Fehlerprotokolle, Wartungshistorie und Leistungstrends – mithilfe prädiktiver Analysen, um Ausfallrisikoniveaus abzuschätzen und Instrumentenrisikobewertungen zu generieren.
- Vorausschauende Wartungswarnungen vor Ausfällen
- Reduzierte Ausfallzeiten und Verzögerungen der Instrumente
- Optimierte Wartungsplanung
KI-gestützte Probenahmezeitschätzung für die pharmazeutische Qualitätskontrolle
Die KI-Engine analysiert historische Probenahmedaten basierend auf Produkttyp, Materialkategorie, Anzahl der Behälter, Chargengröße und Komplexität des Probenahmeverfahrens, um die erwartete Probenahmezeit für jede Charge abzuschätzen.
- Verbesserte Laborplanung und Personalplanung
- Reduzierte Verzögerungen bei der Probenentnahme
- Erhöhte betriebliche Effizienz
OCR-fähige Dokumentenverarbeitung für Labordaten
Die optische Zeichenerkennung (OCR) extrahiert automatisch Informationen aus hochgeladenen Dokumenten – einschließlich PDFs, Bildern, gescannten Berichten, Zertifikaten und handschriftlichen Aufzeichnungen – und wandelt sie in strukturierte digitale Aufzeichnungen um, die in die LIMS-Datenbank integriert werden.
- Automatisierte Datenextraktion aus gescannten Dokumenten
- Eliminierung der manuellen Dateneingabe
- Schnellere Dokumentenverarbeitung und verbesserte Zugänglichkeit
KI-Probentests, TAT-Vorhersage für die Laboreffizienz
KI analysiert historische Testdauern und prognostiziert die erwartete Abschlusszeit für jede Probe – unter Berücksichtigung der Komplexität der Testmethode, der Instrumentenverfügbarkeit, der Arbeitsbelastung der Analysten und der historischen Testdauer für eine genaue TAT-Prognose.
- Genaue Prognose der Bearbeitungszeit
- Verbesserte Probenplanung und Priorisierung
- Erhöhte Laborproduktivität
LIMS-Workflow-Architektur
Durchgängige Automatisierung der Arbeitsabläufe im Labor von der Probenaufnahme bis zur behördlichen Berichterstattung
Stammdaten
Produkte, Methoden, Instrumente, Benutzer, Standards
Stabilität
Studien & Haltbarkeit
Qualifikation
IQ/OQ/PQ-Validierung
COA/ROA
Regulatorisch
Stammdaten
- •Produkte
- •Methoden
- •Instrumente
- •Benutzer
- •Qualitätsstandards
Hilfsmanagement
- •Vermögensverwaltung
- •Verfolgung von Chemikalien und Reagenzien
- •Spaltenverwaltung
- •Referenzstandards
- •Lösungsvorbereitung
- •Medienmanagement
- •Kulturmanagement
Beispiellebenszyklus
- •Musterregistrierung
- •Abholung und Empfang
- •Melden Sie sich beim System an
- •Zuordnung zu Tests
- •Analyseausführung
- •Ergebnisüberprüfung und -genehmigung
- •Analysezertifikat (COA)
Regulatorischer Output
- •Analysezertifikat (COA)
- •Analysebericht (ROA)
- •Zulassungsanträge
LIMS-Datenintegrität und Einhaltung gesetzlicher Vorschriften
ALCOA+-Datenintegrität, 21 CFR Part 11, EU Annex 11, ISO 17025 und GxP-Konformität – integriert in die AmpleLogic Enterprise LIMS-Plattform
ALCOA+ Datenintegritäts-Framework
Jeder Datenpunkt ist zuordenbar, lesbar, zeitnah, originell und genau – mit in die Plattform integrierten vollständigen, konsistenten, dauerhaften und verfügbaren Erweiterungen.
- Unveränderliche Prüfpfade für jede Datenänderung
- Elektronische Signaturen mit Absicht und Bedeutung
- Automatisierte Sicherung mit Validierung der Datenwiederherstellung
- Manipulationssichere Datenspeicherarchitektur
Konformität mit FDA 21 CFR Part 11
Vorvalidierte elektronische Aufzeichnungen und Signaturen mit geschlossenen Systemkontrollen, Behördenprüfungen und Geräteverifizierung für von der FDA regulierte Labore.
- Konfigurierbare elektronische Signatur-Workflows
- Berechtigungsprüfungen und rollenbasierte Zugriffskontrolle
- Mit Zeitstempel versehene, zuordenbare Prüfaufzeichnungen
- Sicherheitsarchitektur mit geschlossenem System
Einhaltung von EU-Anhang 11
Computergestützte Systemkontrollen für die europäische Arzneimittelherstellung, einschließlich Validierungsanforderungen, Datenspeicherung, Ausdrucke und Geschäftskontinuität.
- Unterstützung der computergestützten Systemvalidierung (IQ/OQ/PQ)
- Datenmigrations- und Archivierungskontrollen
- Geschäftskontinuität und Notfallwiederherstellung
- Dokumentation zur Lieferantenqualifikation
Einhaltung der GxP-Vorschriften
Umfassende Einhaltung bewährter Praktiken in GLP-, GMP- und GCP-Umgebungen mit integrierten Kontrollen für ICH, WHO, PIC/S und über 16 globale Gesundheitsbehörden.
- GLP-, GMP- und GCP-Workflow-Vorlagen
- Ausrichtung der ICH-Richtlinien Q2, Q7, Q10
- Inspektionsfertige Berichtspakete
- Unterstützung bei Änderungskontrolle und Revalidierung
Integriertes digitales GxP-Ökosystem für Pharma- und Biotech-Labore
Das pharmazeutische LIMS von AmpleLogic lässt sich nativ in 13 GAMP-Lösungen integrieren – ein Wettbewerbsvorteil, den kein anderer Anbieter erreichen kann
OOS-Ergebnisse Auto-Trigger-Abweichungen; CAPA-Ergebnisse aktualisieren Testmethoden; Änderungskontrollen verwalten Aktualisierungen analytischer Verfahren
Bidirektional: OOS → Abweichungen, CAPAs → Methodenaktualisierungen
Stabilitätsdaten und COAs fließen direkt in die Zulassungsanträge ein; Der Registrierungsstatus aktualisiert die Probentestanforderungen
LIMS → Stabilitätsdaten → RIMS-Einreichungen
In-Prozess-Proben werden automatisch aus Chargenprotokollen erstellt; QC-Ergebnisse lösen Entscheidungen zur Chargenfreigabe aus; Chargenbezogene Umweltdaten
Bidirektional: Chargenproben ↔ QC-Ergebnisse
QC-Trenddaten, Stabilitätsergebnisse und OOS-Statistiken füllen die jährlichen Produktbewertungsberichte automatisch aus, ohne dass eine manuelle Zusammenstellung erforderlich ist
LIMS → QC-Trends + OOS-Statistiken → APQR-Berichte
SOPs, Analysemethoden und Spezifikationen versioniert im DMS; Effektive Dokumente werden bei der LIMS-Testausführung automatisch verknüpft
DMS → Kontrollierte Dokumente → LIMS-Methodenausführung
Überprüfung der Qualifikationen des Analysten vor der Testdurchführung; Nach Abschluss der Schulung wird der Zugriff auf die Analysemethode automatisch aktiviert
LMS → Schulungsstatus → LIMS-Analystenqualifikation
In-Prozess- und Release-Testdaten speisen CPV-Statistikmodelle für die kontinuierliche Überwachung der Prozessfähigkeit ein
LIMS → Prozessdaten → CPV-Statistikanalyse
Mit Produktionschargen verknüpfte Reinraumüberwachungsdaten; Exkursionen lösen automatisierte Halte-/Freigabe-Workflows im LIMS aus
EMS → Umweltdaten → LIMS Chargensperre/-freigabe
Im Gegensatz zu älteren LIMS-Anbietern für Unternehmen, die sich auf Forschung und Entwicklung konzentrieren oder auf modularen Analysen basieren, ist AmpleLogic der einzige Anbieter, der ein vollständiges, nativ integriertes GxP-Ökosystem bietet, in dem LIMS-Daten ohne Middleware nahtlos über Qualitäts-, Regulierungs-, Fertigungs- und Compliance-Systeme fließen.
Unternehmens-LIMS-Integration: ERP, ELN und Gerätekonnektivität
Verbinden Sie die LIMS-Plattform Ihres Unternehmens mit Ihrem gesamten betrieblichen Ökosystem
Laborinstrumente
Nahtlose Konnektivität mit Analysegeräten
- Massenspektrometrie (MS)
- HPLC
- GC
- ICP-OES
- UV-Vis
Unternehmenssysteme
Integration mit Geschäfts- und Fertigungssystemen
- SAFT
- Orakel
- NetSuite
- MES (Manufacturing Execution System)
- QMS (Qualitätsmanagementsystem)
- DMS (Dokumentenmanagementsystem)
- ELN (Elektronisches Labornotizbuch)
Daten und Analysen
Stellen Sie eine Verbindung zu Data Warehouses und Business Intelligence her
- Data Warehouses
- BI-Plattformen (Business Intelligence).
- KI/ML-Engines
- Cloud-Analyse
Konnektivitätsoptionen
Mehrere Protokolle für flexible Integration
- Über 100 vorgefertigte Anschlüsse
- REST-APIs
- SFTP
- Direkte Datenbankverbindungen
- HL7 (Gesundheitsprotokolle)
API-First-Architektur
Moderne, erweiterbare Plattform für individuelle Integrationsanforderungen
- RESTful-APIs
- Webhook-Unterstützung
- Benutzerdefinierte Anschlüsse
- Integrations-Frameworks von Drittanbietern
Automatisierte LIMS-Compliance: Eliminieren Sie sich wiederholende manuelle Überprüfungen
Die Automatisierungsplattform reduziert den Aufwand für die manuelle Überprüfung
Automatisierte regelbasierte Überprüfungen
Eliminieren Sie manuelle QC-Prüfungen durch konfigurierbare Geschäftslogik und Compliance-Regeln
Vorlagengesteuerte Methodenausführung
Vorkonfigurierte Vorlagen sorgen für eine konsistente Ausführung und reduzieren die manuelle Konfiguration
Echtzeit-Instrumentenqualifikationsstatus
Automatische Verfolgung der Systemeignung und Wartungspläne
Stammdatenharmonisierung
Eine zentrale Informationsquelle für Standards, Methoden und Verfahren im gesamten QC-Labor
Ausnahmegesteuerte Bewertungen
Konzentrieren Sie die Aufmerksamkeit der Analysten auf Abweichungen und Ergebnisse, die nicht den Spezifikationen entsprechen
End-to-End-Prozessablauf
Automatisierte Weiterleitung von Proben und Ergebnissen durch den gesamten Laborablauf
LIMS-Software-ROI: Messbare geschäftliche Auswirkungen für Qualitätslabore
Echte Ergebnisse der LIMS-Transformation
+25%
Auswirkungen auf die Zykluszeit
-20%
Durchsatzverlust
+30%
Compliance-Arbeitsbelastung
20%
TAT-Reduzierung
20 % schnellere Bearbeitungszeit für Analyseergebnisse
25%
Produktivitätssteigerung
25 % mehr Proben werden pro Analystenschicht verarbeitet
90%
Audit-Bereitschaft
90 % kürzere Zeit bis zum Abschluss von Beobachtungen
Die versteckten Kosten von Legacy-LIMS
Leerlaufzeit der Ausrüstung
Zwischen manuellen Umstellungen bleiben die Instrumente ungenutzt
10–30 % Kapazitätsverlust
Engpass bei Analysten
Manuelle Überprüfungen und Genehmigungen verlangsamen die Ergebnisbereitstellung
Verzögerungen bei der Probenbearbeitung
Systemübergreifende Datensilos
ELN, MES und CDS arbeiten unabhängig voneinander
Manuelle Konsolidierung und Fehlerrisiko
Wiederholte manuelle Überprüfungen
Bei jedem Schritt werden identische Überprüfungen durchgeführt
+25 % Zykluszeitinflation
Validierungs- und Änderungskontrollaufwand
Bei Systemänderungen sind umfangreiche Tests erforderlich
+30 % Compliance-Aufwand
Wie intelligentes Low-Code-LIMS traditionelle Plattformen übertrifft
Direkter Vergleich der Bereitstellungsansätze
| Dimension | Legacy Monolithisch | Traditionell modular | Intelligenter Low-Code |
|---|---|---|---|
| Zeitplan für die Implementierung | 18-24 Monate | 12-18 Monate | 3-6 Monate |
| Gesamtbetriebskosten (TCO) | 2,5-3,5 Mio. $ | 1,8–2,5 Millionen US-Dollar | 1,0–1,5 Mio. USD |
| KI und Analytik | Legacy, beschränkt auf die Berichterstattung | Zusatzfunktionen, zusätzliche Kosten | Eingebettete KI, native prädiktive Analysen |
| Anpassung und Flexibilität | Hartcodiert, hoher Änderungskontrollaufwand | Modular, erfordert aber Entwickler | Low-Code/No-Code, Geschäftsbenutzer können konfigurieren |
Zeitplan für die Implementierung
Vermächtnis: 18-24 Monate
Traditionell: 12-18 Monate
Intelligent: 3-6 Monate
Gesamtbetriebskosten (TCO)
Vermächtnis: 2,5-3,5 Mio. $
Traditionell: 1,8–2,5 Millionen US-Dollar
Intelligent: 1,0–1,5 Mio. USD
KI und Analytik
Vermächtnis: Legacy, beschränkt auf die Berichterstattung
Traditionell: Zusatzfunktionen, zusätzliche Kosten
Intelligent: Eingebettete KI, native prädiktive Analysen
Anpassung und Flexibilität
Vermächtnis: Hartcodiert, hoher Änderungskontrollaufwand
Traditionell: Modular, erfordert aber Entwickler
Intelligent: Low-Code/No-Code, Geschäftsbenutzer können konfigurieren
AmpleLogic LIMS: Marktpositionierung und Wettbewerbsvorteil
Wie AmpleLogic im Vergleich zu etablierten LIMS-Anbietern abschneidet
| Kategorie | Anbieterinnen | Positionierung | Einschränkung |
|---|---|---|---|
| Legacy Enterprise LIMS | Traditionelle Anbieter | Hochgradig konfigurierbar, etablierter Pharma-Kundenstamm, breite Instrumentenunterstützung | Bereitstellungszeit für 18–24 Monate, umfangreiche Anpassung erforderlich, hohe Gesamtbetriebskosten, kein integriertes GxP-Ökosystem |
| Forschungs- und Entwicklungsplattformen für Unternehmen | Auf Forschung und Entwicklung ausgerichtete Anbieter | Molekulare Modellierung + Laborinformatik, Cloud-Plattformen, KI/GenAI-Assistenten | F&E konzentriert sich nicht auf Qualitätssicherung, teuer, Anbieterbindung an geschlossene Ökosysteme, begrenzte Fertigungsintegration |
| Moderne digitale Laborplattformen | Cloud-native Startups | Cloud-native, moderne UX, API-first, schnelle Bereitstellung für Forschung und Entwicklung | Begrenzte Pharma-QC-Funktionen, unzureichende Einhaltung gesetzlicher Vorschriften, nicht GMP-validiert für die Herstellung |
| Modular Analytics LIMS | Analytics-First-Anbieter | Integrierte Analyse/ML, Cloud-natives HTML5, integrierter LIMS+ELN+LES+SDMS-Stack | Komplexe Implementierung, begrenztes GxP-Ökosystem und KI-Funktionen erfordern einen Validierungsaufwand |
| Integrierte GxP-Plattform | AmpleLogic | KI-gesteuerte Laborinformatik + komplettes digitales GxP-Ökosystem (13 GAMP-Lösungen), Low-Code/No-Code, 3–6 Monate Bereitstellung | Referenzbasis für neuere Marktteilnehmer im Baugewerbe |
Legacy Enterprise LIMS
Traditionelle AnbieterPositionierung: Hochgradig konfigurierbar, etablierter Pharma-Kundenstamm, breite Instrumentenunterstützung
Einschränkung: Bereitstellungszeit für 18–24 Monate, umfangreiche Anpassung erforderlich, hohe Gesamtbetriebskosten, kein integriertes GxP-Ökosystem
Forschungs- und Entwicklungsplattformen für Unternehmen
Auf Forschung und Entwicklung ausgerichtete AnbieterPositionierung: Molekulare Modellierung + Laborinformatik, Cloud-Plattformen, KI/GenAI-Assistenten
Einschränkung: F&E konzentriert sich nicht auf Qualitätssicherung, teuer, Anbieterbindung an geschlossene Ökosysteme, begrenzte Fertigungsintegration
Moderne digitale Laborplattformen
Cloud-native StartupsPositionierung: Cloud-native, moderne UX, API-first, schnelle Bereitstellung für Forschung und Entwicklung
Einschränkung: Begrenzte Pharma-QC-Funktionen, unzureichende Einhaltung gesetzlicher Vorschriften, nicht GMP-validiert für die Herstellung
Modular Analytics LIMS
Analytics-First-AnbieterPositionierung: Integrierte Analyse/ML, Cloud-natives HTML5, integrierter LIMS+ELN+LES+SDMS-Stack
Einschränkung: Komplexe Implementierung, begrenztes GxP-Ökosystem und KI-Funktionen erfordern einen Validierungsaufwand
Integrierte GxP-Plattform
AmpleLogicPositionierung: KI-gesteuerte Laborinformatik + komplettes digitales GxP-Ökosystem (13 GAMP-Lösungen), Low-Code/No-Code, 3–6 Monate Bereitstellung
Einschränkung: Referenzbasis für neuere Marktteilnehmer im Baugewerbe
Anerkennung und Branchenpreise für LIMS-Softwareanalysten
Führende Organisationen vertrauen darauf und werden von Analysten anerkannt
Frostradar – Anführerquadrant
Frost & Sullivan
Anerkannt als Marktführer im Low-Code-LIMS-Bereich mit 10-mal schnellerer Bereitstellung
Über 120 globale Implementierungen
AmpleLogic
Nachgewiesene Erfolgsbilanz bei Unternehmenskunden und Fortune-500-Unternehmen
Gartner-Bewertung 2024–2025
Gartner
Im Gartner Magic Quadrant für LIMS-Bewertung mit Glaubwürdigkeit Dritter enthalten
2024-2025
"Einfach zu bedienende und benutzerfreundliche Oberfläche für die Laborverwaltung. Reduzierte manuelle Arbeit und half uns bei der Umstellung auf völlig papierlose Laborabläufe."
Laborleiter
Pharmazeutische Qualitätskontrolle
"Gute Herstellerunterstützung und Reaktionsfähigkeit während der Implementierung. Die Instrumentenintegrationsfunktionen haben unsere QC-Testabläufe erheblich optimiert."
QC-Analyst
Lebenswissenschaften
"Die Module Stabilitätsmanagement und Probenplanung sind außergewöhnlich. Die Datentransparenz in Echtzeit über alle Laborabläufe hinweg war für unser Team von entscheidender Bedeutung."
Verifizierter G2-Benutzer
Laborleiter
Sind Sie bereit, Ihren QC-Laborbetrieb zu transformieren?
Schließen Sie sich führenden Pharma- und Biotech-Unternehmen an, die mit AmpleLogic LIMS QC-Zyklen beschleunigen und die Produktivität steigern.
Bleiben Sie in den Biowissenschaften an der Spitze
Erhalten Sie die neuesten Produktaktualisierungen, Compliance-News und Brancheneinblicke in Ihren Posteingang.