Controle cada documento: desde la creación hasta la jubilación
El software de gestión de documentos farmacéuticos de AmpleLogic ofrece software de control de documentos de nivel empresarial con cumplimiento de grado farmacéutico, códigos de barras, gestión controlada de SOP, emisión de impresiones, controles de versión y sustitución, y automatización inteligente.
25%
Reducción de los resultados de la auditoría
30%
Es hora de publicar la mejora
50%
Esfuerzo manual guardado
FDA
21 CFR Parte 11 Listo

Desafíos clave de GMP sin software de control de documentos farmacéuticos
Puntos críticos que afectan el cumplimiento, la eficiencia y la trazabilidad en la gestión de documentos farmacéuticos
Los sistemas de documentos farmacéuticos en papel o parcialmente digitales aún persisten
Sin un sistema de gestión de documentos de cumplimiento, el seguimiento manual de documentos consume entre 15 y 20 horas por semana, lo que aumenta los errores y el tiempo de recuperación.
Deficiencias en las funciones del EDMS: control de versiones de SOP débil y emisión de impresiones limitada
Los operadores utilizan SOP obsoletos debido a la falta de software de control de versiones de documentos, lo que genera hallazgos de auditoría e infracciones de cumplimiento.
Sin seguimiento de documentos basado en códigos de barras y gestión de sustitución débil
Los documentos obsoletos permanecen en circulación sin seguimiento controlado de copias ni retiro automatizado.
Difícil integración de DMS con sistemas LMS, eQMS, LIMS y MES
Los sistemas desconectados interrumpen la trazabilidad, lo que aumenta el esfuerzo de preparación de auditorías y el tiempo de respuesta.
Lo que debe ofrecer un EDMS de calidad farmacéutica para cumplir con las GMP
Gestión del ciclo de vida de los documentos, cumplimiento normativo, gestión controlada de SOP y automatización validada.
Gestión del ciclo de vida de los documentos
Software completo de gestión del ciclo de vida de los documentos que abarca la creación, la revisión, la aprobación, la liberación y el archivo con sustitución y obsolescencia controladas.
Validación y controles
Software de flujo de trabajo de aprobación de documentos validado con controles asignados a los requisitos reglamentarios y capacidades del sistema de control de documentos digitales.
Integraciones y Automatización
Integraciones perfectas de sistemas, búsqueda avanzada y automatización impulsada por IA para reducir la conciliación manual.
21 CFR Parte 11 y Anexo 11 de la UE Cumplimiento normativo
Un sistema de gestión de documentos que cumple con 21 CFR Parte 11 y cumple con los requisitos del sistema de gestión de documentos de la FDA, el Anexo 11 de la UE y GxP con controles asignados.
Trazabilidad y Seguridad
Sólido software de control de versiones de documentos, pistas de auditoría, firmas electrónicas y seguimiento de impresión y recuperación de copias controladas.
Tipos de documentos GMP básicos gestionados en software de gestión de documentos farmacéuticos
Software de gestión del ciclo de vida de documentos con pistas de auditoría y metadatos para la preparación GMP
Documentos de Calidad
- Procedimientos operativos estándar (SOP) con control de versiones
- Registros de control de cambios con flujos de trabajo de aprobación
- Registros de capacitación vinculados para la trazabilidad del cumplimiento
- Gestión de copias obsoletas y control de sustitución.
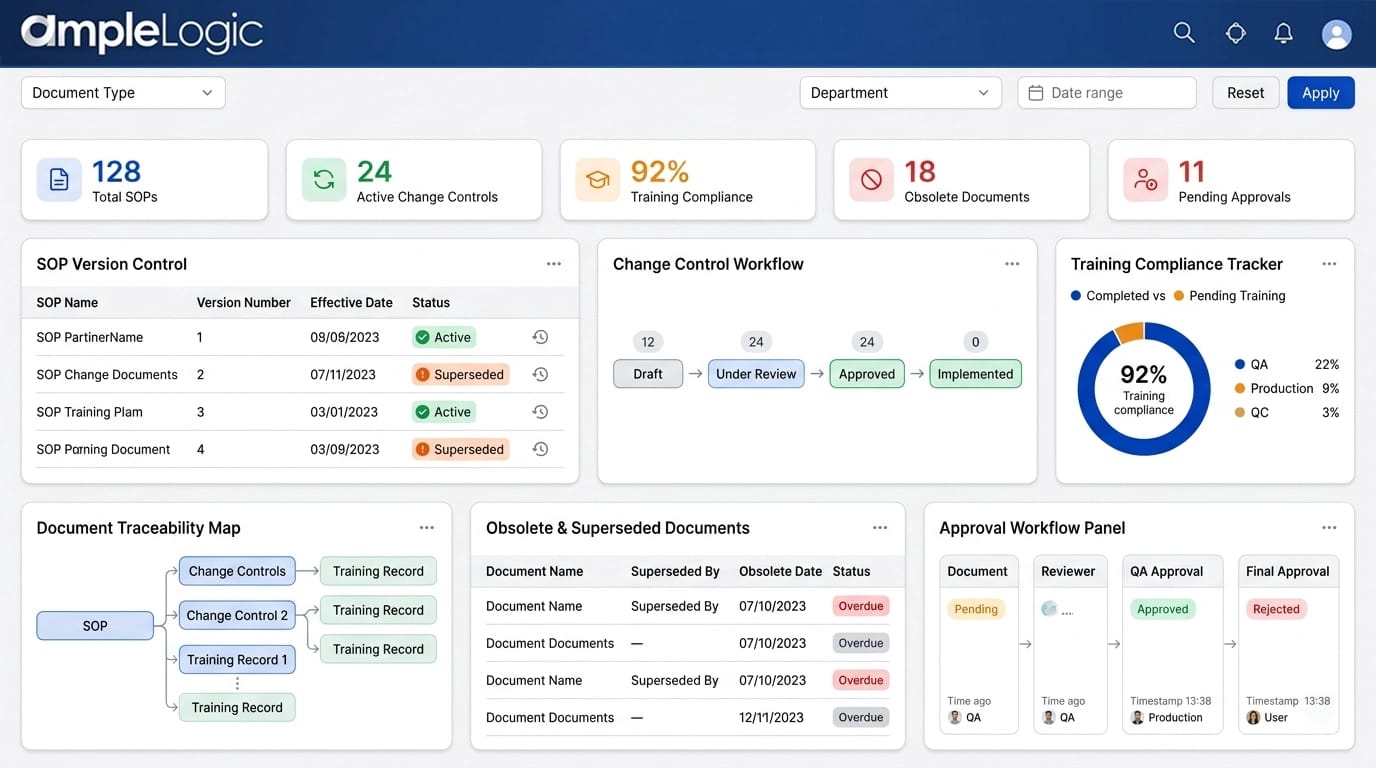
Software de control de versiones SOP: controles de ciclo de vida, copias obsoletas y reemplazantes
Asegúrese de que solo los documentos actuales impulsen procesos regulados con control de documentos digitales
Borrador
Edición controlada de documentos con estado de borrador claro y acceso restringido.
Revisar
Revisión paralela por parte de equipos multifuncionales con seguimiento de auditoría completo de los comentarios de los revisores con sellos de fecha y hora.
Aprobar
Flujo de trabajo de aprobación formal con paso de lectura y reconocimiento obligatorio.
Lanzamiento (versionado)
Numeración de versiones, gestión de impresiones y asignación de códigos de barras para impresiones.
Reemplazar
Reemplazo automatizado de versiones anteriores y notificaciones a los usuarios.
Obsoleta y Archivo
Revocación explícita de documentos obsoletos, acceso controlado a archivos y uso bloqueado en procesos activos.
Borrador
Edición controlada de documentos con estado de borrador claro y acceso restringido.
Revisar
Revisión paralela por parte de equipos multifuncionales con seguimiento de auditoría completo de los comentarios de los revisores con sellos de fecha y hora.
Aprobar
Flujo de trabajo de aprobación formal con paso de lectura y reconocimiento obligatorio.
Lanzamiento (versionado)
Numeración de versiones, gestión de impresiones y asignación de códigos de barras para impresiones.
Reemplazar
Reemplazo automatizado de versiones anteriores y notificaciones a los usuarios.
Obsoleta y Archivo
Revocación explícita de documentos obsoletos, acceso controlado a archivos y uso bloqueado en procesos activos.

Emisión de impresiones, distribución controlada de copias y seguimiento de recuperación
Asegúrese de que solo lleguen a producción los documentos actuales y autorizados, incluidas copias no controladas, de capacitación y borradores.
Aprobar
Finalice el documento con metadatos de versión y aprobación a través del software de flujo de trabajo de aprobación de documentos.
Versión de bloqueo
Congelar la versión aprobada; Evite ediciones y marque estados reemplazados utilizando las salvaguardias del sistema de control de documentos digitales.
Emisión de impresión
Otorgue derechos de impresión por función/sitio, genere marcas de agua como copia controlada, copia no controlada, copia de capacitación y copia borrador. Habilite la impresión y recuperación de copias controladas en todos los sitios.
Distribución
Publique en sitios controlados y listas basadas en roles con etiquetas de códigos de barras y acuse de recibo en el momento de la entrega.
Conciliación y seguimiento de auditoría
Realice un seguimiento de los detalles de impresión y concilie las copias impresas emitidas con auditorías para lograr una trazabilidad completa del sistema de control de documentos farmacéuticos.
Control y verificación de impresión
Cerrar la brecha entre los sistemas digitales y las copias físicas mediante el seguimiento basado en códigos de barras
Generación dinámica de códigos de barras
Marca de agua automática y generación de códigos de barras únicos para cada copia física impresa.
Verificación del punto de uso
Escaneo de códigos de barras en tiempo real en el piso de producción para verificar el estado y la versión de aprobación del documento.
Auditoría de impresión integral
Seguimiento completo de copias físicas distribuidas, incluidos registros de impresión por usuario y datos de ubicación.

Búsqueda inteligente de OCR e IA para su sistema de gestión de documentos de cumplimiento GxP
Haga que los documentos regulados sean buscables, revisables y accesibles a través de su sistema de control de documentos digitales
OCR impulsado por IA
Convierte escaneos e imágenes en texto editable y con capacidad de búsqueda.
Reduzca la transcripción manual y permita un descubrimiento más rápido.
Búsqueda inteligente
Muestra contenido regulado con relevancia contextual.
Mejore la precisión de la recuperación en todos los almacenes de documentos.
Búsqueda activada por voz
Acelera la recuperación y revisión con manos libres.
Acceso más rápido durante auditorías y flujos de trabajo del equipo.
Soporte de auditoría y descubrimiento electrónico
Permite una revisión de documentos, recuperación de evidencia y respuestas de auditoría más rápidas.
Cumplimiento de ayudas, trazabilidad y auditorías reguladas.
Accesibilidad para todo el equipo
Proporciona acceso consistente a documentos controlados en todas las funciones.
Habilite la trazabilidad y la colaboración en entornos regulados.
Integraciones de DMS compatibles con GMP con eQMS, LMS, LIMS y MES
Perfectamente conectado al ecosistema del sistema de gestión de documentos GxP de su empresa para una trazabilidad de documentos de extremo a extremo
LMS
Necesidades de capacitación a partir de la introducción de nuevos SOP y cambios de versión. Comprobación de finalización de la formación.
eQMS
Cambio de versión desde Control de cambios, Resultados de auditoría, CAPA.
LLANTAS
Cambio de versión a partir de hallazgos regulatorios.
LIMAS
Métodos de prueba y STP con resultados y registros de laboratorio.
Libro de registro electrónico
Referencia de plantilla de libro de registro.
Validación de limpieza
Acceso a SOP para procedimientos de limpieza.
eBMR/MES
Gestión y acceso a documentos BMR/BPR.
GORRAS
Manuales de equipos/SOP para procedimientos de calibración.
SAVIA
Integración de la planificación de recursos empresariales.
SUM
Integración del sistema de gestión de usuarios.
Fortalezas de la plataforma AmpleLogic Low-Code DMS y valor habilitado por la IA
Flexibilidad de código bajo, preparación para el cumplimiento y automatización controlada para las ciencias biológicas
Diseñadora de arrastrar y soltar LCNC
El constructor visual reduce el código personalizado y acelera la entrega para una composición rápida de la aplicación.
Gestión de documentos en la nube para farmacia
Software de gestión de documentos en la nube para el sector farmacéutico con plazos acelerados y un rápido impacto empresarial: retorno de la inversión en tan solo 3 meses.
Gestión de documentos industriales regulados
Software de gestión documental industrial regulado diseñado para documentación y auditorías. Preparado para USFDA, MHRA e ISO.
Más de 18 aplicaciones de CUNAS
Aplicaciones prediseñadas para flujos de trabajo comunes de ciencias biológicas, listas para implementarse de inmediato.
Más de 100 clientes de ciencias biológicas
La base de clientes demuestra una fuerte tracción de la industria y una adopción de plataforma validada.
Automatización habilitada por IA
La IA ayuda a la automatización, la extracción y el ensamblaje de aplicaciones para acelerar la composición y el procesamiento.
ROI del software DMS: beneficios comerciales de la gestión de documentos farmacéuticos digitales
Cumplimiento, velocidad, precisión y calidad digital escalable
25%
Reducción de los resultados de la auditoría
Objetivo de reducción porcentual de los hallazgos después de la implementación.
30%
Es hora de publicar la mejora
Reducción proyectada en el tiempo para liberar documentos.
50%
Esfuerzo manual guardado
Reducción estimada de horas de procesamiento manual.
"De fácil acceso y manejo. Trabajo sin papel y puede mantener registros del control de cambios realizados y fácil acceso desde cualquier ubicación. Menos tiempo consumible."
Shweta Ramdas R.
Especialista en Control de Documentos
"El software es fácil de usar e implementar a nivel de operador. La actividad en línea con pistas de auditoría hace que el cumplimiento sea perfecto."
Silpa K.
Seguro de calidad
"Flujos de trabajo configurables, beneficios de cumplimiento y reducción del uso de papel en toda la organización. La atención al cliente es rápida y la implementación fue sencilla."
Ramesh T.
Gerente de TI farmacéutica
Programe una demostración de DMS en vivo con procedimientos operativos estándar de muestra y registros de lotes
Experimente la impresión controlada, la emisión de impresiones y la trazabilidad de un extremo a otro con el sistema de gestión de documentos electrónicos impulsado por IA de AmpleLogic.
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.

