
Industria de las ciencias biológicas Tendencias y perspectivas
Perspectivas de expertos sobre fabricación farmacéutica, cumplimiento, automatización de IA y transformación digital en ciencias de la vida.


Los cinco principales desafíos de cumplimiento que enfrentan los laboratorios y cómo puede ayudar LIMS

Seis estrategias comprobadas para cerrar las brechas de cumplimiento en el sector farmacéutico

Cómo automatizar el cumplimiento de la fabricación: racionalización de los procesos para una mayor eficiencia

De las moléculas a los metadatos: guía para la privacidad y seguridad de los datos en la industria farmacéutica

El papel de AmpleLogic en las tendencias futuras en los sistemas de gestión de calidad (QMS)

¿Cómo se pueden utilizar los datos APQR para la verificación continua de procesos?

Cómo se lleva a cabo la validación de la limpieza en las ciencias biológicas: una guía paso a paso

Por qué optimizar la validación de la limpieza para lograr el cumplimiento y la eficiencia

¿Cómo mejora el CPV el flujo de datos en la fabricación?

¿Qué esperar durante una auditoría ISO 9001?

Investigación de resultados de OOS en pruebas analíticas
Una guía completa para investigar resultados fuera de especificación (OOS) en pruebas analíticas. Aprenda flujos de trabajo estructurados, análisis de causa raíz y enfoques que cumplan con las normativas utilizando el eQMS de AmpleLogic para garantizar la integridad de los datos, el control de calidad y la gestión eficaz de CAPA en industrias reguladas.

Ciclo de vida del sistema QMS para dominar la calidad y el cumplimiento en el sector farmacéutico
Descubra cómo el eQMS de AmpleLogic simplifica el ciclo de vida de un sistema de gestión de calidad en la industria farmacéutica. Desde la implementación hasta la mejora continua, logre un cumplimiento perfecto, mejore la calidad del producto y digitalice los procesos de calidad críticos con una plataforma avanzada y escalable.

Seis herramientas digitales que reducen los errores humanos en las ciencias biológicas
Los errores humanos en las ciencias biológicas pueden generar riesgos de cumplimiento y costosas desviaciones. Explore seis herramientas digitales esenciales que agilizan los flujos de trabajo, automatizan la captura de datos y garantizan la precisión en todas las operaciones farmacéuticas y biotecnológicas.

Cipla transforma el acceso de los usuarios con AmpleLogic UMS en el sector farmacéutico
Explore cómo Cipla simplificó la gestión del acceso de usuarios en sus operaciones farmacéuticas utilizando la solución UAM avanzada de AmpleLogic. Este estudio de caso destaca el cumplimiento mejorado, el aprovisionamiento automatizado de usuarios y el control de acceso seguro y listo para auditorías alineado con los requisitos de GxP.

Requisitos reglamentarios para el cálculo de MACO y la validación de limpieza
Comprender los requisitos reglamentarios para el cálculo de MACO y la validación de limpieza en la fabricación farmacéutica. Esta guía explica cómo agencias globales como la FDA, EMA, CDSCO y la OMS esperan límites de residuos basados en el riesgo y científicamente justificados utilizando PDE y enfoques basados en dosis para garantizar el cumplimiento, la seguridad del paciente y la preparación para las auditorías.

Reducción del error humano en la fabricación farmacéutica mediante una solución digital
El error humano sigue siendo una de las principales causas de problemas de cumplimiento en la fabricación farmacéutica. Al adoptar soluciones digitales como eBMR, QMS y LIMS, las organizaciones pueden eliminar las ineficiencias manuales, mejorar la precisión de los datos y garantizar el cumplimiento normativo mediante la automatización, el monitoreo en tiempo real y los flujos de trabajo estandarizados.

La ventaja digital de Teva con AmpleLogic
Explore cómo Teva aprovechó el eQMS de AmpleLogic para digitalizar los procesos de calidad, mejorar el cumplimiento y reducir las cargas de trabajo manuales. Este estudio de caso destaca cómo una plataforma digital unificada permitió operaciones más rápidas, una mejor preparación para las auditorías y una gestión de calidad escalable en la industria farmacéutica.

¿Su software de aplicación está desactualizado o simplemente es seguro?
El software de aplicaciones obsoleto puede exponer a las organizaciones a importantes riesgos de seguridad, fallos de cumplimiento e ineficiencias operativas. Este artículo explora cómo los sistemas heredados afectan a las industrias reguladas, como la farmacéutica, y por qué es esencial actualizar a soluciones digitales modernas y seguras. Descubra cómo AmpleLogic ayuda a las empresas a cumplir las normas, ser seguras y estar preparadas para el futuro.

Sistema de Gestión del Aprendizaje para la Industria Cosmética
El LMS de AmpleLogic para la industria cosmética agiliza la capacitación, garantiza el cumplimiento normativo y mejora la competencia de la fuerza laboral. Con automatización impulsada por IA, gestión de SOP y funciones listas para GMP, permite a las empresas de cosméticos mantener la calidad, la seguridad y la preparación para las auditorías en un entorno altamente regulado.

Transforme los laboratorios de control de calidad con software avanzado de planificación y programación
El software de planificación y programación de control de calidad de AmpleLogic brinda a los laboratorios farmacéuticos una planificación inteligente, programación automatizada y ejecución basada en campañas. Mejora la utilización de recursos, reduce el tiempo de respuesta y garantiza el cumplimiento a través de visibilidad en tiempo real y flujos de trabajo de laboratorio optimizados.

Obtenga su lista de verificación de libro de registro electrónico: una herramienta práctica para equipos de control de calidad, control de calidad y producción
Una práctica lista de verificación del libro de registro electrónico ayuda a los equipos de control de calidad, control de calidad y producción a estandarizar la documentación, reducir los errores humanos y mantener el cumplimiento de las GMP. Al digitalizar los libros de registro, las empresas farmacéuticas pueden mejorar la integridad de los datos, garantizar la preparación para las auditorías y optimizar los flujos de trabajo operativos diarios.

Transformación Digital de la Gestión de Calidad en OCuSOFT con EQMS
Descubra cómo OCuSOFT aprovechó el eQMS de AmpleLogic para digitalizar los procesos de calidad de un extremo a otro, reduciendo los registros en papel en un 85 % y mejorando al mismo tiempo la visibilidad, el cumplimiento y la preparación para las auditorías. La solución simplificó el control de documentos, CAPA y los flujos de trabajo de auditoría en un entorno regulado.

Cómo responder eficazmente a las normas 483 de la FDA y evitar errores comunes
Responder a las observaciones de la FDA 483 requiere un enfoque oportuno, estructurado y basado en evidencia. Las organizaciones deben abordar cada observación con un análisis de causa raíz, acciones correctivas y preventivas (CAPA) y cronogramas claros para evitar cartas de advertencia y fortalecer el cumplimiento.

¿Qué sucede cuando el control de calidad no participa en los cambios de las instalaciones?
Excluir el control de calidad de los cambios en las instalaciones puede generar brechas de cumplimiento, fallas de validación y un mayor riesgo regulatorio. El control de calidad desempeña un papel fundamental a la hora de evaluar el impacto, garantizar la documentación adecuada y mantener los estándares GMP a través de procesos estructurados de control de cambios y gestión de riesgos.

Registros de lotes incompletos: un riesgo oculto en cada auditoría de la FDA
Los registros de lotes incompletos son una importante señal de alerta durante las auditorías de la FDA, y a menudo dan lugar a 483 observaciones y cartas de advertencia. Las firmas faltantes, las entradas poco claras y las lagunas de datos generan preocupaciones sobre la calidad del producto, la trazabilidad y la integridad de los datos, lo que hace que las prácticas de documentación sólidas sean esenciales para el cumplimiento.

El 80% del libro de registro manual actual del año 2000 se maneja con sólo 60 a 65 registros

Validación de próxima generación: adopción de la validación de procesos continuos para una fabricación farmacéutica ágil y adaptable

Maximice la eficiencia y el conocimiento con el panel gráfico APQR

Simplificación de la validación de la limpieza en la fabricación farmacéutica con sistemas MES

Guía definitiva sobre el libro de registro electrónico para la fabricación farmacéutica

Control estadístico de procesos y APQR: mejorar la garantía de calidad farmacéutica

Mejores prácticas para implementar la planificación y programación del control de calidad en el sector farmacéutico

Una guía para la validación de sistemas informáticos (CSV) en productos farmacéuticos

Cómo los sistemas de planificación y programación de control de calidad mejoran la eficiencia del laboratorio

El papel de la verificación continua de procesos en la validación de procesos

Cómo la validación de procesos garantiza una calidad constante del producto en el sector farmacéutico

Una guía paso a paso para la validación de procesos en el sector farmacéutico

Cómo automatizar los procesos de validación de limpieza en el sector farmacéutico

13 formas de potenciar su laboratorio con el software LIMS

Liberando la eficiencia del laboratorio a través de sistemas LIMS validados

Fallos de integridad de datos de la MHRA y cómo prevenirlos
Conozca las fallas comunes de integridad de datos de la MHRA en el sector farmacéutico y cómo prevenirlas. Mejore el cumplimiento, garantice los principios de ALCOA+ y manténgase preparado para las auditorías con las mejores prácticas.

¿En qué se diferencia el LIMS estéril del LIMS OSD?
Descubra en qué se diferencia el LIMS estéril del LIMS OSD en el sector farmacéutico. Compare flujos de trabajo, necesidades de cumplimiento y gestión de datos para elegir la solución adecuada.

Error humano e integridad de datos en el sector farmacéutico | Guía de cumplimiento de la FDA
Comprenda cómo el error humano afecta la integridad de los datos en el sector farmacéutico. Conozca los requisitos de cumplimiento de la FDA, los principios ALCOA+ y las estrategias comprobadas para prevenir fallas en las auditorías.

Investigación de resultados de OOS en pruebas analíticas
Aprenda a investigar resultados OOS (fuera de especificación) en pruebas analíticas. Comprender el análisis de la causa raíz, las pautas de la FDA y las estrategias CAPA para el cumplimiento farmacéutico.

Industria 4.0: Fabricación digital en la industria farmacéutica

Enfoques basados en riesgos para la revisión anual de la calidad del producto (APQR) Desarrollo de SOP: garantizar el enfoque en los atributos críticos de calidad

Decoding Pharma MES: exploración de sistemas de ejecución de fabricación para la fabricación farmacéutica

Aprovechamiento del software de seguimiento de la calidad del producto para mejorar el APQR en la fabricación farmacéutica

Mejora de la revisión de la calidad del producto mediante el manejo automatizado de excursiones en la fabricación farmacéutica

Monitoreo en tiempo real: implementación de límites de control dinámico para la mejora continua de procesos en el sector farmacéutico

Abordar las discrepancias en los registros de lotes con los sistemas MES: garantizar la precisión y el cumplimiento

Problemas de estabilidad de la producción farmacéutica: aprovechar MES para el monitoreo y la corrección en tiempo real

Comprensión de los requisitos del libro de registro GMP

Navegando por la integración de IA y ML en el software Pharma MES

Comprensión de la importancia del libro de registro secuencial de equipos en ciencias biológicas

Comprender la revisión anual de la calidad del producto y desbloquear la excelencia en los procesos comerciales con el software AmpleLogic APQR

Innovaciones de vanguardia en mejora continua de la calidad para la industria de las ciencias biológicas

En la industria de las ciencias biológicas, la precisión es necesaria para mantener los más altos estándares de calidad y el cumplimiento normativo. La mejora continua de la calidad (CQI) es la piedra angular de la excelencia en la fabricación de ciencias biológicas y encarna una filosofía de refinamiento y optimización incesantes en todas las facetas de la producción. Este artículo profundiza en la vanguardia de la innovación que impulsa la CQI en el sector de las ciencias biológicas, mostrando tecnologías y metodologías innovadoras preparadas para revolucionar la gestión de la calidad, la eficiencia operativa y el cumplimiento normativo. Evolución de la mejora continua de la calidad en las ciencias biológicas La evolución de la CQI en la industria de las ciencias biológicas ha estado marcada por un viaje desde los enfoques tradicionales de gestión de la calidad hacia metodologías de vanguardia basadas en datos. Inicialmente arraigado en los principios de Gestión de Calidad Total (TQM), CQI ha experimentado un cambio de paradigma hacia un modelo más proactivo e impulsado por la tecnología. Hoy en día, los avances en análisis, monitoreo en tiempo real y tecnología de gemelos digitales han marcado el comienzo de una nueva era de mejora continua de la calidad, permitiendo a las empresas de ciencias biológicas anticipar, prevenir y abordar problemas de calidad con una precisión y agilidad sin precedentes. Innovaciones que impulsan la CQI en la industria de las ciencias biológicas Algunas de las innovaciones de vanguardia en la industria de las ciencias biológicas para mejorar la CQI son: Análisis avanzado y modelado predictivo La convergencia de análisis avanzados y modelos predictivos ha revolucionado la forma en que las empresas de ciencias biológicas analizan y aprovechan los datos. Al aprovechar el poder de los algoritmos de aprendizaje automático y el análisis de big data, las empresas pueden extraer información procesable de vastos conjuntos de datos, lo que les permite predecir tendencias de calidad, optimizar procesos y tomar decisiones basadas en datos que mejoran la seguridad del paciente y la eficacia del producto. Sistemas de control y monitoreo en tiempo real Los sistemas de control y monitoreo en tiempo real representan un cambio de paradigma en la gestión de calidad, ofreciendo a los fabricantes de ciencias biológicas una visibilidad y un control incomparables sobre sus procesos de producción. Al aprovechar sensores, dispositivos IoT y plataformas basadas en la nube, las empresas pueden monitorear continuamente parámetros de calidad críticos en tiempo real, detectar desviaciones instantáneamente e implementar acciones correctivas de manera proactiva para garantizar la calidad y el cumplimiento del producto. Innovaciones que impulsan la CQI en la industria de las ciencias biológicas Tecnología de gemelos digitales La tecnología de gemelos digitales ha surgido como un punto de inflexión en la industria de las ciencias biológicas, permitiendo a las empresas crear réplicas virtuales de sus procesos y sistemas de fabricación. Al simular y optimizar operaciones en un entorno virtual, las empresas pueden identificar ineficiencias, probar hipótesis y optimizar los parámetros del proceso sin interrumpir la producción. Los gemelos digitales ofrecen un entorno de pruebas libre de riesgos para la innovación, lo que permite a las empresas experimentar, iterar y perfeccionar sus procesos con una velocidad y precisión sin precedentes. Blockchain y transparencia de la cadena de suministro La tecnología Blockchain encierra una inmensa promesa para mejorar la transparencia y la trazabilidad en la cadena de suministro de las ciencias biológicas. Al aprovechar el libro de contabilidad inmutable y la seguridad criptográfica de blockchain, las empresas pueden crear un registro transparente y auditable de cada transacción e intercambio de datos a lo largo de la cadena de suministro. Desde el abastecimiento de materias primas hasta la distribución y más, blockchain garantiza visibilidad, integridad y cumplimiento de extremo a extremo, salvaguardando la autenticidad del producto y la seguridad del paciente. Impacto de las innovaciones en la industria de las ciencias biológicas La adopción de estas innovaciones ha catalizado un cambio de paradigma en la industria de las ciencias biológicas, impulsando la excelencia en múltiples dimensiones: Calidad mejorada del producto y seguridad del paciente: al aprovechar análisis avanzados, monitoreo en tiempo real y gemelos digitales, las empresas de ciencias biológicas pueden garantizar la calidad y seguridad constantes de sus productos, salvaguardando la salud y la confianza de los pacientes. Mejora de la eficiencia operativa y ahorro de costos: las innovaciones en la mejora continua de la calidad permiten a las empresas optimizar los procesos de producción, optimizar la utilización de recursos y reducir el desperdicio, lo que conduce a una mayor eficiencia y ahorro de costos. Cumplimiento normativo y preparación para las auditorías: al implementar medidas sólidas de control de calidad y sistemas de trazabilidad, las empresas pueden demostrar el cumplimiento de los requisitos reglamentarios y mantener la preparación para las auditorías en todo momento. Innovación acelerada y tiempo de comercialización: adoptando tecnologías digitales y pre Gracias al modelado dictivo, las empresas de ciencias biológicas pueden acelerar los ciclos de innovación, reducir el tiempo de comercialización y ofrecer tratamientos que salvan vidas a los pacientes de forma más rápida y eficiente. Conclusión La frontera de la mejora continua de la calidad en la industria de las ciencias biológicas se caracteriza por una innovación sin precedentes, impulsada por tecnologías de vanguardia y un compromiso incesante con la excelencia. A medida que las empresas adoptan análisis avanzados, monitoreo en tiempo real y gemelos digitales, están preparadas para elevar la calidad del producto, mejorar la eficiencia operativa y garantizar el cumplimiento normativo en cada etapa del ciclo de vida del producto. La búsqueda de la excelencia a través de la mejora continua de la calidad no es simplemente un imperativo estratégico sino una obligación moral para las empresas de ciencias biológicas dedicadas a promover la salud y el bienestar humanos.

Avance de la garantía de calidad farmacéutica: sinergia de pruebas de liberación en tiempo real, verificación continua de procesos y APQR

Aprovechamiento del software estadístico para el control de calidad y el análisis APQR en ciencias biológicas

Garantía de la calidad mediante software de validación de limpieza en la fabricación farmacéutica

Parámetros críticos del proceso en la fabricación farmacéutica

IA y sin código: el futuro de la fabricación farmacéutica
Explore cómo la IA y las plataformas sin código están transformando la fabricación farmacéutica con un control de calidad más inteligente, mantenimiento predictivo y documentación lista para inspección.

The Real Cost of Delaying Low-Code & AI Adoption in Pharma
Discover the hidden operational debt pharma companies face by delaying low-code and AI adoption—and how AmpleLogic helps reduce it with GxP-compliant workflows.

¿Por qué todo equipo regulador necesita una solución RIMS?
Descubra por qué los equipos de reglamentación farmacéutica necesitan una solución RIMS para gestionar presentaciones, renovaciones, actualizaciones de CMC y presentaciones globales con precisión con AmpleLogic RIMS.

¿Por qué toda planta farmacéutica necesita un libro de registro electrónico?
Descubra por qué las plantas farmacéuticas necesitan libros de registro electrónicos para garantizar el cumplimiento, eliminar errores manuales y mejorar la integridad de los datos con soluciones impulsadas por IA.

Cómo la IA reduce el tiempo de gestión de desviaciones en Pharma QMS
AmpleLogic AI reduce el tiempo de manejo de las desviaciones farmacéuticas, automatiza el análisis de la causa raíz, mejora el cumplimiento y acelera las investigaciones.

Guía completa para la validación de la limpieza en la fabricación farmacéutica
La guía AmpleLogic para la validación de la limpieza en el sector farmacéutico garantiza el cumplimiento de las GMP, previene la contaminación y mejora la eficiencia de fabricación.

Actavis lanzó la solución AmpleLogic eLogbook

Eisai Pharmaceuticals puso en marcha con éxito el software de gestión de formación de empleados AmpleLogic
Eisai Pharmaceuticals puso en marcha con éxito el software de gestión de formación de empleados AmpleLogic

Hetero Labs Limited lanza el software de calibración y mantenimiento preventivo AmpleLogic
Hetero Labs Limited lanza el software de calibración y mantenimiento preventivo AmpleLogic

El laboratorio farmacéutico de EE. UU. elige el software de estabilidad AmpleLogic

Tirupati Lifesciences nos eligió para implementar la solución DMS

Indoco Remedies Ltd elige las soluciones de software de calidad de AmpleLogic

FDC Limited elige AmpleLogic para implementar soluciones de calidad

Micro Labs entra en funcionamiento con el sistema AmpleLogic DMS

Los 9 principales desafíos y soluciones para el software eDMS en la industria farmacéutica

¿Por qué sigue siendo intimidante adoptar el sistema de gestión de documentos?

Beneficios del sistema de gestión de formación

Categorías GAMP 5, modelo V y 21 CFR Parte 11, Anexo 11 de la UE

Integración de Inteligencia Artificial y Aprendizaje Automático en QMS

Análisis de causa raíz con ejemplo de la técnica “5” Por qué

APQR 2.0: el salto cuántico de AmpleLogic en garantía de calidad y excelencia centrada en el futuro

¿Están sus libros de registro listos para la próxima auditoría?
Como fabricante de productos farmacéuticos, probablemente esté familiarizado con los estrictos requisitos reglamentarios que rigen la industria. Un aspecto crítico del cumplimiento es mantener registros y documentación precisos y actualizados. Pero, ¿ha considerado el papel de los libros de registro en su sistema de mantenimiento de registros? Si no, quizás quieras empezar.

Los sistemas de gestión de documentos son una bendición para los sectores farmacéuticos tópicos
La incorporación de tecnologías digitales en la industria de las ciencias biológicas se ha convertido en los últimos tiempos en una necesidad empresarial. Con actualizaciones regulatorias diarias, documentación cada vez mayor y la necesidad de auditorías más rápidas, las empresas farmacéuticas se están alejando constantemente de los procesos manuales. Uno de esos cambios es hacia los sistemas de gestión de documentos (DMS), una herramienta que se está volviendo vital para garantizar el cumplimiento, la eficiencia y la integridad de los datos. Si bien las innovaciones digitales han llegado a todos los sectores, su papel en las operaciones farmacéuticas y el control de calidad es especialmente transformador. Entre las muchas herramientas que están transformando la industria, DMS se destaca como una solución importante, que automatiza los flujos de trabajo de documentos, reduce la dependencia del papel y ofrece control centralizado sobre documentación crucial.

Implementación de la validación de tiempo y contenido con software de gestión del aprendizaje
El creciente favor del aprendizaje electrónico a través del software de sistemas electrónicos de gestión del aprendizaje ha ganado un impulso significativo en diversas industrias, especialmente en el sector farmacéutico. Como uno de los sectores más vitales en Europa y otras economías, la industria farmacéutica ha experimentado un rápido crecimiento en los últimos años. Después de la pandemia, la atención sanitaria y la vacunación se convirtieron en máximas prioridades para muchos países. Sin embargo, la urgencia se extendió también a otros medicamentos esenciales en el mercado. En este entorno acelerado, el LMS farmacéutico se ha convertido en una característica fundamental para capacitar a nuevo personal y ofrecer certificaciones para garantizar que los trabajadores estén preparados para manejar las crecientes demandas del sector. A medida que la industria farmacéutica continúa expandiéndose, la necesidad de mano de obra calificada aumenta constantemente. Según el informe más reciente de MarketsandMarkets:

Adopción de Pharma 4.0 en India: un catalizador para la modernización del sector farmacéutico
El término Pharma 4.0 ya no es un concepto que se discute en conferencias; se está poniendo a trabajar sobre el terreno en la India. En los laboratorios de formulación y las unidades de fabricación, las empresas farmacéuticas están actualizando constantemente los sistemas obsoletos, incorporando automatización, visibilidad de datos e infraestructura más inteligente. Este cambio resuelve los problemas de la industria local: retrasos en la producción, fallas en la integridad de los datos, dependencias manuales y un creciente escrutinio regulatorio. A medida que el sector farmacéutico indio adopta la digitalización y las tecnologías avanzadas, se están llevando a cabo varias transformaciones necesarias:

¿Es el sistema de gestión del aprendizaje una demanda de digitalización de la nueva era hoy?

AmpleLogic: Ofrecer beneficios y máxima calidad a un costo mínimo

Por qué las empresas farmacéuticas en crecimiento deberían automatizar su proceso de calidad

CSA (Computer Software Assurance) Un paso desde el CSV tradicional

Pharma 4.0: Faster Digitalization with Low Code Platforms

Las 3 principales tendencias que transformarán las perspectivas de la industria farmacéutica en 2025

7 problemas comunes de cumplimiento que enfrenta la industria farmacéutica

Cumplimiento del Anexo M de la Ley de Medicamentos y Cosméticos (2018)

Presentación de los 8 beneficios del software de gestión de calidad en el sector farmacéutico

Las 7 consultas principales abordadas: integridad de los datos y cumplimiento de CGMP

La armonización de libros de registro voluminosos facilita el mantenimiento de registros en la industria farmacéutica

11 KPI importantes para el sistema de gestión de calidad

Lograr la integridad de los datos es más fácil con eDMS en la industria farmacéutica

Optimización de la fabricación farmacéutica con el software DMS

Elementos esenciales para mejorar la calidad de la atención sanitaria: cinco componentes clave

8 violaciones comunes de las BPC en ensayos clínicos

Una visión integral de los distintos tipos de auditoría en la gestión de la calidad

Implementación de la solución AmpleLogic eQMS 'Go-Live' en Medopharm

Teva se pone en marcha con el software de gestión de programas de calibración AmpleLogic

Notable apogeo de la digitalización en las empresas farmacéuticas con DMS

AmpleLogic: Ofreciendo un sistema de gestión de calidad GMP para lograr un retorno de la inversión óptimo

Industria 4.0: Fabricación digital en la industria farmacéutica
La industria farmacéutica está en la cúspide de una revolución digital. Las tecnologías de la Industria 4.0 están transformando la forma en que se fabrican, prueban y distribuyen los medicamentos a nivel mundial.

13 formas de potenciar su laboratorio con el software LIMS
Un sistema de gestión de información de laboratorio (LIMS) es una herramienta vital para los laboratorios farmacéuticos modernos, ya que optimiza los flujos de trabajo, mejora el cumplimiento e impulsa la eficiencia.

Garantizar el cumplimiento normativo en la validación de la limpieza farmacéutica
El cumplimiento normativo en la validación de limpieza farmacéutica no es negociable. Comprender e implementar los protocolos correctos garantiza la seguridad del producto y la integridad de fabricación.

Mejores prácticas para implementar la validación de limpieza en el sector farmacéutico
Implementar las mejores prácticas de validación de limpieza en la fabricación farmacéutica es esencial para mantener la calidad del producto, prevenir la contaminación cruzada y garantizar el cumplimiento de las GMP.

Diez funciones imprescindibles para su software LIMS ideal
Seleccionar el software LIMS adecuado es una decisión crítica para los laboratorios farmacéuticos. El sistema adecuado puede transformar las operaciones del laboratorio, mejorar el cumplimiento y acelerar el tiempo de obtención de resultados.

Navegando por la integración de IA y ML en el software Pharma MES
La integración de la inteligencia artificial y el aprendizaje automático en los sistemas de ejecución de fabricación está transformando la producción farmacéutica con análisis predictivos y optimización en tiempo real.

Planificación a largo plazo en el ecosistema farmacéutico
La planificación a largo plazo es un imperativo estratégico para las empresas farmacéuticas que navegan por panoramas regulatorios complejos, dinámicas de mercado en evolución y transformación tecnológica.

Liberando el poder de aPaaS con COTS y plataformas Low-Code
La convergencia de aPaaS (plataforma de aplicaciones como servicio) con soluciones COTS (comerciales listas para usar) y el desarrollo de código bajo está remodelando la forma en que las empresas farmacéuticas crean e implementan aplicaciones.

Dominar la calidad farmacéutica con la integración de la capacidad de proceso y APQR
En la industria farmacéutica y biotecnológica la competencia es extremadamente alta, por lo que los estándares de calidad se ven perjudicados. Esto requiere una supervisión e investigación constante de los procesos involucrados.

Monitoreo ambiental continuo mediante BMR en la fabricación farmacéutica
El monitoreo continuo de las condiciones ambientales es primordial en la industria farmacéutica y varios otros sectores, asegurando el cumplimiento de los estándares regulatorios y la calidad del producto.

Mejora del cumplimiento normativo con BMR sin papel en el sector farmacéutico
La industria farmacéutica avanza cada vez más hacia registros de fabricación por lotes (BMR, por sus siglas en inglés) sin papel, impulsada por las expectativas regulatorias y la necesidad de mejorar la integridad y el cumplimiento de los datos.

Pautas de validación de limpieza en la industria farmacéutica
La validación de la limpieza en la industria farmacéutica es un proceso esencial descrito por los organismos reguladores para mantener la calidad del producto y prevenir la contaminación cruzada.

El enfoque moderno en software de revisión de productos: revolucionando la gestión de calidad y cumplimiento
En las industrias actuales, aceleradas y altamente reguladas, el software de revisión de productos se ha convertido en una herramienta indispensable. Evolucionando desde sistemas de seguimiento básicos a plataformas sofisticadas e integradas.

Explorando las herramientas de investigación de desviaciones
En la búsqueda de la excelencia operativa y el aseguramiento de la calidad, las desviaciones de las normas establecidas no sólo se esperan sino que se anticipan. Lo que realmente diferencia a las organizaciones exitosas es cómo manejan estas desviaciones.
%20Software.webp&w=3840&q=75)
Mejora del rendimiento empresarial y la calidad del producto mediante el software de revisión anual de productos (APR)
En el competitivo panorama empresarial actual, mantener una alta calidad del producto y mejorar continuamente la oferta es esencial para el éxito. El software APR se ha convertido en una herramienta poderosa.
Seguimiento de registros de lotes con el software Pharma MES
En el mundo dinámico y altamente regulado de la fabricación farmacéutica, la integración de tecnología avanzada es esencial para sobresalir en procesos comerciales clave y garantizar una calidad estándar del producto.
Explorando las 3 W de APQR: qué, por qué y dónde
Al embarcarse en una exploración de los aspectos esenciales que rodean la Revisión Anual de la Calidad del Producto (APQR), esta investigación profundiza en las preguntas fundamentales de qué, por qué y dónde.

De manual a automatizado: mejora de la validación de BMR en el sector farmacéutico
En la industria farmacéutica, la validación de los registros de fabricación por lotes (BMR) es fundamental para garantizar la calidad, la seguridad y el cumplimiento normativo del producto. Tradicionalmente, esta validación ha sido un proceso manual.

Simplificación de las operaciones farmacéuticas: el impacto del software de gestión de activos empresariales
En el panorama farmacéutico en rápida evolución, la gestión eficiente de los activos es primordial. Desde laboratorios de investigación hasta instalaciones de fabricación y redes de distribución.

Implementación de ALCOA+ en sus procesos de fabricación
En la industria farmacéutica, la integridad de los datos es primordial. Los principios ALCOA (atribuible, legible, contemporáneo, original y preciso) se establecieron para garantizar la integridad de los datos en la fabricación.

AmpleLogic establece un nuevo estándar con IA en el sistema de gestión de aprendizaje farmacéutico
Los sistemas de gestión de aprendizaje (LMS) son cada vez más vitales en la industria farmacéutica, ya que proporcionan una forma estructurada y eficiente de gestionar la formación, el cumplimiento y el desarrollo profesional.
-in-Equipment.webp&w=3840&q=75)
Integración de registros electrónicos de lotes (EBR) en operaciones de equipos
La eficiencia y la precisión son aspectos esenciales en las industrias de ciencias de la vida y farmacéutica. Ayudan a las empresas a alcanzar la excelencia en los procesos comerciales a partir de los procesos manuales tradicionales.

Inteligencia artificial: revolucionando las revisiones anuales de calidad de productos farmacéuticos
La Revisión Anual de la Calidad del Producto (APQR) es un proceso crítico para que las empresas farmacéuticas evalúen los estándares de calidad de sus productos, garanticen el cumplimiento normativo e impulsen la mejora continua.

Desafíos del control de cambios en una industria regulada
El control de cambios es un proceso crítico en industrias reguladas, como la farmacéutica, los dispositivos médicos y la de alimentos y bebidas. Implica gestionar cambios en productos, procesos y sistemas.

Optimización del software de mantenimiento de equipos en la producción y fabricación farmacéutica
El mantenimiento de equipos es un aspecto crucial para garantizar la eficiencia y productividad de los departamentos de producción y fabricación farmacéutica. El software de mantenimiento de equipos ha revolucionado el campo.
El impacto del sistema de seguimiento de activos en la fabricación de productos farmacéuticos
En el intrincado mundo de la fabricación farmacéutica, donde la precisión, el cumplimiento y la eficiencia son activos clave, las empresas buscan soluciones innovadoras para sortear las complejidades.

Navegando el camino hacia la excelencia operativa: el papel del análisis APQR
En el panorama intrincado y en constante evolución de la industria moderna, donde la búsqueda de la excelencia operativa es a la vez un imperativo estratégico y una piedra angular del éxito sostenido.
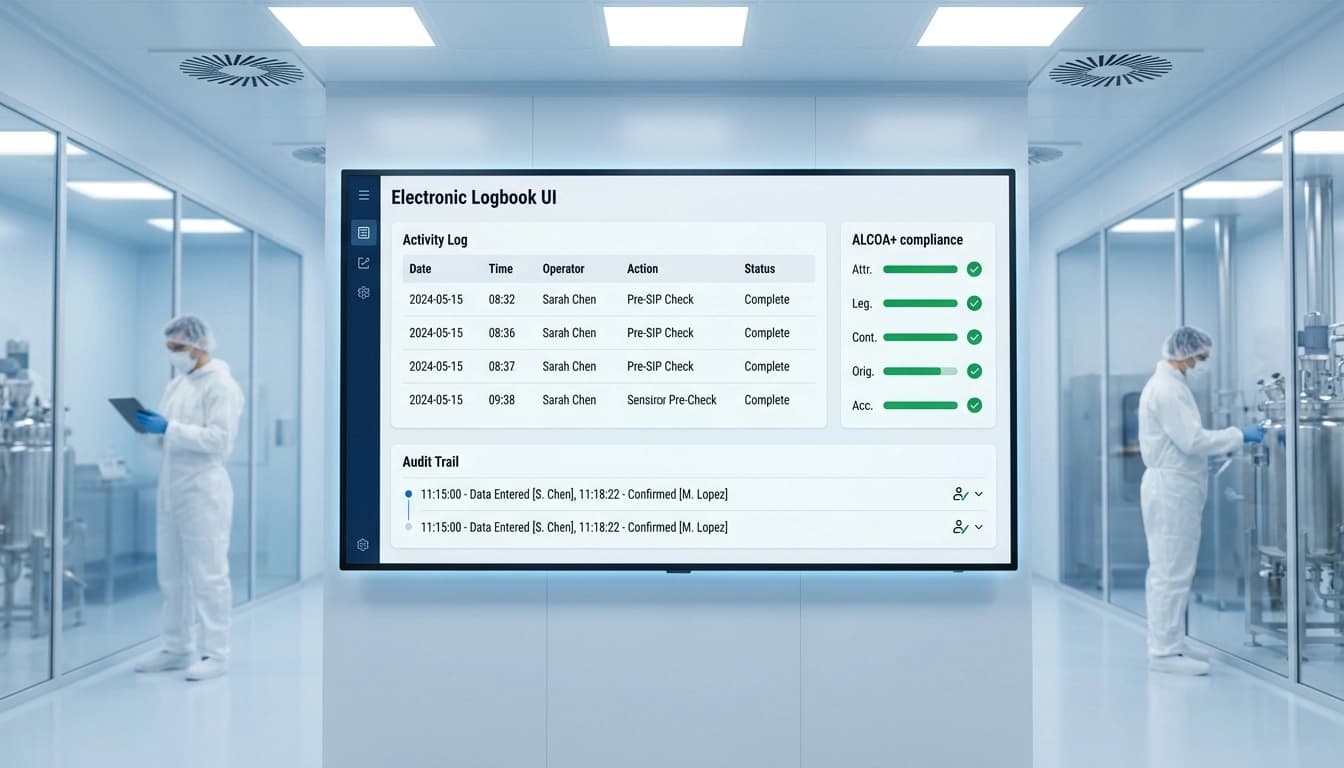
Garantizar la integridad de los datos con un libro de registro electrónico en la fabricación farmacéutica
En la industria farmacéutica, mantener la integridad de los datos es crucial para garantizar la calidad del producto, la seguridad del paciente y el cumplimiento normativo. La integridad de los datos se refiere a la precisión y coherencia de los datos.
-Software-in-Deviation-Handling.webp&w=3840&q=75)
Papel del software de registros electrónicos de lotes (EBR) en el manejo de desviaciones en la fabricación farmacéutica
La eficiencia, la precisión y el cumplimiento son componentes esenciales en la industria de fabricación farmacéutica. Cualquier desviación de los procedimientos operativos estándar puede comprometer la calidad del producto.

Análisis de causa raíz con ejemplo de la técnica "5" Por qué
El Análisis de Causa Raíz (RCA) es un método utilizado para abordar un problema o no conformidad en el proceso de calidad para llegar a la "causa raíz" de la no conformidad. RCA ayuda a corregir o eliminar la causa y evitar que el problema vuelva a ocurrir mediante acciones preventivas.

Beneficios de un sistema de gestión de formación para el cumplimiento de las GMP farmacéuticas
Un sistema de gestión de formación (TMS) farmacéutico agiliza la formación sobre el cumplimiento de las GMP, el seguimiento de competencias y la preparación para las auditorías reglamentarias. Descubra cómo un LMS moderno reduce los costos de capacitación hasta en un 50 %, acelera la calificación de los empleados y garantiza el cumplimiento de 21 CFR Parte 11 en todas las operaciones globales.

¿Por qué sigue siendo intimidante adoptar el sistema de gestión de documentos?
El Sistema de Gestión de Documentos Electrónicos (eDMS) ha cambiado fundamentalmente la forma en que las empresas farmacéuticas y de ciencias biológicas manejan la documentación. Sin embargo, a pesar de la validación de la FDA 21 CFR Parte 11 y los claros beneficios de cumplimiento, muchas organizaciones aún dudan en adoptar plenamente esta transformación digital.

Modificación del modelo V para acelerar las automatizaciones GMP y abordar los problemas de integridad de los datos
Una larga lista de advertencias sobre la integridad de los datos recibidas por las empresas farmacéuticas les ha hecho centrarse en construir y fortalecer sus mecanismos de seguimiento. Una de las soluciones es la digitalización, pero el desafío actual es que la transformación digital va más lentamente de lo esperado.
Suscríbete a nuestro boletín
Manténgase actualizado con las últimas tendencias en fabricación, cumplimiento y transformación digital de productos farmacéuticos.
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.
