Reemplace los libros de registro en papel con registros digitales compatibles con ALCOA+
AmpleLogic es un sistema de registro electrónico compatible con GMP diseñado específicamente para las necesidades de software de registro de producción farmacéutica. Cierre la brecha del contexto operativo entre los equipos heredados y los MES modernos mediante libros de registro sin papel impulsados por IA en la fabricación farmacéutica: digitalice las observaciones sin afectar la lógica del sistema validado.
100%
Profundidad del seguimiento de auditoría
#1
Alineación regulatoria
100%
Adopción de firma electrónica
10x
Implementación más rápida con IA
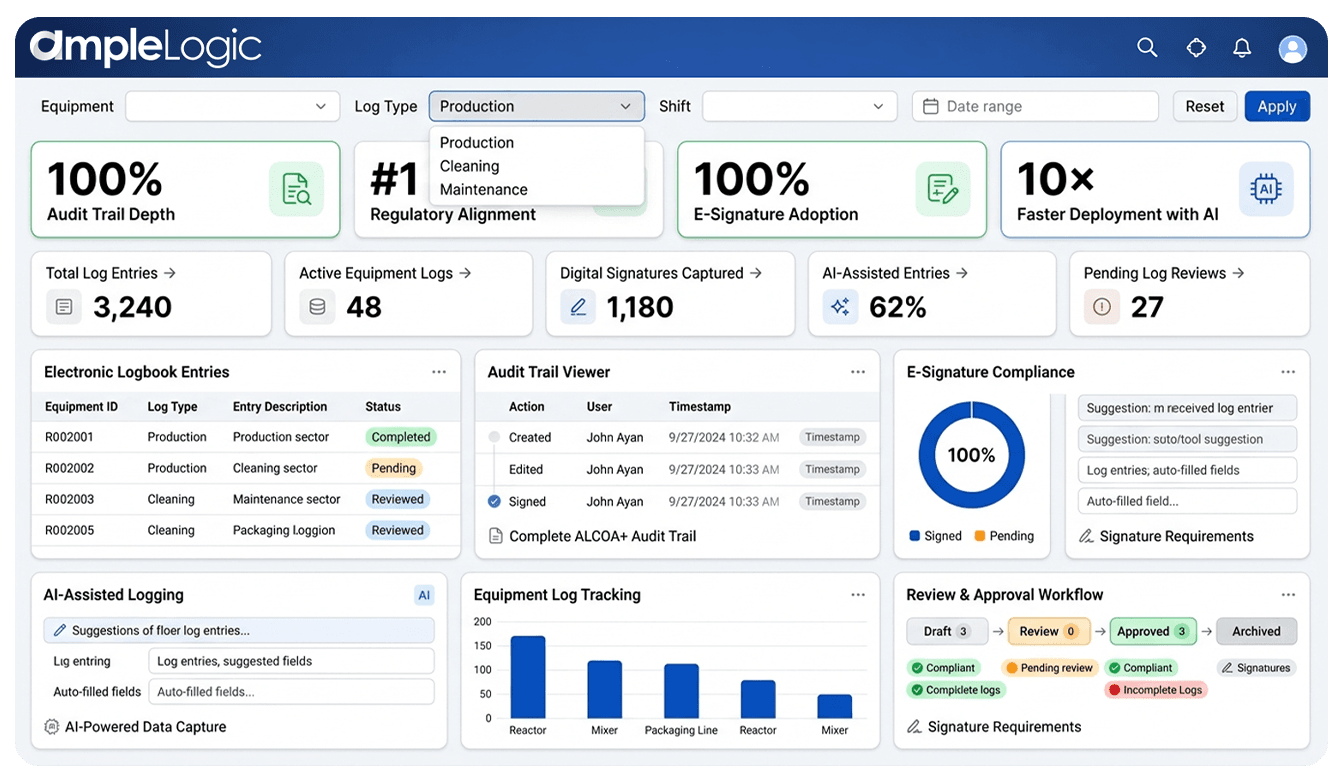
Libro de registro electrónico para productos farmacéuticos que cumple con 21 CFR Parte 11 y Anexo 11 de la UE
La arquitectura eLogbook está diseñada para satisfacer las expectativas regulatorias más rigurosas para registros electrónicos e integridad de datos.
Profundidad del seguimiento de auditoría
Captura completa de cada entrada, modificación y eliminación con marcas de tiempo. Registros atribuibles y contemporáneos de ALCOA+ desde el primer día.
Alineación regulatoria
Totalmente compatible con los marcos FDA 21 CFR Parte 11 y Anexo 11 de la UE. Creado para satisfacer las expectativas GxP más rigurosas a nivel mundial.
Adopción de firma electrónica
Autenticación biométrica o MFA obligatoria para todas las aprobaciones GxP críticas. No repudio y vinculación de firmas según los requisitos de la Parte 11.
Integridad de datos por diseño
Todo registro es atribuible, legible, contemporáneo, original y exacto. La integridad, la coherencia, la resistencia y la disponibilidad se aplican automáticamente.
eLogbook: Operaciones de equipos flexibles y grabación fuera de línea para operaciones de ciencias biológicas
eLogbook sirve como puente contextual sobre la ejecución automatizada de MES y los datos de instrumentación sin procesar.
Capa de ejecución MES
Datos transaccionales estructurados y aplicación de registros por lotes para líneas automatizadas de alta velocidad. Maneja transacciones binarias de aprobación/falla y flujos de trabajo de fabricación estructurados.
Capa de contexto del libro de registro electrónico
libro de registro electrónicoCaptura datos de observación, juicios situacionales y contexto operativo basado en excepciones. La capa de documentación flexible que se encuentra por encima de las actividades manuales y automatizadas del taller.
Capa de instrumentación
Datos sin procesar de PLC, SCADA y equipos heredados independientes en toda la instalación. Lecturas de equipos en tiempo real, datos de sensores y alarmas automáticas se incorporan al libro de registro electrónico.
Por qué MES por sí solo no es suficiente para el cumplimiento de la documentación farmacéutica GMP
Los sistemas transaccionales priorizan la velocidad de ejecución, perdiendo a menudo el contexto humano vital de las operaciones.
Puntos ciegos del equipo indirecto
MES carece de la flexibilidad para documentar equipos indirectos como HVAC o sistemas de agua purificada sin una gran personalización. Los eLogbooks capturan estas observaciones críticas de forma nativa.
Contexto humano perdido
Los ELB capturan evaluaciones de operadores y juicios situacionales que no son transacciones binarias de aprobación/rechazo. El contexto humano de las operaciones se preserva para auditorías e investigaciones.
Brechas de actividad no estructuradas
La documentación de actividades no estructuradas, como traspasos de turnos y narrativas de excepciones, se admite de forma nativa en eLogbooks frente a la lógica estructurada de MES.

La ventaja del libro de registro electrónico
MES versus libro de registro electrónico: comparación del alcance de la documentación GMP
Comparación del alcance de la documentación entre las capas de Ejecución de fabricación y Libro de registro
| Categoría de actividad | Enfoque MES | Enfoque del libro de registro electrónico |
|---|---|---|
| Limpieza y liquidación | Marca de tiempo de aprobación/fallo | Observaciones visuales y métodos específicos utilizados. |
| Monitoreo de servicios públicos | Alarmas automatizadas | Narrativa situacional de las desviaciones (por ejemplo, HVAC) |
| Transiciones de turnos | N/A (Proceso específico) | Narrativa de continuidad y conocimiento institucional. |
| Calibración | Fecha de referencia | Registros de verificación y comprobaciones manuales de instrumentos. |
| Monitoreo Ambiental | Registros de sensores automatizados | Observaciones del operador, narrativas de desviaciones, notas correctivas. |
| Manejo de materiales | Eventos de escaneo de códigos de barras | Condiciones de recepción, inspecciones visuales, excepciones de almacenamiento. |
Software de registro de equipos GMP para productos farmacéuticos, biotecnológicos y de fabricación regulada
Desde el creador de libros de registro de arrastrar y soltar hasta el software de libros de registro para salas limpias y el software de libros de registro de almacén: todas las funciones están diseñadas para entornos regulados por GxP.
Integración de datos en tiempo real
Las transmisiones en vivo desde PLC, SCADA e instrumentos independientes se transmiten directamente al libro de registro electrónico para la fabricación farmacéutica. Elimine los errores de transcripción manual y garantice la captura de datos contemporánea en toda la instalación.
Generador de libros de registro de arrastrar y soltar
Software de registro de equipos para farmacia
Software de registro de salas limpias
Software de registro de calibración
Software de registro de laboratorio de control de calidad
Libro de registro de monitoreo ambiental
Software de registro de almacén
Libros de registro basados en roles
Listas de verificación y entrelazamiento
Notificaciones y alertas inteligentes
Análisis y paneles
Escaneo de códigos de barras/QR
Acceso sin conexión (aplicación nativa)
Registro habilitado por voz
Seguimiento de auditoría inmutable
Generación de informes inteligentes
Flujos de trabajo de firma electrónica
Libro de registro electrónico en 4 pilares operativos farmacéuticos
Dominios de registro automatizados consolidados dentro del ecosistema AmpleLogic eLogbook
Registros de área y equipo
- Supervise las operaciones de UTA, enfriadores y calderas con un software de registro de equipos para productos farmacéuticos
- Automatizar el software del libro de registro de calibración y los registros de mantenimiento preventivo
- Realice un seguimiento del ciclo de vida, los cambios de estado y la utilización del libro de registro de mantenimiento del equipo.
- Registrar las condiciones ambientales mediante el cuaderno de vigilancia ambiental de las zonas clasificadas.
Operaciones de laboratorio de control de calidad
- Cerrar la brecha LIMS con el software de registro de laboratorio de control de calidad para inspecciones físicas y desinfección
- Seguimiento del ciclo de vida de la columna y de los registros de uso de instrumentos
- Registrar la preparación, estandarización y caducidad de los reactivos.
- Preparación de medios documentales y pruebas de promoción del crecimiento.
Producción y almacén
- Digitalice registros de dispensación, embalaje y recubrimiento con el software de registro de producción farmacéutica
- Software de registro de almacén para manejo de materiales y registros ambientales
- Realice un seguimiento de los controles durante el proceso y de las actividades de limpieza de líneas.
- Inicio/detención de lotes de documentos, conciliación de rendimiento y excepciones
Calidad y cumplimiento
- Automatizar OOC, solicitudes de extensión y registros de desviaciones
- Registrar la asistencia a la capacitación y los registros de emisión de materiales.
- Gestionar narrativas de control de cambios y evaluaciones de impacto.
- Seguimiento de las acciones de CAPA vinculadas a las observaciones del cuaderno de bitácora

Hoja de ruta de implementación
Evaluación heredada
Identifique registros en papel de alto riesgo y equipos antiguos que carecen de salida digital. Mapee las lagunas críticas en la documentación y priorice áreas para lograr el máximo impacto en el cumplimiento.
Superposición no intrusiva
Implemente plantillas de eLogbook sin modificar la lógica de control subyacente ni el código PLC/SCADA validado. Evite costosos ciclos de revalidación con la integración de solo lectura.
Validación y formación
Ejecutar protocolos de validación 21 CFR Parte 11 y capacitar a los operadores en captura de observación digital. Se incluye documentación completa de IQ/OQ/PQ.
Sinergia empresarial
Integre los datos del eLogbook con MES, ERP, eQMS y LIMS para obtener informes operativos unificados. Logre una única fuente de información en toda la empresa de fabricación.
Generación automática impulsada por IA de registros GxP a partir de plantillas de Word para reducir el tiempo de documentación
El motor de código bajo de AmpleLogic convierte instantáneamente plantillas de Word estándar en registros electrónicos totalmente compatibles y con seguimiento de versiones: la generación automática de registros impulsada por IA a partir de plantillas de Word elimina por completo la configuración manual.
Generación automática de registros impulsada por IA a partir de plantillas de Word
Cargue cualquier plantilla de Word existente; La IA identifica automáticamente estructuras de datos y mapea campos de cumplimiento sin esfuerzo manual. La generación automática de registros impulsada por IA a partir de plantillas de Word convierte formularios en papel en libros de registro electrónicos digitales al instante, lo que elimina semanas de configuración manual.
Cumplimiento automatizado
Los libros de registro electrónicos generados cumplen inherentemente con los estándares FDA 21 CFR Parte 11 y Anexo 11 de la UE. Este sistema de registro electrónico compatible con GMP ofrece preparación para auditorías globales desde el primer día sin configuración de cumplimiento manual.
Versiones perfectas
El seguimiento integrado captura todos los cambios a lo largo del ciclo de vida del documento. Proporciona un seguimiento de auditoría transparente e inmutable con trazabilidad completa de quién cambió qué y cuándo.
Implementación rápida (10 veces más rápida)
Logre el estado de entrada en funcionamiento 10 veces más rápido que los métodos tradicionales. La IA reduce drásticamente el tiempo que los equipos empresariales dedican a la configuración, validación y creación de plantillas.
Detección de anomalías
La IA detecta datos atípicos para identificar errores, problemas de cumplimiento o condiciones fuera de especificación en tiempo real. Las alertas proactivas previenen las desviaciones antes de que aumenten.
Mantenimiento predictivo
La IA predice fallas en los equipos utilizando datos históricos del libro de registro y tendencias de los sensores. Las alertas automatizadas evitan el tiempo de inactividad no planificado y garantizan el cumplimiento de los programas de mantenimiento.
Alternativa rentable de registro electrónico a las integraciones de software farmacéutico personalizado
Los eLogbooks eliminan la necesidad de interfaces de hardware personalizadas para cada pieza del equipo del taller.
Interfaces de hardware personalizadas para equipos heredados
Integraciones de puntos y hardware personalizadas
Sin hardware personalizado; ELB no intrusivo
Cronogramas de implementación
Programas MES largos (años)
Implementación rápida del ELB (meses)
Mantenimiento y actualizaciones del ciclo de vida
Sistemas estrechamente acoplados
Arquitectura ELB desacoplada
Un camino hacia la madurez digital
Digitalización pragmática
Reemplace los registros en papel con libros de registro electrónicos para lograr un cumplimiento inmediato y la integridad de los datos. Logre la preparación para la auditoría sin interrumpir los sistemas validados.
Estandarización de plantillas
Unifique la documentación en turnos, sitios y departamentos para garantizar la retención del conocimiento institucional y prácticas GxP consistentes a nivel mundial.
Contexto integrado
Sinergice los datos del eLogbook con las métricas de MES para obtener una vista holística de 360 grados del lote. Habilite el análisis predictivo y la mejora continua.
Digitalización de entornos GxP heredados con software de registro electrónico que cumple con las normativas
Integración no intrusiva con instrumentos independientes, PLC, sistemas SCADA y aplicaciones empresariales
eQMS
Flujos de trabajo automatizados de control de cambios, CAPA y desviaciones vinculados a las observaciones del libro de registro
LIMAS
Sincronice los resultados de laboratorio, los registros de instrumentos y el seguimiento de muestras de control de calidad en tiempo real
ERP y mantenimiento
Integre el estado del equipo, repuestos y cronogramas de mantenimiento preventivo.
eBMR/MES
Uso compartido de contexto por lotes bidireccional entre registros de ejecución y registros de observación
PLC / SCADA / Registrador de datos
Conexiones no intrusivas de solo lectura a través de protocolos RS 232/485, Ethernet, API u OPC
Aplicaciones de terceros
Conectividad API abierta y CAMS/OPC/Link Server para cualquier integración de sistema externo
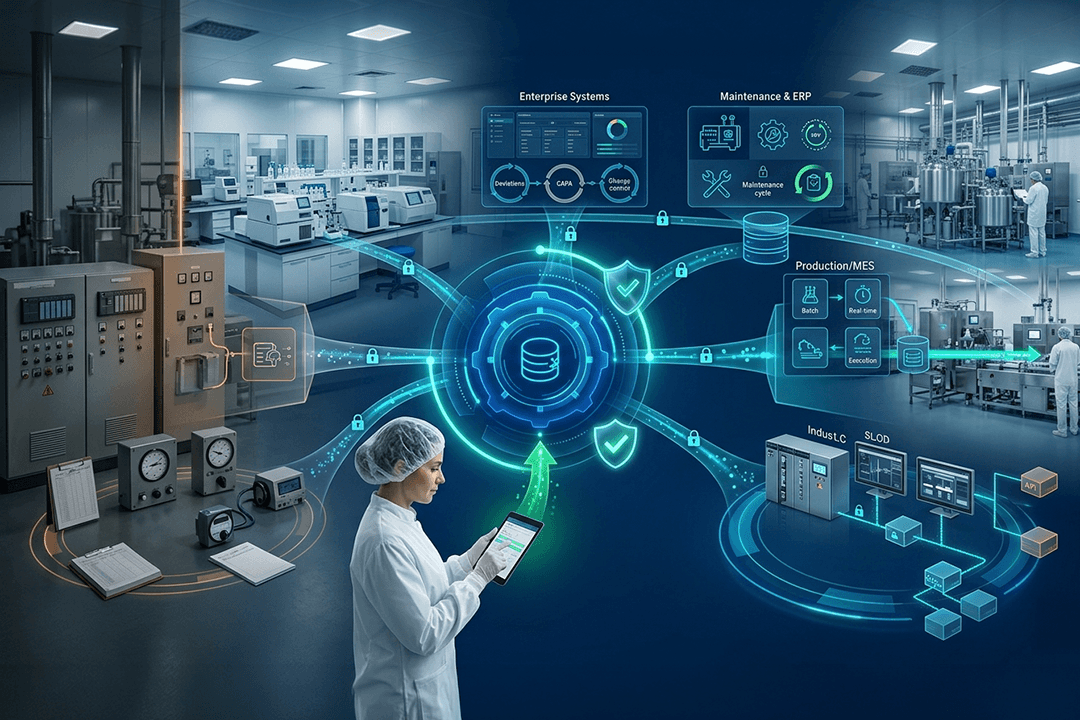
Integridad lógica del equipo
Logre la digitalización sin modificar el código PLC o SCADA validado. Las conexiones no intrusivas y de solo lectura evitan costosos ciclos de revalidación y al mismo tiempo capturan el contexto operativo completo.
Industrias que utilizan el libro de registro electrónico AmpleLogic para la fabricación farmacéutica GMP
Soluciones de libros de registro electrónicos que cumplen con GxP, desde software de libros de registro para salas limpias y software de libros de registro de laboratorio de control de calidad hasta software de libros de registro de almacenes, diseñados para entornos de fabricación regulados.
Productos farmacéuticos
Libro de registro electrónico de extremo a extremo para la fabricación farmacéutica: digitalice I+D, API, formulación y producción de dosis terminadas con capacidades del sistema de registro electrónico que cumplen con GMP.
Biotecnología
Libros de registro sin papel especializados en la fabricación farmacéutica para entornos de bioprocesamiento, fermentación, cultivo celular y producción de productos biológicos.
Dispositivos médicos
Software de registro de salas blancas compatible con operaciones de fabricación, esterilización, ensamblaje y embalaje de dispositivos médicos.
Alimentos y bebidas
Libros de registro digitales alineados con HACCP para flujos de trabajo de registros de producción, saneamiento, CIP/COP y monitoreo ambiental en la fabricación de alimentos.
Terapia genética
Registro de precisión para la producción de vectores virales, la fabricación de terapias celulares y la gestión de la cadena de frío con el cumplimiento farmacéutico del cuaderno de registro de equipos electrónicos.
Cosmética y Belleza
Libros de registro electrónicos que cumplen con GMP para fabricación por lotes, control de calidad y monitoreo de higiene con tecnología de software de registro de producción farmacéutica.
Lo que dicen las críticas de G2 AmpleLogic libro de registro electrónico
"Las funciones de seguimiento de auditoría y cumplimiento son excelentes. Es compatible con FDA 21 CFR Parte 11 y Anexo 11 de la UE, lo que nos brinda plena confianza en nuestros registros electrónicos."
Usuario verificada
Garantía de Calidad, Farmacéutica
"La armonización de los registros entre departamentos es perfecta. El seguimiento del uso del equipo y la integración con nuestro eDMS y LMS hicieron que la adopción fuera muy fluida."
Gerente de TI
Farmacéutica del mercado medio
"La implementación fue rápida y el equipo de soporte es muy receptivo. La interfaz de usuario basada en web simplifica las tareas diarias del libro de registro para nuestros operadores."
Supervisora de control de calidad
Empresa farmacéutica
Logre un 100 % de preparación para las auditorías con libros de registro sin papel
Únase a las empresas líderes en ciencias biológicas que utilizan el libro de registro electrónico AmpleLogic para la fabricación farmacéutica para eliminar los riesgos de cumplimiento manual y acelerar la transformación digital con libros de registro sin papel impulsados por IA en la fabricación farmacéutica.
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.