Suivez chaque soumission et enregistrement à l'échelle mondiale
Système de gestion des informations réglementaires conçu spécifiquement pour l'industrie pharmaceutique — automatisez les soumissions, suivez les dossiers ANDA & DMF, et gérez les cycles de vie des médicaments dans plus de 120 pays grâce à un logiciel de conformité réglementaire propulsé par l'IA.
120+
Pays pris en charge
50%
Soumissions accélérées
100%
Prêt pour l'audit
24/7
Surveillance de la conformité
Défis du RIMS : Pourquoi la gestion réglementaire manuelle est insuffisante
Défis critiques qui entravent la conformité, les soumissions et l'accès au marché
Réglementations mondiales en constante évolution
Suivre le rythme de la FDA, de l'EMA, de la MHRA, du CDSCO, de l'OMS, de Santé Canada, de la TGA et de plus de 100 autorités régionales exige une vigilance permanente et une adaptation rapide.
Données réglementaires fragmentées
Les informations réglementaires critiques dispersées dans les e-mails, les tableurs, les lecteurs partagés et les systèmes hérités créent des angles morts et des lacunes en matière de conformité.
Formats de soumission complexes
La gestion des soumissions eCTD, ACTD, NeeS et papier dans différentes régions nécessite une expertise spécialisée et une coordination manuelle sujette aux erreurs.
Visibilité et suivi insuffisants
Absence de tableau de bord unifié pour le statut en temps réel des soumissions mondiales, des approbations, des requêtes et des calendriers de renouvellement sur tous les marchés.
Processus manuels et sujets aux erreurs
La forte dépendance aux communications par e-mail, à la saisie manuelle des données et aux tableurs déconnectés augmente le risque de délais non respectés et de pénalités réglementaires.
Défis d'intégration
Les systèmes QMS, DMS, ERP et Sécurité déconnectés entraînent une duplication des données, des incohérences et ralentissent les flux de travail réglementaires transverses.
Problèmes d'évolutivité
Les portefeuilles de produits croissants à travers les zones géographiques augmentent exponentiellement la complexité réglementaire, dépassant les capacités des approches manuelles de suivi.
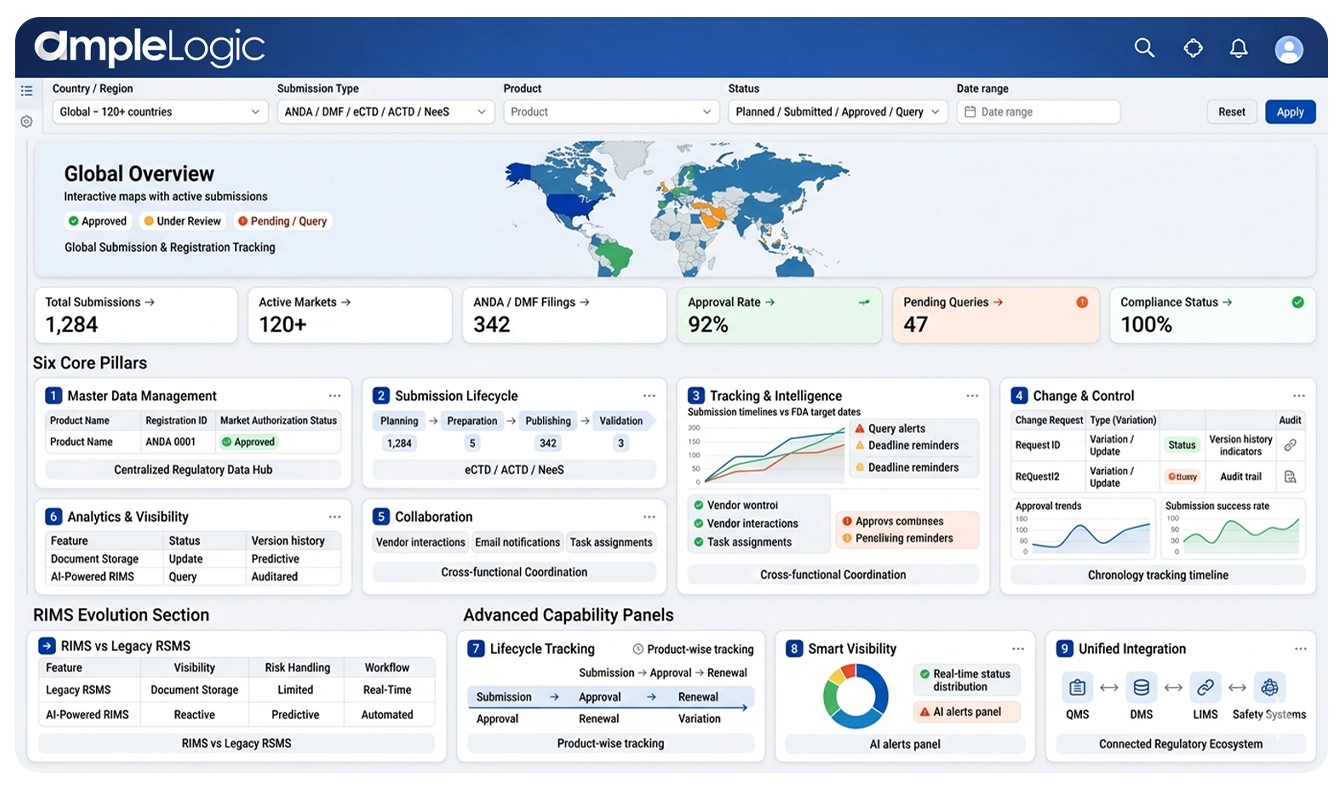
Aperçu du logiciel AmpleLogic RIMS
Six piliers permettant une gestion complète du cycle de vie réglementaire
Gestion des données de référence
Enregistrement centralisé des produits, autorisation de mise sur le marché mondiale et suivi du cycle de vie auprès de toutes les autorités réglementaires.
Cycle de vie des soumissions
Flux de travail automatisés pour la planification, la préparation, la publication et la validation des soumissions eCTD, ACTD et NeeS, avec suivi ANDA et DMF.
Suivi et intelligence
Statut des soumissions en temps réel, gestion des approbations et des requêtes, dates cibles FDA et surveillance proactive des délais sur tous les marchés.
Gestion des changements et contrôle
Contrôle des modifications, gestion des variations et processus d'amélioration continue (CIP) avec pistes d'audit complètes et historique des versions.
Collaboration
Coordination des fournisseurs, notification des clients et alertes par e-mail automatisées pour des flux de travail réglementaires transverses fluides.
Analytique et visibilité
Tableaux de bord graphiques, suivi chronologique, analytique du cycle de vie et intelligence prête pour la conformité pour des décisions réglementaires éclairées.
RIMS : La prochaine évolution du RSMS
Alors que les plateformes RSMS héritées étaient de simples entrepôts de documents passifs, le RIMS est un écosystème de gestion réglementaire intelligent et propulsé par l'IA qui favorise activement la conformité, prédit les risques et accélère la mise sur le marché.
Gestion des données
Enregistrement complet des produits et données réglementaires mondiales dans un système centralisé avec gouvernance des données de référence et suivi du cycle de vie.
Suivi du cycle de vie
Surveillance des approbations, des variations et des renouvellements pour assurer une conformité réglementaire continue sur tous les marchés.
Visibilité intelligente
Visibilité mondiale en temps réel et surveillance proactive grâce à des alertes intelligentes et des tableaux de bord de conformité.
Intégration unifiée
Intégration transparente avec les systèmes QMS, DMS, LIMS et Sécurité pour construire un écosystème de gestion réglementaire unifié.
Modules de flux de travail RIMS : Gestion du cycle de vie des soumissions
Huit modules interconnectés guidant les processus réglementaires, de la stratégie à la conformité continue
Fondation des données réglementaires
Configuration du marché mondial et référentiel de données de référence pour le suivi du cycle de vie des DMF, CEP, LOA et produits auprès de toutes les autorités.
Planification des soumissions
Développement de stratégies, gestion des délais, suivi des jalons et allocation des ressources pour les soumissions réglementaires mondiales.
Préparation des soumissions
Compilation des dossiers, contrôle des versions et assemblage des documents pour la conformité eCTD / ACTD / NeeS avec vérifications de validation automatisées.
Exécution des soumissions
Validation, publication auprès des autorités sanitaires, soumission via passerelle, suivi ANDA et surveillance en temps réel du statut auprès des autorités.
Gestion de l'examen
Suivi des requêtes, gestion des insuffisances, journaux de communication avec les autorités et surveillance des délais de réponse sur tous les marchés.
Gestion du cycle de vie du médicament
Variations, renouvellements, modifications post-approbation et mises à jour des étiquettes avec suivi complet du cycle de vie et alertes automatisées.
Surveillance de la conformité
Alertes automatisées, suivi des engagements, préparation aux inspections et veille réglementaire proactive.
Analytique et rapports
Tableaux de bord en temps réel, rapports graphiques, informations sur les soumissions mondiales et analyses spécifiques GDUFA/autorités.

Orchestration de bout en bout
Chaque module de flux de travail s'intègre de manière transparente avec les systèmes QMS, DMS, LIMS et Sécurité, éliminant les silos de données et les transferts manuels tout au long du cycle de vie réglementaire.
Fonctionnalités clés du logiciel AmpleLogic RIMS
Douze capacités critiques permettant l'excellence réglementaire
Suivi des enregistrements de produits
Suivez les enregistrements de produits dans plus de 120 pays avec des mises à jour de statut automatisées, des alertes de délais et une gestion complète du cycle de vie des médicaments.
Préparation et publication des soumissions
Surveillance des approbations et rejets
Tracker ANDA et dates cibles FDA
Tracker DMF et contrôle des modifications
Gestion des engagements et des variations
Gestion des fournisseurs et des parties prenantes
Rapports graphiques et tableaux de bord
Flux de travail réglementaires pharmaceutiques automatisés
Signatures électroniques et pistes d'audit
Référentiel documentaire centralisé
Moteur de validation des soumissions
RIMS propulsé par l'IA : Analytique réglementaire intelligente
Six capacités propulsées par l'IA accélérant les flux de travail réglementaires et réduisant les risques
Suivi de la conformité par IA
Surveille et s'adapte en permanence à l'évolution des normes réglementaires locales et mondiales, en mettant automatiquement à jour les processus pour garantir la conformité sans intervention manuelle.
Analytique prédictive
Analyse les données historiques et en temps réel pour identifier les risques potentiels et les lacunes de conformité avant qu'ils ne s'aggravent, permettant de remédier proactivement aux problèmes et d'éviter les pénalités.
Rapports automatisés
L'IA automatise la génération de rapports et de documentation réglementaires, garantissant leur exactitude, leur ponctualité et leur conformité aux exigences d'audit avec une intervention humaine minimale.
Moteur d'atténuation des risques
Des algorithmes propulsés par l'IA évaluent les schémas de données pour signaler les risques de conformité potentiels, offrant des perspectives prédictives et recommandant des actions correctives.
Intelligence sur les changements réglementaires
Suit et traite les modifications réglementaires en temps réel, en les intégrant automatiquement dans vos systèmes pour assurer la conformité continue aux dernières normes.
Optimisation des flux de travail
L'IA optimise les flux de travail, minimisant les coûts opérationnels, accélérant les processus réglementaires et garantissant une conformité cohérente à tous les niveaux de l'entreprise.
Trackers réglementaires mondiaux : Surveillance FDA, EMA & RoW
Trois modules de suivi régional pour une autorisation de mise sur le marché complète
Tracker réglementaire FDA USA
Tracker ANDA et tracker DMF avec jalons du cycle de vie FDA incluant les dates d'action cibles IND, NDA, ANDA, BLA, les frais GDUFA et les soumissions 505(b)(2).
Tracker réglementaire UE & Royaume-Uni
Gérez les procédures EMA et MHRA, les variations centralisées/décentralisées/de reconnaissance mutuelle, les calendriers PSUR et les soumissions post-Brexit au Royaume-Uni avec des flux de travail automatisés.
Tracker réglementaire mondial RoW
Rationalisez les soumissions APAC, LATAM, MENA et Afrique avec un suivi du cycle de vie spécifique à chaque pays pour Santé Canada, TGA, CDSCO, OMS PQ et plus de 100 autorités.
Conformité RIMS : Normes réglementaires mondiales
Prise en charge complète des cadres réglementaires mondiaux et des normes de conformité
Prise en charge des principales autorités
Couverture complète de la FDA américaine, de l'EMA, de la MHRA, de l'OMS, de Santé Canada, de la TGA, du CDSCO, de l'ANVISA, du PMDA et de plus de 100 autorités sanitaires mondiales.
Gestion des formats multi-régions
Prise en charge native des formats eCTD, ACTD, NeeS et papier avec surveillance automatisée des renouvellements et validation spécifique aux formats.
21 CFR Part 11 & EU Annex 11
Contrôles entièrement conformes incluant les signatures électroniques, les pistes d'audit, les mesures de protection de l'intégrité des données et le contrôle sécurisé des versions.
Surveillance proactive et alertes
Alertes automatisées pour les délais, les dates d'échéance des engagements, les fenêtres de renouvellement et les modifications réglementaires avec réduction des risques en temps réel.
Conformité IDMP
Prend en charge les normes ISO IDMP pour les données sur les substances, les produits, les organisations et les données de référence afin de se préparer aux exigences d'identification de l'EMA.
Prêt pour ICH eCTD 4.0
Pérennisé pour le modèle de données eCTD 4.0 de nouvelle génération avec planification structurée du contenu, gestion des métadonnées et capacités de soumission aux autorités.
AmpleLogic RIMS vs. Concurrents
Comment AmpleLogic surpasse les RIMS hérités et les solutions ponctuelles
| Capacité | AmpleLogic RIMS | Concurrents |
|---|---|---|
| Architecture | Low-Code / No-Code sur aPaaS unifié | Architecture rigide, personnalisation importante requise |
| Approche des données | Référentiel de données de référence unifié | Données fragmentées entre modules et silos |
| Couverture du cycle de vie | De bout en bout (de la planification au suivi post-approbation) | Nécessite souvent des modules complémentaires séparés |
| Intégration | Transparente (QMS, DMS, ERP, Sécurité, LIMS) | Autonome, coût et effort d'intégration élevés |
| Automatisation & IA | Alertes propulsées par l'IA, analytique prédictive, rapports automatiques | Automatisation limitée, flux de travail manuels statiques |
| Coût total de possession | TCO réduit, déploiement rapide, paiement à l'usage | Frais de licence élevés et coûts de maintenance continus |
| Vitesse de déploiement | Quelques semaines avec des modèles pré-validés | Des mois à des années de mise en œuvre |
| Conformité eCTD 4.0 | Pérennisé avec un modèle de données structuré | Dépendant de la feuille de route, calendrier incertain |
Intégrations entreprise RIMS
Dix modules d'intégration reliant les systèmes réglementaires, qualité et de fabrication
eQMS
Contrôle des modifications bidirectionnel, CAPA et liaison des déviations
DMS
Documents réglementaires et SOPs avec contrôle des versions
LMS
Registres de formation et gestion des compétences
LIMS
Données analytiques et intégration des CoA pour les soumissions
eLogbook
Données de cahiers de laboratoire GxP liées aux dossiers réglementaires
eBMR/MES
Données des dossiers de lots pour les soumissions réglementaires
CVS
Données de validation du nettoyage pour les dépôts réglementaires
CAPS
Registres d'étalonnage des équipements pour la conformité
SAP/Oracle
Synchronisation des données de référence des matières et de la chaîne d'approvisionnement
PV
Données sur les événements indésirables et intégration PSUR/PBRER
ROI RIMS : Impact réglementaire mesurable
Impact quantifié de la gestion du cycle de vie réglementaire assistée par l'IA
Préparation des soumissions
50 à 60 % plus rapideProcessus manuel
8 à 12 semaines
Avec AmpleLogic RIMS
3 à 5 semaines
Saisie des données réglementaires
Réduction de 75 %Processus manuel
40+ heures/semaine
Avec AmpleLogic RIMS
8 à 10 heures/semaine
Respect des délais
Quasi-zéro délai manquéProcessus manuel
85 à 90 % dans les délais
Avec AmpleLogic RIMS
99 %+ dans les délais
Délai de réponse aux requêtes
Réponse 70 % plus rapideProcessus manuel
5 à 10 jours ouvrables
Avec AmpleLogic RIMS
1 à 3 jours ouvrables
Préparation aux audits
90 % de gain de tempsProcessus manuel
2 à 4 semaines
Avec AmpleLogic RIMS
En quelques heures (toujours prêt)
Génération de rapports
95 % plus rapideProcessus manuel
3 à 5 jours par rapport
Avec AmpleLogic RIMS
En quelques minutes (généré automatiquement)
Référencé dans le rapport Gartner
AmpleLogic RIMS a été reconnu comme fournisseur représentatif dans le guide de marché Gartner® pour les solutions de gestion des informations réglementaires dans les sciences de la vie, septembre 2024 (ID G00769345).
Secteurs desservis par AmpleLogic RIMS
Huit secteurs verticaux tirant parti d'AmpleLogic RIMS pour l'excellence réglementaire
Pharmaceutique
Logiciel réglementaire conforme aux BPF pour l'enregistrement des médicaments, les soumissions NDA/ANDA et l'autorisation de mise sur le marché mondiale avec une gestion complète du cycle de vie
Biotechnologie
Soumissions BLA, enregistrements de biosimilaires et gestion du cycle de vie des produits biologiques complexes
Dispositifs médicaux
Soumissions 510(k), PMA, marquage CE, EUDAMED/UDI et gestion de la classification des dispositifs
Thérapie génique
Soumissions IND/BLA pour les thérapies avancées avec suivi spécialisé des voies réglementaires
Fabricants d'API
Tracker DMF pour les demandes CEP et l'enregistrement mondial des API auprès des autorités
Alimentation & Boissons
Enregistrements d'additifs alimentaires, demandes de nouveaux aliments et soumissions de déclarations de santé
Cannabis & Tabac
Suivi réglementaire spécialisé pour les licences cannabis et les soumissions de produits du tabac
Cosmétiques
Notifications de produits cosmétiques, enregistrements CPNP/FDA et suivi de la conformité des ingrédients
Prêt à transformer vos opérations réglementaires ?
Remplacez les tableurs fragmentés et le suivi manuel par une intelligence réglementaire propulsée par l'IA, prête pour l'audit.
Gardez une longueur d'avance dans les sciences de la vie
Recevez les dernières mises à jour produit, actualités de conformité et analyses du secteur directement dans votre boîte mail.