Secteur des Sciences de la Vie Tendances & Perspectives
Points de vue d'experts sur la fabrication pharmaceutique, la conformité, l'automatisation par IA et la transformation numérique dans les sciences de la vie.

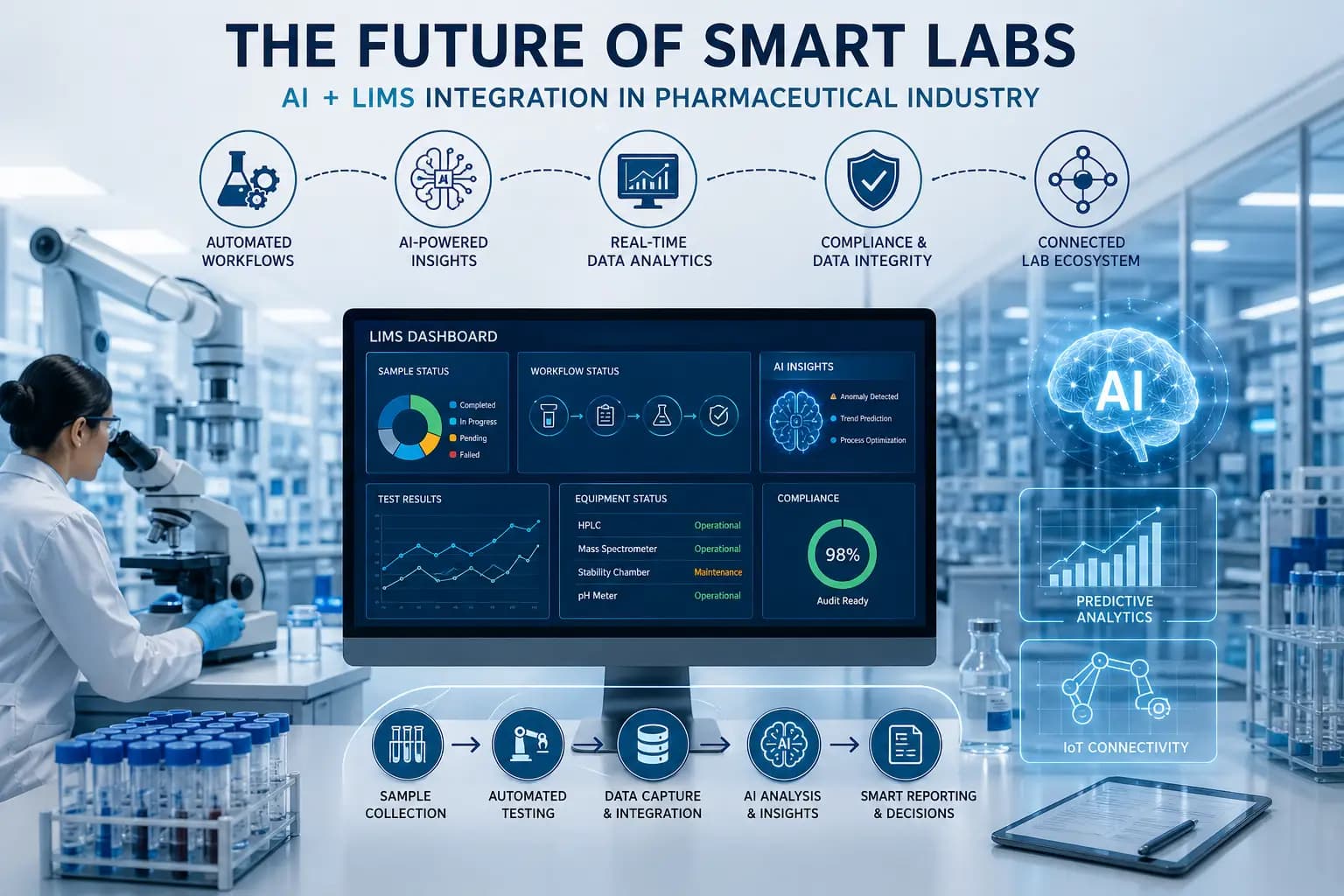
L’avenir de l’intelligence artificielle des Smart Labs et de l’intégration LIMS dans l’industrie pharmaceutique

Plateforme d'applications en tant que service
Application Platform as a Service (aPaaS) est un modèle de cloud computing qui fournit un environnement complet pour créer, déployer et gérer des applications sans gérer l'infrastructure sous-jacente. Il permet aux entreprises d'accélérer le développement, de réduire les coûts et de faire évoluer efficacement leurs applications. En proposant des outils, des cadres et l'automatisation, l'aPaaS simplifie l'ensemble du cycle de vie des applications, de la conception au déploiement, aidant les organisations à innover plus rapidement et à rester compétitives dans un monde axé sur le numérique.

Bref sur gamp 5 catégories v modèle et 21 cfr partie 11 eu annexe 11
GAMP 5 fournit une approche structurée pour valider les systèmes informatisés dans l'industrie pharmaceutique, garantissant qu'ils sont adaptés à l'utilisation prévue et alignés sur les attentes réglementaires. Il fonctionne aux côtés de frameworks tels que le V-Model, qui prend en charge un processus de validation basé sur le cycle de vie, depuis les exigences jusqu'aux tests. Des réglementations telles que 21 CFR Part 11 et l'Annexe 11 de l'UE définissent des règles strictes pour les enregistrements et les signatures électroniques, garantissant l'intégrité, la sécurité et la traçabilité des données entre les systèmes. Ensemble, ces normes créent un solide écosystème de conformité dans lequel les organisations peuvent développer, mettre en œuvre et maintenir efficacement des systèmes logiciels validés. En combinant la validation basée sur les risques, la gestion du cycle de vie et l'alignement réglementaire, les entreprises peuvent réduire les risques de non-conformité, améliorer la qualité des produits et accélérer la transformation numérique des opérations pharmaceutiques.

Plateforme low-code
Une plate-forme low-code permet aux organisations de concevoir, développer et déployer des applications avec un minimum de codage manuel à l'aide d'interfaces visuelles et de composants prédéfinis. Pour les sociétés pharmaceutiques, elle offre un moyen plus rapide et plus conforme de numériser les processus, d'automatiser les flux de travail et de faire évoluer les opérations tout en préservant les normes réglementaires et l'intégrité des données.

Logiciel d'émission d'enregistrements de lots (BMR) et de génération de numéros de lots pharmaceutiques
Les logiciels d'émission de lots d'enregistrements (BMR) et de génération de numéros de lots aident les sociétés pharmaceutiques à automatiser et à contrôler les processus de fabrication critiques. Il garantit un suivi précis des lots, réduit les erreurs manuelles et maintient la conformité aux normes réglementaires en fournissant des flux de travail numériques sécurisés, traçables et efficaces.

Automatisation des processus pharmaceutiques par lots AQ/CQ Usines USFDA MHRA CGMP
L'automatisation des processus par lots d'AQ/CQ pharmaceutiques permet aux entreprises de rationaliser les activités d'assurance et de contrôle qualité tout en garantissant la conformité aux normes USFDA, MHRA et cGMP. En numérisant les flux de travail et en automatisant les processus critiques, les organisations peuvent améliorer l’intégrité des données, réduire les erreurs manuelles et accélérer la libération des lots.

Plateforme de développement d'applications Low Code
Une plate-forme de développement d'applications low-code permet aux organisations de concevoir, créer et déployer rapidement des applications à l'aide d'outils visuels et d'un minimum de codage. Dans l’industrie pharmaceutique, il prend en charge une innovation plus rapide, une conformité améliorée et une automatisation efficace des flux de travail tout en préservant l’intégrité des données et les normes réglementaires.

Plateforme apaas Low Code
Une plate-forme aPaaS (Application Platform as a Service) low-code fournit un environnement basé sur le cloud pour créer, déployer et gérer rapidement des applications avec un minimum de codage. Il permet aux organisations pharmaceutiques de rationaliser les flux de travail, de garantir la conformité et de faire évoluer efficacement leurs opérations tout en accélérant la transformation numérique.

GMP (SOP) Planificateur de formation Logiciel de suivi de gestion Pharmaceutique
Le logiciel de planification, de gestion et de suivi de la formation GMP SOP aide les sociétés pharmaceutiques à gérer efficacement les programmes de formation des employés tout en garantissant la conformité réglementaire. En automatisant les calendriers de formation, en suivant les progrès et en conservant des enregistrements prêts à être audités, les organisations peuvent améliorer les compétences de leur personnel et rationaliser les processus de conformité.

Logiciel de gestion CAPA
Le logiciel de gestion CAPA aide les organisations pharmaceutiques à gérer efficacement les actions correctives et préventives pour remédier aux écarts et améliorer les processus qualité. En automatisant les flux de travail et en garantissant la traçabilité, il améliore la conformité, réduit les risques et soutient l'amélioration continue.

Logiciel de suivi d'automatisation du contrôle des modifications Pharmaceutique
Les logiciels d'automatisation et de suivi du contrôle des modifications aident les organisations pharmaceutiques à gérer, documenter et suivre efficacement les modifications tout en garantissant la conformité réglementaire. En automatisant les flux de travail et en conservant des pistes d'audit, il améliore la traçabilité, réduit les risques et améliore les processus de gestion de la qualité.

Logiciel d'automatisation du système de gestion de la qualité (QMS) Pharmaceutique Biotechnologie
Le logiciel d'automatisation QMS aide les entreprises pharmaceutiques et biotechnologiques à rationaliser les processus qualité, à gérer la conformité et à améliorer l'efficacité opérationnelle. En automatisant les flux de travail tels que CAPA, les écarts, les audits et le contrôle des documents, il garantit une qualité constante et le respect des réglementations.

Outil de gestion de serveur Exchange
Un outil de gestion Exchange Server aide les organisations à gérer, surveiller et sécuriser efficacement leur infrastructure de messagerie. En automatisant les tâches administratives, en suivant les performances et en améliorant la sécurité, il garantit une communication fiable et des opérations informatiques rationalisées.

Plateforme de développement d'applications sans code
Une plate-forme de développement d'applications sans code permet aux utilisateurs de créer et de déployer des applications sans écrire de code à l'aide d'interfaces visuelles et de composants prédéfinis. Dans l’industrie pharmaceutique, cela permet une innovation plus rapide, une conformité améliorée et une automatisation efficace des flux de travail.

Automatisations Excel
L'automatisation d'Excel simplifie les tâches répétitives en utilisant des outils, des macros et des flux de travail pour améliorer l'efficacité et la précision. Pour les environnements pharmaceutiques et d’entreprise, il permet un traitement des données plus rapide, réduit les erreurs manuelles et améliore la productivité grâce à des opérations rationalisées.

Système de surveillance environnementale (EMS)
Un système de surveillance environnementale (EMS) est essentiel pour les installations pharmaceutiques et biotechnologiques afin de surveiller les conditions environnementales critiques telles que la température, l'humidité, la pression et la contamination microbienne. Il garantit la qualité des produits, la conformité réglementaire et la réduction des risques en fournissant des données en temps réel, des alertes automatisées et une traçabilité complète dans les environnements de fabrication.

Suite de qualité
Une Quality Suite est une plateforme intégrée qui aide les entreprises pharmaceutiques et biotechnologiques à gérer les processus qualité tels que les CAPA, les écarts, les audits et le contrôle des documents. En automatisant les flux de travail et en garantissant la conformité, il améliore l'efficacité, l'intégrité des données et la qualité globale des produits.

Système de gestion des actifs
Un système de gestion des actifs aide les organisations à suivre, gérer et optimiser le cycle de vie des actifs, de l'approvisionnement à la maintenance et à l'élimination. Dans les environnements pharmaceutiques et d'entreprise, il garantit l'efficacité opérationnelle, réduit les temps d'arrêt et prend en charge la conformité réglementaire.

Logiciel de validation de processus
Un logiciel de validation de processus aide les sociétés pharmaceutiques à garantir que les processus de fabrication produisent systématiquement des produits de qualité. En automatisant les flux de travail de validation et en conservant une documentation détaillée, il améliore la conformité, améliore l'intégrité des données et prend en charge une gestion efficace du cycle de vie.

5 signes que votre processus APQR n'est pas prêt à être conforme
Vous êtes aux prises avec des retards, des feuilles de calcul manuelles ou un manque de traçabilité dans votre processus APQR ? Ce sont des signes clairs que votre examen annuel de la qualité des produits n’est peut-être pas prêt à être conforme. Découvrez les 5 principaux signaux d'alarme et découvrez comment les systèmes APQR numériques peuvent améliorer l'efficacité, garantir la préparation aux audits et renforcer la conformité réglementaire des opérations pharmaceutiques.

Erreurs courantes lors de l'examen annuel de la qualité des produits (APQR) et comment les éviter
Vous êtes aux prises avec des inefficacités dans votre processus APQR ? Des erreurs courantes telles que des données incomplètes, un manque de standardisation et une mauvaise traçabilité peuvent avoir un impact sur la conformité et la prise de décision. Apprenez à éviter ces pièges et améliorez votre examen annuel de la qualité des produits grâce à une approche numérique structurée.

Comment améliorer la préparation aux audits dans le secteur pharmaceutique grâce aux systèmes APQR numériques
Vous avez du mal à rester prêt pour les audits dans le secteur pharmaceutique ? Les processus APQR manuels entraînent souvent des retards, une mauvaise traçabilité et des risques de non-conformité. Découvrez comment les systèmes APQR numériques améliorent la préparation aux audits grâce à des données centralisées, une visibilité en temps réel, une documentation automatisée et des pistes d'audit complètes.

No-Code pour la fabrication : signification, avantages et tendances pour les équipes pharmaceutiques

Cipla implémente AmpleLogic Secure Snap pour la conformité GMP

Réduire les erreurs humaines dans la fabrication pharmaceutique grâce à des solutions numériques

Votre logiciel d’application est-il obsolète ou simplement sécurisé ?

Comment répondre efficacement aux normes FDA 483 et éviter les erreurs courantes

Gartner reconnaît Amplelogic dans son guide du marché pour les systèmes de gestion de l'information de laboratoire

L'intégration de QMS avec ERP, LMS et LIMS peut améliorer la conformité et l'efficacité de 70 % en 2025

Faits saillants passionnants de l’AL Ideathon 2024 !

Qu’est-ce que le Master Batch Record (MBR) ?

Exploiter la puissante force du rapport sur la qualité des produits

Le guide ultime du logiciel d'enregistrement électronique des lots

Étude de cas de Sun Pharma – Solution de journal de bord numérique

Implémentation du système eQMS chez Ind-Swift Laboratories Ltd

Windlas est lancé avec le système de gestion électronique de documents AmpleLogic

Indoco Remedies est lancé avec le système AmpleLogic DMS

Bharat Serums and Vaccines Limited a été mis en service avec le système APQR

Le système de gestion de la qualité est mis en service chez FDC Limited

Laurus Labs choisit AmpleLogic pour mettre en œuvre un logiciel d'étalonnage et de maintenance préventive

Implémentation du logiciel EQMS chez Bharat Serums and Vaccines Limited

Implémentation du système EQMS chez Pontika Aerotech

OCuSOFT Inc lance la solution AmpleLogic DMS

Vieco Pharmaceuticals lance le système AmpleLogic DMS et QMS

Caplin Steriles lance le module de plaintes du marché AmpleLogic

Umedica a été mis en service avec succès avec le système EDMS

Slayback Pharma lance la solution AmpleLogic EDMS

Bharat Serums and Vaccines Limited est lancé avec le système LMS AmpleLogic

Institut du sérum de l'Inde Pvt. Ltd démarre avec le logiciel LMS AmpleLogic

Implémentation de la solution QMS chez Umedica Laboratories Pvt. Ltée

Chemo India utilise le logiciel LMS AmpleLogic

Comment choisir le bon LMS pour la formation à la conformité

Étude de cas de Shilpa Medicare Limited – Logiciel EDMS

Étude de cas sur le système logiciel de gestion de formation SOP et GMP

Étude de cas AL Andalous – Logiciel QMS numérique

Hetero Labs utilise AmpleLogic LMS pour gérer les programmes de formation

Étude de cas de Sun Pharma pour Energy Tracker

Étude de cas de Sun Pharma – Feuilles de calcul Excel

Étude de cas du ciblage des ventes du Dr Reddys

Annora Pharma renforce ses opérations Qualité avec le logiciel BIMS

Étude de cas de Sun Pharma – Système MIS

Julphar remplace le QMS manuel par AmpleLogic EQMS

Étude de cas sur le logiciel QMS électronique pharmaceutique

Le parcours de Bharat Serum avec le logiciel APQR

Prix d'été G2 d'Amplelogic 2024

Comparaison des meilleurs fournisseurs de QMS

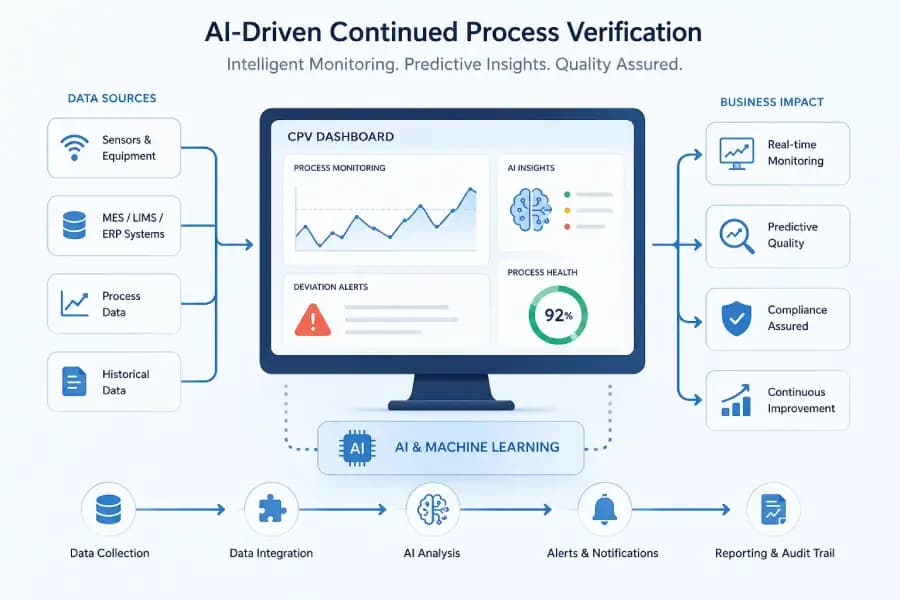
Vérification continue des processus : accélérer l'assurance qualité et la conformité dans la fabrication pharmaceutique

AmpleLogic obtient 21 badges dans le rapport du printemps 2024 de G2

Étude de cas de JSW Steel – Gestion de l’énergie d’entreprise

Les Prix pharmaceutiques CPHL 2018

Étude de cas sur la solution de gestion de la qualité pharmaceutique

Principales attentes de la FDA concernant le CPV dans le cadre de la validation du processus de phase 3
La vérification continue des processus (CPV) de la FDA Stage 3 est une phase critique du cycle de vie de validation des processus qui garantit que les processus de fabrication restent dans un état validé pendant la production commerciale. Il se concentre sur la surveillance continue des paramètres critiques du processus (CPP) et des attributs critiques de la qualité (CQA), à l'aide d'outils statistiques et d'analyses de données en temps réel pour détecter les tendances, la variabilité et les écarts potentiels. En adoptant une approche axée sur le cycle de vie, la FDA souligne que la validation n'est pas une activité ponctuelle mais un processus continu piloté par la gestion des données et des risques. CPV intègre les données de performance des processus dans les examens annuels des produits et les décisions de gestion, permettant une assurance qualité proactive et une conformité réglementaire. Grâce à des solutions numériques avancées comme AmpleLogic, les organisations peuvent rationaliser la mise en œuvre du CPV, améliorer l'intégrité des données et garantir une conformité continue avec l'évolution des attentes de la FDA.

Comment l'IA aide à prévenir la perte de lots grâce à la détection précoce des pannes

Qu'est-ce qu'un système de gestion de documents conforme à la norme 21 CFR Part 11 ?
Un système de gestion de documents conforme à la norme 21 CFR Part 11 est essentiel pour les organisations pharmaceutiques et des sciences de la vie en transition vers des opérations numériques. 21 CFR Part 11 établit les critères selon lesquels les enregistrements électroniques et les signatures électroniques sont considérés comme dignes de confiance, fiables et équivalents à la documentation sur papier. En mettant en œuvre un système de gestion de documents conforme, les organisations peuvent créer, stocker, récupérer et gérer en toute sécurité des documents réglementés tout en conservant des pistes d'audit complètes, un accès contrôlé et des flux de travail validés. Ces systèmes contribuent à garantir l'intégrité des données, à empêcher les modifications non autorisées et à prendre en charge les inspections réglementaires en fournissant des enregistrements traçables et infalsifiables. Avec des solutions comme AmpleLogic, les entreprises peuvent numériser les processus de contrôle des documents, automatiser les approbations à l'aide de signatures électroniques et assurer une conformité transparente avec les réglementations de la FDA, améliorant ainsi l'efficacité opérationnelle, réduisant les risques de non-conformité et garantissant la préparation aux audits dans les fonctions qualité et réglementaires.

Autorisation FDA 510(k) : Un guide pratique pour les fabricants de dispositifs médicaux
Le processus d'autorisation FDA 510(k) constitue une voie réglementaire essentielle pour les fabricants de dispositifs médicaux cherchant à pénétrer le marché américain. Également connue sous le nom de notification préalable à la commercialisation, elle oblige les entreprises à démontrer que leur dispositif est « substantiellement équivalent » à un dispositif sous-jacent déjà légalement commercialisé en termes de sécurité et d’efficacité. Principalement applicable aux appareils de classe II et à certains appareils de classe I, le processus 510(k) implique la soumission d'une documentation détaillée, comprenant des descriptions d'appareils, l'utilisation prévue, l'étiquetage, l'analyse des risques et les données de tests de performances. La FDA évalue ces informations pour déterminer si le dispositif répond aux normes réglementaires en matière d'autorisation et de distribution commerciale. En adoptant des solutions de conformité numériques et automatisées comme AmpleLogic, les fabricants peuvent rationaliser la gestion de la documentation, garantir l'intégrité des données et accélérer le cycle de vie des soumissions 510(k), contribuant ainsi à réduire les retards, à améliorer la préparation aux audits et à commercialiser plus rapidement des dispositifs médicaux innovants tout en maintenant la conformité réglementaire.

Numérisation de la planification et de l'ordonnancement des laboratoires : meilleures pratiques et informations
La numérisation de la planification et de l'ordonnancement des laboratoires est essentielle pour les laboratoires de contrôle qualité modernes confrontés à des charges de travail croissantes, à des exigences de tests complexes et à des normes de conformité strictes. Les approches traditionnelles, qui s'appuient souvent sur des feuilles de calcul, des tableaux blancs ou des systèmes de base, ont du mal à gérer la complexité croissante des opérations de laboratoire, où des milliers de tests doivent être coordonnés efficacement. En adoptant des solutions numériques, les laboratoires peuvent améliorer considérablement leur efficacité, réduire les délais d'exécution et optimiser l'utilisation des ressources. Les avantages éprouvés incluent une exécution plus rapide des tests, des besoins en stocks réduits et un meilleur respect des flux de travail de test basés sur les priorités. Les meilleures pratiques clés incluent la mise en œuvre de la modélisation de jumeaux numériques pour la simulation, la priorisation des tests du chemin critique, l'exploitation de l'exécution basée sur les campagnes, l'intégration de la planification des ressources et la possibilité d'une planification adaptative en temps réel. Ces stratégies offrent une meilleure visibilité, minimisent les goulots d'étranglement et améliorent la prise de décision. Avec des plateformes comme AmpleLogic, les organisations peuvent intégrer une planification intelligente, des informations basées sur l'IA et une surveillance en temps réel pour transformer les opérations de laboratoire, en garantissant la conformité, en améliorant la productivité et en établissant une base évolutive pour l'amélioration continue des environnements des sciences de la vie.

Libération automatisée de lots avec le logiciel PQR d'Amplelogic
La libération des lots est l’une des étapes les plus critiques et les plus réglementées de la fabrication pharmaceutique, nécessitant un examen et une approbation approfondis de toutes les données de production et de qualité avant la distribution du produit. Les processus de révision manuels traditionnels sont souvent longs, sujets aux erreurs et difficiles à suivre, ce qui entraîne des retards et des risques de non-conformité. Le logiciel PQR d'AmpleLogic répond à ces défis en introduisant une liste de contrôle automatisée de libération des lots qui standardise et rationalise l'ensemble du processus d'examen. Il intègre les données des enregistrements de fabrication par lots (BMR), des écarts, des CAPA et des systèmes qualité dans un flux de travail structuré et prêt pour l'audit, garantissant l'exhaustivité et la traçabilité à chaque étape. Avec des listes de contrôle configurables basées sur les SOP, des indicateurs de validation automatisés, des signatures numériques et des tableaux de bord en temps réel, la plateforme permet aux équipes d'assurance qualité de détecter les problèmes plus tôt, de réduire les efforts manuels et d'accélérer les approbations par lots. Cela se traduit par une meilleure intégrité des données, une conformité améliorée et une mise sur le marché plus rapide, ce qui rend la libération des lots plus efficace, plus fiable et prête à l'inspection.

11 lettres d'avertissement courantes de la FDA peuvent éviter d'utiliser des solutions numériques
Les lettres d'avertissement de la FDA sont émises lorsque les sociétés pharmaceutiques ne respectent pas les normes réglementaires telles que les bonnes pratiques de fabrication actuelles (CGMP), qui sont essentielles pour garantir la qualité des produits et la sécurité des patients. Ces lettres mettent souvent en évidence des lacunes récurrentes en matière de conformité qui peuvent entraîner des rappels de produits, des perturbations opérationnelles et des atteintes à la réputation si elles ne sont pas traitées de manière proactive. Les problèmes courants identifiés dans les lettres d'avertissement de la FDA comprennent des tests inadéquats sur les matières premières, une mauvaise qualification des fournisseurs, le manque de documentation appropriée et de surveillance de la qualité, une validation insuffisante des processus et du nettoyage, ainsi que des défaillances dans les contrôles de laboratoire et l'intégrité des données. De plus, les carences dans les tests de stabilité, la gestion des enregistrements de lots, la surveillance environnementale et les processus de contrôle des modifications sont fréquemment citées par les régulateurs. Pour relever ces défis, les organisations adoptent de plus en plus de systèmes numériques de gestion de la qualité, de LIMS et de flux de travail automatisés qui garantissent la traçabilité, renforcent la conformité et réduisent les erreurs humaines. En mettant en œuvre des solutions numériques intégrées telles que celles proposées par AmpleLogic, les entreprises peuvent identifier de manière proactive les risques, rationaliser les processus qualité et maintenir une préparation continue aux audits, évitant ainsi les lettres d'avertissement coûteuses de la FDA et garantissant la conformité réglementaire à long terme.

Logiciel LIMS pour les laboratoires d'aliments et de boissons
Les laboratoires du secteur agroalimentaire jouent un rôle essentiel en garantissant la sécurité, la qualité et la conformité réglementaire des produits tout au long du cycle de vie de la production. Des tests de matières premières à la validation des produits finis, ces laboratoires doivent gérer des flux de travail complexes, de gros volumes de données et des normes strictes de sécurité alimentaire. Le logiciel LIMS pour les laboratoires d'aliments et de boissons fournit une plate-forme centralisée pour rationaliser le suivi des échantillons, automatiser la capture des données et garantir la conformité aux réglementations mondiales telles que ISO 17025, HACCP et les normes de sécurité alimentaire. Il permet une traçabilité de bout en bout, depuis l'approvisionnement des ingrédients jusqu'à la sortie du produit final, tout en réduisant les erreurs manuelles et en améliorant l'intégrité des données. Grâce à des fonctionnalités avancées telles que la traçabilité des lots et des lots, l'intégration d'instruments, des flux de travail automatisés et des rapports en temps réel, les solutions LIMS modernes permettent aux laboratoires d'améliorer leur efficacité opérationnelle, d'accélérer les cycles de test et de maintenir leur préparation aux audits. En adoptant des plateformes comme AmpleLogic, les organisations peuvent transformer les processus de gestion de la qualité des aliments et garantir des résultats de produits cohérents, conformes et de haute qualité.

QMS sur papier vs QMS numérique AmpleLogic : lequel est le meilleur ?
Alors que les organisations pharmaceutiques et des sciences de la vie sont confrontées à une pression réglementaire croissante et à une complexité opérationnelle croissante, le débat entre le QMS papier et le QMS numérique est devenu plus pertinent que jamais. Les systèmes papier traditionnels, autrefois la norme, sont désormais confrontés à des inefficacités telles que la documentation manuelle, la lenteur des approbations et la difficulté à maintenir la préparation aux audits. Le système de gestion de la qualité sur papier entraîne souvent des risques tels que des documents égarés, des problèmes de contrôle de version et une visibilité limitée sur les processus qualité, ce qui rend la gestion de la conformité plus difficile dans des environnements hautement réglementés. En revanche, un QMS numérique (eQMS) centralise tous les processus qualité, automatise les flux de travail et garantit un accès en temps réel à des données précises et traçables. Les solutions QMS numériques offrent des avantages significatifs, notamment un contrôle automatisé des documents, des pistes d'audit sécurisées, des signatures électroniques et des tableaux de bord de reporting en temps réel. Ces fonctionnalités améliorent l'intégrité des données, réduisent les erreurs humaines et améliorent l'efficacité opérationnelle globale tout en garantissant la conformité aux réglementations telles que les normes FDA 21 CFR Part 11 et GMP. Avec des plateformes comme AmpleLogic, les organisations peuvent passer d'une gestion réactive et manuelle de la qualité à une approche proactive basée sur les données, permettant une prise de décision plus rapide, une conformité améliorée et des opérations de qualité évolutives. À l’ère numérique d’aujourd’hui, un système de gestion de la qualité moderne n’est pas seulement une mise à niveau mais une nécessité stratégique pour maintenir la compétitivité et l’excellence réglementaire.

Système de gestion des documents de conformité pour les sciences de la vie
La gestion de la documentation dans le secteur des sciences de la vie est complexe en raison d'exigences réglementaires strictes, de volumes de données élevés et de la nécessité d'une traçabilité complète. Un système de gestion des documents de conformité (DMS) aide les organisations à numériser, contrôler et normaliser les processus documentaires tout en garantissant le respect des réglementations mondiales telles que la FDA 21 CFR Part 11, l'Annexe 11 de l'UE et les directives GxP. Les systèmes traditionnels sur papier ou fragmentés entraînent souvent des inefficacités, des problèmes de contrôle de version et des risques de conformité. En revanche, un système de gestion électronique de documents moderne offre un contrôle centralisé sur les cycles de vie des documents (de la création et de la révision à l'approbation, la publication et l'archivage), garantissant l'exactitude, la cohérence et la préparation à l'audit. Avec des fonctionnalités avancées telles que les signatures électroniques, les pistes d'audit, les flux de travail automatisés et la recherche basée sur l'IA, des plates-formes comme AmpleLogic permettent aux organisations des sciences de la vie d'améliorer l'intégrité des données, d'améliorer la collaboration et de réduire les efforts manuels. En numérisant les processus de contrôle des documents, les entreprises peuvent obtenir des approbations plus rapides, une meilleure visibilité sur la conformité et une base évolutive pour l'excellence réglementaire dans des environnements hautement réglementés.

Stratégies de réduction des coûts informatiques pharmaceutiques qui permettent d'économiser 70 %
Les sociétés pharmaceutiques sont confrontées à une pression croissante pour réduire leurs coûts informatiques tout en maintenant la conformité, l'innovation et l'efficacité opérationnelle. L'augmentation des dépenses d'infrastructure, les systèmes existants et les exigences réglementaires complexes font de l'informatique l'un des centres de coûts les plus importants du secteur. La réduction stratégique des coûts informatiques se concentre sur l’optimisation (et non seulement sur la réduction) des dépenses en améliorant l’efficacité du système, en éliminant les redondances et en tirant parti des technologies modernes. Par exemple, la consolidation de l'infrastructure informatique, la rationalisation des applications et l'externalisation des services de support peuvent réduire considérablement les frais généraux d'exploitation. Des études montrent que la rationalisation des systèmes informatiques et de la gestion des fournisseurs peut à elle seule réduire les coûts informatiques totaux d'environ 30 % sur une courte période. Les stratégies clés incluent l'adoption de plates-formes basées sur le cloud, l'automatisation des processus manuels, l'intégration de systèmes de qualité et de conformité et la réduction de la dépendance à l'égard de plusieurs outils déconnectés. De plus, l'externalisation de fonctions spécialisées et l'amélioration de l'utilisation des ressources peuvent générer des gains d'efficacité substantiels, certaines organisations réalisant des économies considérables grâce à ces approches combinées. Avec des plateformes comme AmpleLogic, les sociétés pharmaceutiques peuvent unifier leurs systèmes, automatiser les flux de travail et améliorer la visibilité des données, permettant ainsi une prise de décision plus intelligente et une transformation numérique évolutive. En mettant en œuvre la bonne combinaison d'automatisation, de consolidation et d'optimisation des processus, les organisations peuvent réduire considérablement leurs coûts informatiques tout en améliorant la conformité, l'agilité et les performances globales de l'entreprise.

7 défis liés à la conduite de l'APQR et comment les surmonter
La réalisation d’un examen annuel de la qualité des produits (APQR) efficace est essentielle pour garantir une qualité constante des produits et la conformité réglementaire dans l’industrie pharmaceutique. Cependant, les organisations sont souvent confrontées à de multiples défis qui rendent le processus complexe, long et sujet aux erreurs. L'un des principaux défis réside dans la fragmentation des données réparties sur des systèmes tels que LIMS, QMS, ERP et feuilles de calcul, ce qui rend l'agrégation des données difficile et sujette aux erreurs. De plus, la gestion manuelle des données entraîne des incohérences, des duplications et des problèmes d'intégrité des données, qui peuvent compromettre l'exactitude des rapports APQR. D'autres défis courants incluent la pression de conformité réglementaire, les capacités analytiques limitées pour l'analyse des tendances, la collaboration interfonctionnelle inefficace et le manque de traçabilité lors des audits. Ces problèmes entraînent souvent des retards, une augmentation des efforts manuels et une efficacité réduite du processus de révision. Pour surmonter ces défis, les sociétés pharmaceutiques adoptent des solutions numériques qui intègrent des sources de données, automatisent les flux de travail et fournissent des analyses en temps réel. La mise en œuvre de SOP standardisées, l'amélioration de la gouvernance des données, la collaboration entre les départements et l'exploitation du logiciel APQR avancé peuvent améliorer considérablement l'efficacité, garantir la conformité et transformer l'APQR en un processus qualité proactif et axé sur les données.

Logiciel en tant que dispositif médical (SaMD) : exigences relatives aux fichiers techniques
Le logiciel en tant que dispositif médical (SaMD) fait référence à un logiciel destiné à exécuter des fonctions médicales, telles que le diagnostic, le traitement ou la surveillance, sans faire partie d'un dispositif médical physique. Selon les organismes de réglementation mondiaux tels que l'International Medical Device Regulators Forum (IMDRF) et la FDA, SaMD fonctionne sur des plates-formes à usage général telles que des ordinateurs, des appareils mobiles ou des environnements cloud, tout en fournissant des résultats cliniquement pertinents. Les solutions SaMD sont largement utilisées dans le secteur des soins de santé, depuis l'analyse d'imagerie diagnostique et les systèmes d'aide à la décision clinique jusqu'aux applications de santé mobiles qui surveillent l'état des patients. Ces systèmes doivent se conformer à des exigences réglementaires strictes, notamment des normes de classification des risques, de validation, de cybersécurité et d'intégrité des données, pour garantir la sécurité et l'efficacité des patients. Avec la croissance rapide de la santé numérique et des technologies basées sur l'IA, SaMD transforme la manière dont les soins de santé sont dispensés en permettant un diagnostic plus rapide, un traitement personnalisé et une surveillance en temps réel. Cependant, cela introduit également des défis liés à la conformité, à l’assurance qualité et à la gestion du cycle de vie. Des plateformes comme AmpleLogic aident les organisations à rationaliser la validation, à garantir la conformité réglementaire et à gérer le cycle de vie complet des logiciels de dispositifs médicaux, permettant ainsi une innovation plus rapide tout en maintenant les normes de sécurité et de conformité.

Systèmes de gestion de la qualité (QMS) pour les dispositifs médicaux
Un système de gestion de la qualité (QMS) pour les dispositifs médicaux est un cadre structuré de processus, de procédures et de responsabilités conçu pour garantir la qualité, la sécurité et la conformité réglementaire des produits tout au long de leur cycle de vie, de la conception et du développement à la fabrication et à la surveillance après commercialisation. Les fabricants de dispositifs médicaux doivent se conformer à des réglementations mondiales strictes telles que la norme ISO 13485, le MDR de l’UE et la réglementation du système de gestion de la qualité (QMSR) de la FDA, qui s’aligne sur les normes internationales pour garantir une qualité constante des produits et la sécurité des patients. Un système de gestion de la qualité robuste intègre des éléments critiques tels que les contrôles de conception, la gestion des risques, la gestion de la qualité des fournisseurs, les CAPA (actions correctives et préventives), la gestion de la formation et les processus d'audit. Ces composants aident les organisations à maintenir la traçabilité, à minimiser les risques et à garantir une amélioration continue de l'ensemble des opérations. En adoptant des solutions QMS numériques comme AmpleLogic, les entreprises de dispositifs médicaux peuvent rationaliser les processus qualité, automatiser les flux de travail de conformité et améliorer l'intégrité des données. Cela permet des approbations réglementaires plus rapides, une meilleure préparation aux audits et une livraison cohérente de dispositifs médicaux sûrs et de haute qualité dans un secteur hautement réglementé.

QMS dans l'industrie pharmaceutique : comment l'IA transforme la gestion de la qualité
L'intelligence artificielle transforme rapidement les systèmes de gestion de la qualité (QMS) dans l'industrie pharmaceutique et des sciences de la vie en s'attaquant aux inefficacités des processus manuels traditionnels. Les systèmes de gestion de la qualité conventionnels sont souvent confrontés à des données fragmentées, à des enquêtes retardées et à une visibilité limitée sur les événements liés à la qualité, ce qui a un impact sur la conformité et l'efficacité opérationnelle. En intégrant l'IA dans QMS, les organisations peuvent automatiser les processus qualité critiques tels que CAPA, la gestion des écarts, le contrôle des modifications et la gestion des audits. Les systèmes basés sur l'IA exploitent l'apprentissage automatique et l'analyse prédictive pour identifier les tendances, détecter les anomalies et recommander des actions correctives, permettant ainsi une analyse plus rapide des causes profondes et une atténuation proactive des risques. Le système de gestion de la qualité basé sur l'IA améliore également la prise de décision en fournissant des informations en temps réel, en améliorant la précision des données et en réduisant les interventions manuelles. Des fonctionnalités telles que la détection prédictive OOS/OOT, le traitement automatisé des réclamations et l’évaluation intelligente des risques aident les organisations à améliorer la qualité des produits, à garantir la conformité réglementaire et à réduire les coûts opérationnels. Avec des plateformes comme AmpleLogic, les sociétés pharmaceutiques peuvent adopter un écosystème de qualité entièrement intégré et alimenté par l'IA, rationalisant les flux de travail, accélérant les approbations et réalisant des gains d'efficacité significatifs tout en maintenant une stricte conformité aux réglementations mondiales.

Contrôle des documents relatifs aux dispositifs médicaux : ce que vous devez savoir
Le contrôle des documents relatifs aux dispositifs médicaux est un élément essentiel de la qualité et de la conformité réglementaire, garantissant que tous les documents liés à la conception, à la fabrication et à la gestion de la qualité sont correctement créés, examinés, approuvés et conservés tout au long de leur cycle de vie. Il joue un rôle essentiel dans le maintien de la sécurité des produits, de la traçabilité et de la préparation aux audits dans des environnements hautement réglementés. Les cadres réglementaires tels que FDA 21 CFR Part 820, ISO 13485 et EU MDR exigent que les organisations établissent des procédures formelles pour l'approbation des documents, le contrôle des versions, la distribution et la gestion des modifications. Ces réglementations garantissent que seuls les documents à jour et approuvés sont utilisés et que toutes les modifications sont suivies et validées pour maintenir l'intégrité des données. Un système robuste de contrôle des documents permet aux organisations de gérer les enregistrements critiques tels que les Device Master Records (DMR), les Device History Records (DHR) et les procédures qualité avec une traçabilité complète. En adoptant des solutions numériques comme AmpleLogic, les entreprises peuvent automatiser les flux de travail documentaires, assurer la conformité, maintenir des pistes d'audit sécurisées et améliorer l'efficacité opérationnelle, garantissant ainsi la préparation aux inspections réglementaires et l'excellence de la qualité à long terme.

KPI de qualité dans la fabrication pour la gestion de la qualité pharmaceutique
Les indicateurs clés de performance (KPI) de qualité sont des mesures essentielles utilisées pour évaluer l'efficacité des systèmes de gestion de la qualité (QMS) dans la fabrication pharmaceutique. Ces KPI fournissent des informations mesurables sur la qualité des produits, l'efficacité des processus et la conformité réglementaire, aidant ainsi les organisations à prendre des décisions basées sur les données et à garantir une amélioration continue. Dans la fabrication pharmaceutique, les KPI couramment suivis incluent le taux de rejet de lots, le taux d’écart, l’efficacité CAPA, les incidents hors spécifications (OOS) et le temps de cycle des enquêtes. Ces indicateurs aident à identifier les inefficacités des processus, à détecter rapidement les problèmes de qualité et à garantir des actions correctives en temps opportun. La surveillance de ces KPI est essentielle pour maintenir la conformité aux normes BPF et garantir une qualité constante des produits. De plus, des mesures telles que Right First Time (RFT), le taux de défauts et la durée du cycle de processus fournissent des informations sur les performances de fabrication et l'efficacité opérationnelle. En analysant ces KPI, les organisations peuvent réduire les retouches, minimiser les coûts et améliorer les résultats globaux de production. Avec des plateformes numériques comme AmpleLogic, les sociétés pharmaceutiques peuvent automatiser le suivi des KPI, générer des tableaux de bord en temps réel et obtenir des informations prédictives, transformant ainsi la gestion de la qualité en une fonction proactive basée sur les données qui améliore la conformité, l'efficacité et la fiabilité des produits.

Un pic dans les études de stabilité et l'analyse de régression pour la fiabilité des produits pharmaceutiques
Les études de stabilité sont un élément essentiel du développement pharmaceutique, garantissant que les produits pharmaceutiques conservent leur identité, leur force, leur qualité et leur pureté tout au long de leur durée de conservation dans des conditions environnementales définies. Ces études aident à établir les dates d'expiration, les exigences de stockage et la conformité réglementaire conformément aux directives de l'ICH. L'analyse de régression joue un rôle essentiel dans l'interprétation des données de stabilité en modélisant les modèles de dégradation et en prédisant la durée de conservation des produits. En analysant les tendances influencées par des facteurs tels que la température, l'humidité et l'exposition à la lumière, les techniques de régression permettent une estimation précise des dates de péremption et soutiennent la prise de décision fondée sur les données dans la gestion de la qualité pharmaceutique. Les méthodes statistiques avancées telles que l'ANOVA et l'ANCOVA améliorent encore l'analyse de stabilité en identifiant les variations significatives selon les conditions et en ajustant les variables externes. Ces approches améliorent la précision et la fiabilité des prévisions de stabilité, garantissant ainsi des performances produit cohérentes et une conformité réglementaire. En tirant parti de solutions numériques telles que le logiciel de gestion des études de stabilité d'AmpleLogic, les organisations peuvent automatiser les flux de travail, surveiller les tendances en temps réel et appliquer des modèles statistiques intelligents, transformant ainsi les tests de stabilité en un processus plus efficace, plus précis et plus conforme qui garantit la fiabilité des produits pharmaceutiques à long terme.

Simplifier la gestion des écarts grâce à l'IA : améliorer votre logiciel existant
La gestion des écarts est un élément essentiel des systèmes qualité pharmaceutique, garantissant que toute non-conformité est correctement identifiée, étudiée et résolue conformément aux normes réglementaires. Cependant, les approches traditionnelles sont souvent lentes, manuelles et gourmandes en ressources, ce qui entraîne des retards dans les enquêtes et une augmentation des risques de non-conformité. L'intelligence artificielle transforme la gestion des écarts en automatisant des étapes clés telles que la collecte de données, l'analyse des causes profondes et les recommandations CAPA. Les systèmes basés sur l'IA analysent les écarts historiques, identifient les modèles dans les processus et les équipements et fournissent des informations basées sur les données qui aident les équipes qualité à prendre des décisions plus rapides et plus précises. Avec des solutions basées sur l'IA telles que le QMS d'AmpleLogic, les organisations peuvent réduire considérablement les délais d'enquête, améliorer l'efficacité du CAPA et minimiser la récurrence des écarts. Ces systèmes améliorent la traçabilité, garantissent la préparation aux audits et permettent une gestion proactive de la qualité, passant d'une gestion réactive des problèmes à une conformité prédictive et basée sur l'intelligence.

Rôle du logiciel de stabilité pour garantir la conformité et la qualité du développement pharmaceutique
Les logiciels de stabilité jouent un rôle crucial pour garantir la conformité et maintenir la qualité des produits tout au long du cycle de vie du développement pharmaceutique. Les études de stabilité sont essentielles pour déterminer comment les produits pharmaceutiques conservent leur identité, leur force, leur qualité et leur pureté dans diverses conditions environnementales, ce qui en fait la pierre angulaire de l'approbation réglementaire et de la gestion du cycle de vie. Un logiciel moderne de gestion de la stabilité permet aux organisations de concevoir, d'exécuter et de surveiller efficacement des études de stabilité conformes à l'ICH. Ces systèmes automatisent les processus critiques tels que la gestion des protocoles, la planification des prélèvements d'échantillons, la surveillance environnementale et l'analyse statistique des tendances, garantissant ainsi une prévision précise de la durée de conservation et des soumissions réglementaires solides. En numérisant les flux de travail de stabilité, les sociétés pharmaceutiques peuvent éliminer le suivi manuel, améliorer l'intégrité des données et maintenir des pistes d'audit complètes conformes aux exigences FDA 21 CFR Part 11 et GxP. Les plates-formes avancées s'intègrent également aux systèmes LIMS et QMS, offrant une visibilité en temps réel sur la progression de l'étude et permettant une prise de décision proactive. Avec des solutions comme AmpleLogic, les organisations peuvent rationaliser la gestion des études de stabilité, améliorer la conformité et garantir une qualité de produit constante, accélérant ainsi les délais de développement et améliorant l'efficacité opérationnelle globale dans un environnement hautement réglementé.

Industries réglementées : choisir une plateforme intégrée pour les transformations numériques

LIMS pour les laboratoires de petite et moyenne taille Solutions pour les laboratoires en croissance

Logiciel de planification et de planification QC pour optimiser les opérations pharmaceutiques

Naviguez dans l’évolution des réglementations en matière de contrôle qualité dans le secteur pharmaceutique

Personnalisation du système LIMS pour le flux de travail unique de votre laboratoire

L'avenir des données dans les sciences de la vie : pourquoi le LIMS est-il essentiel ?

Pourquoi le système LIMS basé sur le cloud est la solution ultime pour les laboratoires modernes ?

Système de recommandation basé sur l'IA pour le contrôle des changements dans l'industrie pharmaceutique

Simplifier les audits et les rapports des données de laboratoire avec LIMS

10 signes indiquant que votre laboratoire a besoin d'une mise à niveau du système LIMS

Pourquoi le logiciel QMS basé sur le cloud est crucial pour les sociétés pharmaceutiques européennes

Bharat Biotech transforme la gestion de la qualité avec AmpleLogic eQMS

Parcours de Laurus Labs avec AmpleLogic

Elite Pharmaceuticals choisit le logiciel de stabilité AmpleLogic

10 changements clés dans la deuxième édition de GAMP 5 : un aperçu complet

Comment LIMS peut révolutionner les opérations de laboratoire et la gestion des données

Le voyage d'AmpleLogic au Moyen-Orient !

AmpleLogic s'associe à PSI Saudi

Améliorer la qualité pharmaceutique avec les solutions SaaS PQR

AmpleLogic a célébré son 15e anniversaire

Transition de P&G vers des journaux de bord automatisés avec la plateforme AmpleLogic

Sun Pharma augmente son efficacité opérationnelle globale de 40 %

Qu’est-ce que l’examen annuel de la qualité des produits (APQR) dans le secteur pharmaceutique ?
L'examen annuel de la qualité des produits (APQR) dans le secteur pharmaceutique est une exigence BPF qui évalue la qualité des produits, la cohérence de la fabrication, les écarts et la conformité au fil du temps pour garantir une amélioration continue et le respect de la réglementation.

Principaux défis liés à l'examen de la qualité des produits (APQR) dans le secteur pharmaceutique
Les principaux défis liés à l'examen de la qualité des produits (APQR) dans le secteur pharmaceutique comprennent les problèmes d'intégration des données, la documentation incohérente, la gestion des écarts, les lacunes en matière de conformité réglementaire et l'analyse limitée des tendances, ce qui a un impact sur la qualité, l'efficacité et l'amélioration continue.

APQR manuel ou automatisé : ce que les dirigeants pharmaceutiques doivent savoir
Les APQR manuels et automatisés dans le secteur pharmaceutique explorent les principales différences en termes d'efficacité, d'exactitude des données, de conformité et d'évolutivité pour aider les dirigeants pharmaceutiques à choisir la bonne approche pour l'examen de la qualité et l'amélioration continue.

Gartner reconnaît Amplelogic dans son guide du marché pour les systèmes de gestion de l'information de laboratoire
L'inclusion d'AmpleLogic dans le guide du marché Gartner pour les systèmes de gestion de l'information de laboratoire (LIMS) souligne son influence croissante dans le domaine technologique des sciences de la vie. Grâce à sa plateforme low-code basée sur l'IA, AmpleLogic permet aux laboratoires de rationaliser les flux de travail, d'améliorer l'intégrité des données et d'accélérer les initiatives de transformation numérique. Cette reconnaissance reflète l’engagement de l’entreprise à fournir des solutions innovantes, conformes et évolutives aux laboratoires modernes.

Comment automatiser la libération par lots dans APQR ?
L'automatisation de la libération des lots au sein du processus APQR transforme la façon dont les sociétés pharmaceutiques gèrent la qualité et la conformité. Traditionnellement, la libération des lots implique un examen manuel approfondi des enregistrements de fabrication et de qualité pour garantir qu'un produit est apte à la distribution. L'examen annuel de la qualité des produits (APQR) consolide les données de tous les lots sur une année pour identifier les tendances et garantir une qualité constante des produits. En intégrant l'automatisation dans APQR, les organisations peuvent numériser les flux de travail de révision par lots, mettre en œuvre des validations basées sur des listes de contrôle et permettre le suivi en temps réel des écarts, des CAPA et des mesures de qualité. Cela améliore non seulement l’intégrité des données et la préparation aux audits, mais réduit également considérablement les temps de cycle de publication. Avec des plateformes comme AmpleLogic, les sociétés pharmaceutiques peuvent passer de contrôles de qualité réactifs à des décisions de libération de lots proactives et basées sur les données, garantissant des approbations plus rapides sans compromettre la conformité.

LIMS pour les fabricants : améliorer la qualité et la traçabilité des produits

Les 5 principaux défis de conformité auxquels sont confrontés les laboratoires et comment LIMS peut les aider

6 stratégies éprouvées pour combler les lacunes en matière de conformité dans le secteur pharmaceutique

Comment automatiser la conformité de la fabrication : rationaliser les processus pour une plus grande efficacité

Des molécules aux métadonnées : guide sur la confidentialité et la sécurité des données dans l'industrie pharmaceutique

Comment mettre en œuvre avec succès le LIMS et améliorer l'efficacité du laboratoire

Le rôle d'AmpleLogic dans les tendances futures des systèmes de gestion de la qualité (QMS)

Comment les données APQR peuvent-elles être utilisées pour la vérification continue des processus ?

Comment se déroule la validation du nettoyage dans les sciences de la vie : un guide étape par étape

Pourquoi optimiser la validation du nettoyage pour la conformité et l'efficacité

Comment le CPV améliore-t-il le flux de données dans le secteur manufacturier ?

À quoi s’attendre lors d’un audit ISO 9001 ?

Procédure hors spécifications pour la fabrication de dispositifs médicaux

Enquête sur les résultats OOS dans les tests analytiques
Un guide complet pour enquêter sur les résultats hors spécifications (OOS) dans les tests analytiques. Apprenez les flux de travail structurés, l'analyse des causes profondes et les approches conformes à la réglementation à l'aide de l'eQMS d'AmpleLogic pour garantir l'intégrité des données, l'assurance qualité et la gestion efficace des CAPA dans les secteurs réglementés.

Cycle de vie du système QMS pour maîtriser la qualité et la conformité dans l'industrie pharmaceutique
Découvrez comment l'eQMS d'AmpleLogic simplifie le cycle de vie d'un système de gestion de la qualité dans l'industrie pharmaceutique. Du déploiement à l’amélioration continue, obtenez une conformité transparente, améliorez la qualité des produits et numérisez les processus qualité critiques avec une plateforme avancée et évolutive.

6 outils numériques qui réduisent les erreurs humaines dans les sciences de la vie
Les erreurs humaines dans les sciences de la vie peuvent entraîner des risques de non-conformité et des écarts coûteux. Explorez six outils numériques essentiels qui rationalisent les flux de travail, automatisent la capture des données et garantissent l'exactitude des opérations pharmaceutiques et biotechnologiques.

Comment l’erreur humaine alimente les risques de cybersécurité dans les sciences de la vie
L’erreur humaine reste l’une des principales causes de failles de cybersécurité, représentant jusqu’à 95 % des incidents dans tous les secteurs. Dans les sciences de la vie, même des erreurs mineures peuvent compromettre les données sensibles, perturber la conformité et avoir un impact sur la sécurité des patients, ce qui rend indispensables des systèmes numériques robustes.

Cipla transforme l'accès des utilisateurs avec AmpleLogic UMS dans le secteur pharmaceutique
Découvrez comment Cipla a rationalisé la gestion des accès des utilisateurs dans ses opérations pharmaceutiques à l'aide de la solution UAM avancée d'AmpleLogic. Cette étude de cas met en évidence une conformité améliorée, un provisionnement automatisé des utilisateurs et un contrôle d'accès sécurisé et prêt pour l'audit, aligné sur les exigences GxP.

Exigences réglementaires pour le calcul MACO et la validation du nettoyage
Comprendre les exigences réglementaires pour le calcul MACO et la validation du nettoyage dans la fabrication pharmaceutique. Ce guide explique comment les agences mondiales telles que la FDA, l'EMA, le CDSCO et l'OMS attendent des limites de résidus scientifiquement justifiées et basées sur les risques, utilisant la PDE et des approches basées sur la dose pour garantir la conformité, la sécurité des patients et la préparation aux audits.

Réduire les erreurs humaines dans la fabrication pharmaceutique grâce à une solution numérique
L’erreur humaine reste l’une des principales causes de problèmes de conformité dans la fabrication pharmaceutique. En adoptant des solutions numériques telles que eBMR, QMS et LIMS, les organisations peuvent éliminer les inefficacités manuelles, améliorer la précision des données et garantir la conformité réglementaire grâce à l'automatisation, à la surveillance en temps réel et aux flux de travail standardisés.

L'avantage numérique de Teva avec AmpleLogic
Découvrez comment Teva a exploité l'eQMS d'AmpleLogic pour numériser les processus qualité, améliorer la conformité et réduire les charges de travail manuelles. Cette étude de cas montre comment une plate-forme numérique unifiée a permis des opérations plus rapides, une meilleure préparation aux audits et une gestion de la qualité évolutive dans l'industrie pharmaceutique.

Votre logiciel d’application est-il obsolète ou simplement sécurisé ?
Les logiciels d'application obsolètes peuvent exposer les organisations à des risques de sécurité importants, à des manquements à la conformité et à des inefficacités opérationnelles. Cet article explore l’impact des systèmes existants sur les secteurs réglementés comme le secteur pharmaceutique et pourquoi la mise à niveau vers des solutions numériques modernes et sécurisées est essentielle. Découvrez comment AmpleLogic aide les entreprises à rester conformes, sécurisées et prêtes pour l'avenir.

Système de gestion de l'apprentissage pour l'industrie cosmétique
Le LMS d'AmpleLogic pour l'industrie cosmétique rationalise la formation, garantit la conformité réglementaire et améliore les compétences de la main-d'œuvre. Grâce à l'automatisation basée sur l'IA, à la gestion des SOP et aux fonctionnalités compatibles GMP, il permet aux entreprises de cosmétiques de maintenir la qualité, la sécurité et la préparation aux audits dans un environnement hautement réglementé.

Processus de validation des logiciels FDA : étapes, principes et plus
Le processus de validation des logiciels de la FDA est essentiel pour garantir que les systèmes informatisés du secteur pharmaceutique fonctionnent systématiquement comme prévu tout en répondant aux exigences réglementaires. Ce blog explique les étapes du cycle de vie de validation, la documentation, les approches basées sur les risques et la manière dont les outils numériques contribuent à assurer la conformité, l'intégrité des données et la préparation à l'audit.

Transformez les laboratoires de contrôle qualité avec un logiciel avancé de planification et d'ordonnancement
Le logiciel de planification et de planification QC d'AmpleLogic permet aux laboratoires pharmaceutiques de bénéficier d'une planification intelligente, d'une planification automatisée et d'une exécution basée sur des campagnes. Il améliore l'utilisation des ressources, réduit les délais d'exécution et garantit la conformité grâce à une visibilité en temps réel et des flux de travail de laboratoire optimisés.

Obtenez votre liste de contrôle du journal de bord électronique : un outil pratique pour les équipes d'assurance qualité, de contrôle qualité et de production
Une liste de contrôle pratique du journal de bord électronique aide les équipes d'assurance qualité, de contrôle qualité et de production à normaliser la documentation, à réduire les erreurs humaines et à maintenir la conformité aux BPF. En numérisant les journaux de bord, les sociétés pharmaceutiques peuvent améliorer l'intégrité des données, garantir la préparation aux audits et rationaliser les flux de travail opérationnels quotidiens.

Transformation numérique de la gestion de la qualité chez OCuSOFT avec EQMS
Découvrez comment OCuSOFT a exploité l'eQMS d'AmpleLogic pour numériser les processus qualité de bout en bout, réduisant ainsi les enregistrements papier de 85 % tout en améliorant la visibilité, la conformité et la préparation aux audits. La solution a rationalisé les flux de contrôle des documents, de CAPA et d'audit dans un environnement réglementé.

Comment répondre efficacement aux normes FDA 483 et éviter les erreurs courantes
Répondre aux observations FDA 483 nécessite une approche opportune, structurée et fondée sur des preuves. Les organisations doivent traiter chaque observation avec une analyse des causes profondes, des actions correctives et préventives (CAPA) et des délais clairs pour éviter les lettres d'avertissement et renforcer la conformité.

Que se passe-t-il lorsque l’assurance qualité n’est pas impliquée dans les changements d’installations
L'exclusion de l'assurance qualité des modifications apportées aux installations peut entraîner des lacunes en matière de conformité, des échecs de validation et un risque réglementaire accru. L'assurance qualité joue un rôle essentiel dans l'évaluation de l'impact, la garantie d'une documentation appropriée et le maintien des normes BPF grâce à des processus structurés de contrôle des changements et de gestion des risques.

Comprendre les procédures de délivrance de lots pharmaceutiques
Les procédures de délivrance des lots pharmaceutiques sont essentielles pour garantir la conformité, la traçabilité et la qualité des produits BPF. De l'émission de dossiers de fabrication par lots (BMR) à la vérification des matières premières et à la documentation de chaque étape, ces processus fournissent une piste d'audit complète pour chaque lot et prennent en charge les inspections réglementaires.

Enregistrements de lots incomplets : un risque caché dans chaque audit de la FDA
Les enregistrements de lots incomplets sont un signal d’alarme majeur lors des audits de la FDA, conduisant souvent à 483 observations et lettres d’avertissement. Les signatures manquantes, les entrées peu claires et les lacunes dans les données soulèvent des inquiétudes quant à la qualité des produits, à la traçabilité et à l'intégrité des données, ce qui rend des pratiques de documentation solides essentielles à la conformité.

80 % du journal de bord manuel actuel de 2000 est géré avec seulement 60 à 65 journaux

Validation de nouvelle génération : adopter la validation continue des processus pour une fabrication pharmaceutique agile et adaptative

Maximisez l’efficacité et la visibilité avec le tableau de bord graphique APQR

Rationalisation de la validation du nettoyage dans la fabrication pharmaceutique avec les systèmes MES

Guide ultime sur le journal de bord électronique pour la fabrication pharmaceutique

Contrôle statistique des processus et APQR : améliorer l'assurance qualité pharmaceutique

Meilleures pratiques pour la mise en œuvre de la planification et de l'ordonnancement du contrôle qualité dans le secteur pharmaceutique

Un guide sur la validation des systèmes informatiques (CSV) dans le secteur pharmaceutique

Comment les systèmes de planification et de planification du contrôle qualité améliorent l'efficacité du laboratoire

Le rôle de la vérification continue des processus dans la validation des processus

Comment la validation des processus garantit une qualité constante des produits pharmaceutiques

Un guide étape par étape pour la validation des processus en pharmacie

Comment automatiser les processus de validation du nettoyage dans l'industrie pharmaceutique

13 façons de dynamiser votre laboratoire avec le logiciel LIMS

Libérer l’efficacité des laboratoires grâce à des systèmes LIMS validés

ADC Therapeutics améliore la gestion standard avec le module AmpleLogic
Découvrez comment ADC Therapeutics a numérisé la gestion des normes avec AmpleLogic pour améliorer la conformité, réduire les efforts manuels et améliorer la visibilité et l'efficacité des données.

Échecs de l’intégrité des données MHRA et comment les éviter
Découvrez les défaillances courantes de l’intégrité des données de la MHRA dans le secteur pharmaceutique et comment les éviter. Améliorez la conformité, respectez les principes ALCOA+ et restez prêt pour les audits grâce aux meilleures pratiques.

En quoi le LIMS stérile est-il différent du LIMS OSD ?
Découvrez en quoi le LIMS stérile diffère du LIMS OSD dans le secteur pharmaceutique. Comparez les flux de travail, les besoins de conformité et la gestion des données pour choisir la bonne solution.

Erreur humaine et intégrité des données dans le secteur pharmaceutique | Guide de conformité FDA
Comprenez l’impact de l’erreur humaine sur l’intégrité des données dans le secteur pharmaceutique. Découvrez les exigences de conformité de la FDA, les principes ALCOA+ et les stratégies éprouvées pour éviter les échecs d'audit.

Enquête sur les résultats OOS dans les tests analytiques
Découvrez comment étudier les résultats OOS (hors spécifications) dans les tests analytiques. Comprendre l'analyse des causes profondes, les directives de la FDA et les stratégies CAPA pour la conformité pharmaceutique.

Industrie 4.0 : fabrication numérique dans l'industrie pharmaceutique

Approches basées sur les risques pour l'élaboration de SOP pour l'examen annuel de la qualité des produits (APQR) : garantir l'accent mis sur les attributs de qualité critiques

Décoder le Pharma MES : Explorer les systèmes d'exécution de la fabrication pour la fabrication pharmaceutique

Tirer parti d'un logiciel de surveillance de la qualité des produits pour améliorer l'APQR dans la fabrication pharmaceutique

Améliorer l'examen de la qualité des produits grâce à la gestion automatisée des excursions dans la fabrication pharmaceutique

Surveillance en temps réel : mise en œuvre de limites de contrôle dynamiques pour une amélioration continue des processus dans le secteur pharmaceutique

Résoudre les écarts dans les enregistrements de lots avec les systèmes MES : garantir l'exactitude et la conformité

Problèmes de stabilité de la production pharmaceutique : tirer parti du MES pour la surveillance et la correction en temps réel

Comprendre les exigences du journal de bord GMP

Naviguer dans l'intégration de l'IA et du ML dans le logiciel Pharma MES

Comprendre l'importance du journal de bord séquentiel des équipements dans les sciences de la vie

Comprendre l'examen annuel de la qualité des produits et libérer l'excellence des processus métier avec le logiciel AmpleLogic APQR

Innovations de pointe en matière d'amélioration continue de la qualité pour l'industrie des sciences de la vie

Dans le secteur des sciences de la vie, la précision est nécessaire pour maintenir les normes de qualité les plus élevées et pour se conformer aux réglementations. L'amélioration continue de la qualité (AQI) constitue la pierre angulaire de l'excellence dans la fabrication des sciences de la vie, incarnant une philosophie de raffinement et d'optimisation incessants dans toutes les facettes de la production. Cet article se penche sur l'avant-garde de l'innovation qui stimule l'ACQ dans le secteur des sciences de la vie, en présentant des technologies et des méthodologies révolutionnaires prêtes à révolutionner la gestion de la qualité, l'efficacité opérationnelle et la conformité réglementaire. Évolution de l'amélioration continue de la qualité dans les sciences de la vie L'évolution de l'ACQ dans le secteur des sciences de la vie a été marquée par le passage des approches traditionnelles de gestion de la qualité aux méthodologies de pointe basées sur les données. Initialement ancré dans les principes de gestion de la qualité totale (TQM), CQI a subi un changement de paradigme vers un modèle plus proactif et axé sur la technologie. Aujourd'hui, les progrès en matière d'analyse, de surveillance en temps réel et de technologie de jumeau numérique ont marqué le début d'une nouvelle ère d'amélioration continue de la qualité, permettant aux entreprises des sciences de la vie d'anticiper, de prévenir et de résoudre les problèmes de qualité avec une précision et une agilité sans précédent. Innovations favorisant le CQI dans le secteur des sciences de la vie Certaines des innovations de pointe dans le secteur des sciences de la vie visant à améliorer le CQI sont : Analyse avancée et modélisation prédictive La convergence de l'analyse avancée et de la modélisation prédictive a révolutionné la façon dont les entreprises des sciences de la vie analysent et exploitent les données. En exploitant la puissance des algorithmes d'apprentissage automatique et de l'analyse du Big Data, les entreprises peuvent extraire des informations exploitables à partir de vastes ensembles de données, ce qui leur permet de prédire les tendances en matière de qualité, d'optimiser les processus et de prendre des décisions fondées sur les données qui améliorent la sécurité des patients et l'efficacité des produits. Systèmes de surveillance et de contrôle en temps réel Les systèmes de surveillance et de contrôle en temps réel représentent un changement de paradigme dans la gestion de la qualité, offrant aux fabricants des sciences de la vie une visibilité et un contrôle inégalés sur leurs processus de production. En tirant parti des capteurs, des appareils IoT et des plateformes basées sur le cloud, les entreprises peuvent surveiller en permanence les paramètres de qualité critiques en temps réel, détecter instantanément les écarts et mettre en œuvre des actions correctives de manière proactive pour garantir la qualité et la conformité des produits. Innovations favorisant le CQI dans le secteur des sciences de la vie Technologie des jumeaux numériques La technologie des jumeaux numériques est devenue un véritable tournant dans le secteur des sciences de la vie, permettant aux entreprises de créer des répliques virtuelles de leurs processus et systèmes de fabrication. En simulant et en optimisant les opérations dans un environnement virtuel, les entreprises peuvent identifier les inefficacités, tester des hypothèses et optimiser les paramètres des processus sans perturber la production. Les jumeaux numériques offrent un bac à sable sans risque pour l'innovation, permettant aux entreprises d'expérimenter, d'itérer et d'affiner leurs processus avec une vitesse et une précision sans précédent. Blockchain et transparence de la chaîne d'approvisionnement La technologie Blockchain est extrêmement prometteuse pour améliorer la transparence et la traçabilité de la chaîne d'approvisionnement des sciences de la vie. En tirant parti du registre immuable et de la sécurité cryptographique de la blockchain, les entreprises peuvent créer un enregistrement transparent et vérifiable de chaque transaction et échange de données tout au long de la chaîne d’approvisionnement. De l’approvisionnement en matières premières à la distribution et au-delà, la blockchain garantit une visibilité, une intégrité et une conformité de bout en bout, garantissant ainsi l’authenticité des produits et la sécurité des patients. Impact des innovations sur le secteur des sciences de la vie L'adoption de ces innovations a catalysé un changement de paradigme dans le secteur des sciences de la vie, favorisant l'excellence dans de multiples dimensions : Amélioration de la qualité des produits et de la sécurité des patients : en tirant parti de l'analyse avancée, de la surveillance en temps réel et des jumeaux numériques, les entreprises des sciences de la vie peuvent garantir la qualité et la sécurité constantes de leurs produits, préservant ainsi la santé et la confiance des patients. Efficacité opérationnelle améliorée et économies de coûts : les innovations en matière d'amélioration continue de la qualité permettent aux entreprises de rationaliser les processus de production, d'optimiser l'utilisation des ressources et de réduire les déchets, ce qui entraîne une amélioration de l'efficacité et des économies de coûts. Conformité réglementaire et préparation aux audits : en mettant en œuvre des mesures de contrôle qualité et des systèmes de traçabilité robustes, les entreprises peuvent démontrer leur conformité aux exigences réglementaires et rester prêtes aux audits à tout moment. Innovation accélérée et délais de mise sur le marché : en adoptant les technologies numériques et en pré Grâce à la modélisation dictive, les entreprises des sciences de la vie peuvent accélérer les cycles d'innovation, réduire les délais de mise sur le marché et proposer plus rapidement et plus efficacement aux patients des traitements qui sauvent des vies. Conclusion La frontière de l'amélioration continue de la qualité dans le secteur des sciences de la vie se caractérise par une innovation sans précédent, alimentée par des technologies de pointe et un engagement incessant envers l'excellence. À mesure que les entreprises adoptent l’analyse avancée, la surveillance en temps réel et les jumeaux numériques, elles sont prêtes à améliorer la qualité de leurs produits, à améliorer leur efficacité opérationnelle et à garantir la conformité réglementaire à chaque étape du cycle de vie des produits. La poursuite de l'excellence par l'amélioration continue de la qualité n'est pas simplement un impératif stratégique mais une obligation morale pour les entreprises des sciences de la vie qui se consacrent à l'amélioration de la santé et du bien-être humains.

Faire progresser l’assurance qualité pharmaceutique : synergie des tests de libération en temps réel, de la vérification continue des processus et de l’APQR

Exploiter les logiciels statistiques pour l'assurance qualité et l'analyse APQR dans les sciences de la vie

Assurer la qualité grâce à un logiciel de validation du nettoyage dans la fabrication pharmaceutique

Paramètres de processus critiques dans la fabrication pharmaceutique

IA et No-Code : l'avenir de la fabrication pharmaceutique
Découvrez comment l'IA et les plateformes sans code transforment la fabrication pharmaceutique avec un contrôle qualité plus intelligent, une maintenance prédictive et une documentation prête pour l'inspection.

The Real Cost of Delaying Low-Code & AI Adoption in Pharma
Discover the hidden operational debt pharma companies face by delaying low-code and AI adoption—and how AmpleLogic helps reduce it with GxP-compliant workflows.

L'IA dans les opérations pharmaceutiques : comment AmpleLogic réduit l'effort manuel de 60 %
Automatisez les évaluations annuelles de la qualité des produits avec AmpleLogic. Réduisez le temps de préparation de 70 à 80 %, garantissez la conformité aux BPF et générez plus rapidement des rapports PQR conformes à la réglementation.

Pourquoi chaque équipe de réglementation a besoin d'une solution RIMS ?
Découvrez pourquoi les équipes de réglementation pharmaceutique ont besoin d'une solution RIMS pour gérer avec précision les soumissions, les renouvellements, les mises à jour CMC et les dépôts mondiaux avec AmpleLogic RIMS.

Pourquoi chaque usine pharmaceutique a besoin d’un journal de bord électronique ?
Découvrez pourquoi les usines pharmaceutiques ont besoin de journaux de bord électroniques pour garantir la conformité, éliminer les erreurs manuelles et améliorer l'intégrité des données grâce à des solutions basées sur l'IA.

Comment l’IA réduit le temps de traitement des écarts dans le système QMS pharmaceutique
AmpleLogic AI réduit le temps de traitement des écarts pharmaceutiques, automatise l’analyse des causes profondes, améliore la conformité et accélère les enquêtes.

Guide complet de validation du nettoyage dans la fabrication pharmaceutique
Le guide AmpleLogic pour la validation du nettoyage dans le secteur pharmaceutique garantit la conformité aux BPF, prévient la contamination et améliore l'efficacité de la fabrication.

Actavis a été mis en ligne avec la solution AmpleLogic eLogbook

Eisai Pharmaceuticals a été mis en service avec succès avec le logiciel de gestion de la formation des employés AmpleLogic
Eisai Pharmaceuticals a été mis en service avec succès avec le logiciel de gestion de la formation des employés AmpleLogic

Hetero Labs Limited lance le logiciel d'étalonnage et de maintenance préventive AmpleLogic
Hetero Labs Limited lance le logiciel d'étalonnage et de maintenance préventive AmpleLogic

Un laboratoire pharmaceutique américain choisit le logiciel de stabilité AmpleLogic

Tirupati Lifesciences nous a choisi pour mettre en œuvre la solution DMS

Indoco Remedies Ltd choisit les solutions logicielles de qualité d'AmpleLogic

FDC Limited choisit AmpleLogic pour mettre en œuvre des solutions de qualité

Micro Labs est lancé avec le système AmpleLogic DMS

Les 9 principaux défis et solutions pour les logiciels eDMS dans l'industrie pharmaceutique

Pourquoi l'adoption du système de gestion de documents est-elle toujours intimidante ?

Avantages du système de gestion de la formation

Catégories GAMP 5, modèle V et 21 CFR Part 11, Annexe 11 de l'UE

Intégration de l'intelligence artificielle et de l'apprentissage automatique dans QMS

Analyse des causes profondes avec exemple pour « 5 » Pourquoi la technique

APQR 2.0 : le saut quantique d'AmpleLogic en matière d'assurance qualité et d'excellence tournée vers l'avenir

Vos journaux de bord sont-ils en place pour l’audit à venir ?
En tant que fabricant pharmaceutique, vous connaissez probablement les exigences réglementaires strictes régissant l’industrie. Un aspect essentiel de la conformité est de maintenir des enregistrements et une documentation précis et à jour. Mais avez-vous réfléchi au rôle des journaux de bord dans votre système de tenue de dossiers ? Sinon, vous voudrez peut-être commencer.

Les systèmes de gestion de documents sont une aubaine pour les secteurs pharmaceutiques topiques
L’intégration des technologies numériques dans le secteur des sciences de la vie est devenue une nécessité commerciale ces derniers temps. Avec les mises à jour quotidiennes de la réglementation, l’augmentation de la documentation et la nécessité d’audits plus rapides, les sociétés pharmaceutiques s’éloignent progressivement des processus manuels. L’un de ces changements concerne les systèmes de gestion de documents (DMS), un outil qui devient essentiel pour garantir la conformité, l’efficacité et l’intégrité des données. Même si les innovations numériques ont touché tous les secteurs, leur rôle dans les opérations pharmaceutiques et l’assurance qualité est particulièrement transformateur. Parmi les nombreux outils qui transforment le secteur, DMS se distingue comme une solution importante, automatisant les flux de travail documentaires, réduisant la dépendance au papier et offrant un contrôle centralisé sur la documentation cruciale.

Implémentation de la validation du temps et du contenu avec un logiciel de gestion de l'apprentissage
La popularité croissante de l'apprentissage en ligne via les logiciels de systèmes de gestion de l'apprentissage électronique a gagné du terrain dans diverses industries, en particulier dans le secteur pharmaceutique. L’industrie pharmaceutique, l’un des secteurs les plus vitaux d’Europe et d’autres économies, a connu une croissance rapide ces dernières années. Après la pandémie, les soins de santé et la vaccination sont devenus des priorités absolues pour de nombreux pays. Toutefois, l’urgence s’est également étendue à d’autres médicaments essentiels présents sur le marché. Dans cet environnement en évolution rapide, le LMS pharmaceutique est devenu un élément essentiel pour former le nouveau personnel et offrir des certifications afin de garantir que les travailleurs sont prêts à répondre aux demandes croissantes du secteur. À mesure que l’industrie pharmaceutique continue de se développer, le besoin de main-d’œuvre qualifiée augmente régulièrement. Selon le rapport le plus récent de MarketsandMarkets :

Adoption de Pharma 4.0 en Inde : un catalyseur pour la modernisation du secteur pharmaceutique
Le terme Pharma 4.0 n’est plus un concept discuté lors de conférences ; il est mis en œuvre sur le terrain en Inde. Dans les laboratoires de formulation et les unités de fabrication, les sociétés pharmaceutiques mettent régulièrement à niveau leurs systèmes obsolètes, en y apportant l’automatisation, la visibilité des données et une infrastructure plus intelligente. Ce changement résout les problèmes de l’industrie locale : retards de production, manquements à l’intégrité des données, dépendances manuelles et surveillance réglementaire croissante. Alors que le secteur pharmaceutique indien adopte la numérisation et les technologies avancées, plusieurs transformations nécessaires sont en cours :

Le système de gestion de l’apprentissage est-il aujourd’hui une demande nouvelle en matière de numérisation ?

AmpleLogic : offrir des avantages et une qualité maximale à un coût minimal

Pourquoi les entreprises pharmaceutiques en croissance devraient automatiser leur processus qualité

CSA (Computer Software Assurance) Un passage du CSV traditionnel

Pharma 4.0: Faster Digitalization with Low Code Platforms

TOP 3 des tendances qui transformeront les perspectives de l’industrie pharmaceutique en 2025

7 problèmes de conformité courants rencontrés par l’industrie pharmaceutique

Conformité à l'annexe M de la Loi sur les médicaments et les cosmétiques (2018)

Dévoilement des 8 avantages d'un logiciel de gestion de la qualité en pharmacie

Les 7 principales requêtes traitées : intégrité des données et conformité CGMP

L'harmonisation des registres volumineux facilite la tenue de registres dans l'industrie pharmaceutique

11 KPI importants pour le système de gestion de la qualité

Garantir l’intégrité des données est facilité par l’eDMS dans l’industrie pharmaceutique

Rationaliser la fabrication pharmaceutique avec le logiciel DMS

Éléments essentiels pour améliorer la qualité des soins de santé : 5 éléments clés

8 violations courantes des BPC dans les essais cliniques

Un aperçu complet des différents types d'audit en matière de gestion de la qualité

Implémentation de la solution AmpleLogic eQMS « Go-Live » chez Medopharm

Teva lance le logiciel de gestion des programmes d'étalonnage AmpleLogic

Niveau remarquable de numérisation dans les entreprises pharmaceutiques avec DMS

AmpleLogic : proposer un système de gestion de la qualité GMP pour obtenir un retour sur investissement optimal

Favoriser l'agilité et la conformité avec les solutions QMS et MES Low-Code
Dans l’environnement hautement réglementé actuel des sciences de la vie, les organisations doivent trouver un équilibre entre agilité et exigences de conformité strictes. Les solutions QMS et MES low-code transforment la façon dont les entreprises pharmaceutiques et biotechnologiques gèrent les flux de travail liés à la qualité, à la fabrication et à la réglementation en permettant un développement rapide d'applications sans codage approfondi. La plateforme low-code d'AmpleLogic fournit un écosystème unifié qui intègre la gestion de la qualité, l'exécution de la fabrication, les systèmes de laboratoire et les processus réglementaires dans un cadre unique basé sur les données. Cela élimine les silos, améliore la visibilité en temps réel et permet une prise de décision plus rapide dans toutes les opérations. Grâce à des cadres de conformité intégrés tels que FDA 21 CFR Part 11, GxP et Annexe 11, les organisations peuvent garantir la préparation aux audits tout en accélérant les délais de déploiement de plusieurs mois à plusieurs semaines. La configuration par glisser-déposer de la plateforme, les flux de travail automatisés et les informations basées sur l'IA contribuent à réduire les efforts manuels, à améliorer l'intégrité des données et à favoriser une amélioration continue. En adoptant des solutions QMS et MES low-code, les entreprises peuvent atteindre une plus grande agilité opérationnelle, réduire les coûts et maintenir une conformité réglementaire cohérente, ce qui en fait une stratégie essentielle pour la transformation numérique moderne dans le secteur des sciences de la vie.

Industrie 4.0 : la fabrication numérique dans l'industrie pharmaceutique
L'industrie pharmaceutique est à l'aube d'une révolution numérique. Les technologies de l'Industrie 4.0 transforment la façon dont les médicaments sont fabriqués, testés et distribués dans le monde entier.

13 façons de booster votre laboratoire avec le logiciel LIMS
Un système de gestion des informations de laboratoire (LIMS) est un outil essentiel pour les laboratoires pharmaceutiques modernes, rationalisant les flux de travail, améliorant la conformité et stimulant l'efficacité.

Garantir la conformité réglementaire dans la validation du nettoyage pharmaceutique
La conformité réglementaire dans la validation du nettoyage pharmaceutique est non négociable. Comprendre et mettre en œuvre les bons protocoles garantit la sécurité des produits et l'intégrité de la fabrication.

Meilleures pratiques pour la mise en œuvre de la validation du nettoyage dans le secteur pharmaceutique
La mise en œuvre des meilleures pratiques de validation du nettoyage dans la fabrication pharmaceutique est essentielle pour maintenir la qualité des produits, prévenir la contamination croisée et assurer la conformité GMP.

10 fonctionnalités indispensables pour votre logiciel LIMS idéal
Choisir le bon logiciel LIMS est une décision cruciale pour les laboratoires pharmaceutiques. Le bon système peut transformer les opérations de laboratoire, améliorer la conformité et accélérer le délai d'obtention des résultats.

Naviguer dans l'intégration de l'IA et du ML dans le logiciel MES pharmaceutique
L'intégration de l'intelligence artificielle et de l'apprentissage automatique dans les systèmes d'exécution de fabrication transforme la production pharmaceutique grâce à l'analyse prédictive et à l'optimisation en temps réel.

Planification à long terme dans l'écosystème pharmaceutique
La planification à long terme est un impératif stratégique pour les entreprises pharmaceutiques qui naviguent dans des environnements réglementaires complexes, des dynamiques de marché en évolution et une transformation technologique.

Libérer la puissance de l'aPaaS avec les solutions COTS et les plateformes Low-Code
La convergence de l'aPaaS (Application Platform as a Service) avec les solutions COTS (Commercial Off-The-Shelf) et le développement low-code remodèle la façon dont les entreprises pharmaceutiques conçoivent et déploient leurs applications.

Maîtriser la qualité pharmaceutique grâce à l'intégration de la capabilité de processus et de l'APQR
La concurrence est extrêmement intense dans l'industrie pharmaceutique et biotechnologique, où les standards de qualité sont donc très exigeants. Cela nécessite une surveillance et une investigation constantes des processus impliqués.

Surveillance environnementale continue à l'aide du BMR dans la fabrication pharmaceutique
La surveillance continue des conditions environnementales est primordiale dans l'industrie pharmaceutique et dans divers autres secteurs, garantissant le respect des normes réglementaires et la qualité des produits.

Améliorer la conformité réglementaire grâce aux BMR sans papier dans le secteur pharmaceutique
L'industrie pharmaceutique s'oriente de plus en plus vers des dossiers de fabrication de lots (BMR) sans papier, sous l'impulsion des exigences réglementaires et du besoin d'une meilleure intégrité des données et conformité.

Directives de validation du nettoyage dans l'industrie pharmaceutique
La validation du nettoyage dans l'industrie pharmaceutique est un processus essentiel défini par les organismes de réglementation pour maintenir la qualité des produits et prévenir la contamination croisée.

L'approche moderne des logiciels de revue de produit : révolutionner la gestion de la qualité et de la conformité
Dans les secteurs d'aujourd'hui, rapides et très réglementés, le logiciel de revue de produit est devenu un outil indispensable. Évoluant de simples systèmes de suivi vers des plateformes sophistiquées et intégrées.

Explorer les outils d'investigation des déviations
Dans la quête de l'excellence opérationnelle et de l'assurance qualité, les écarts par rapport aux normes établies ne sont pas seulement attendus, mais anticipés. Ce qui distingue vraiment les organisations performantes, c'est la façon dont elles gèrent ces écarts.
%20Software.webp&w=3840&q=75)
Améliorer les performances commerciales et la qualité des produits grâce au logiciel de revue annuelle des produits (APR)
Dans l'environnement commercial concurrentiel d'aujourd'hui, maintenir une haute qualité des produits et améliorer continuellement les offres est essentiel pour le succès. Le logiciel APR s'est imposé comme un outil puissant.
Suivi des dossiers de lots avec le logiciel MES pharmaceutique
Dans le monde dynamique et très réglementé de la fabrication pharmaceutique, l'intégration de technologies avancées est essentielle pour exceller dans les processus métier clés et garantir une qualité de produit conforme aux normes.
Explorer les 3 questions de l'APQR : Quoi, Pourquoi et Où
En explorant les aspects essentiels entourant la revue annuelle de la qualité des produits (APQR), cette investigation aborde les questions fondamentales du Quoi, Pourquoi et Où.

Du manuel à l'automatisé : améliorer la validation des BMR dans le secteur pharmaceutique
Dans l'industrie pharmaceutique, la validation des dossiers de fabrication de lots (BMR) est essentielle pour garantir la qualité des produits, la sécurité et la conformité réglementaire. Traditionnellement, cette validation était un processus manuel.

Rationaliser les opérations pharmaceutiques : l'impact du logiciel de gestion des actifs d'entreprise
Dans le paysage pharmaceutique en rapide évolution, la gestion efficace des actifs est primordiale. Des laboratoires de recherche aux installations de fabrication et aux réseaux de distribution.

Mettre en œuvre ALCOA+ dans vos processus de fabrication
Dans l'industrie pharmaceutique, l'intégrité des données est primordiale. Les principes ALCOA — Attribuable, Lisible, Contemporain, Original et Exact — ont été établis pour garantir l'intégrité des données en fabrication.

AmpleLogic établit une nouvelle norme avec l'IA dans le système de gestion de l'apprentissage pharmaceutique
Les systèmes de gestion de l'apprentissage (LMS) jouent un rôle de plus en plus vital dans l'industrie pharmaceutique, offrant un moyen structuré et efficace de gérer la formation, la conformité et le développement professionnel.
-in-Equipment.webp&w=3840&q=75)
Intégration des dossiers de lots électroniques (EBR) dans les opérations d'équipements
L'efficacité et la précision sont des aspects essentiels dans les industries des sciences de la vie et pharmaceutiques. Elles aident les entreprises à atteindre l'excellence des processus métier en s'écartant des processus manuels traditionnels.

Intelligence artificielle : révolutionner les revues annuelles de la qualité des produits dans le secteur pharmaceutique
La revue annuelle de la qualité des produits (APQR) est un processus essentiel pour que les entreprises pharmaceutiques évaluent les standards de qualité de leurs produits, assurent la conformité réglementaire et stimulent l'amélioration continue.

Les défis du contrôle des changements dans un secteur réglementé
Le contrôle des changements est un processus essentiel dans les secteurs réglementés, tels que les produits pharmaceutiques, les dispositifs médicaux et les aliments et boissons. Il implique la gestion des modifications apportées aux produits, aux processus et aux systèmes.

Optimiser le logiciel de maintenance des équipements en production et fabrication pharmaceutiques
La maintenance des équipements est un aspect crucial pour garantir l'efficacité et la productivité des départements de production et de fabrication pharmaceutiques. Le logiciel de maintenance des équipements a révolutionné le domaine.
L'impact du système de suivi des actifs dans la fabrication pharmaceutique
Dans le monde complexe de la fabrication pharmaceutique, où la précision, la conformité et l'efficacité sont des atouts clés, les entreprises cherchent des solutions innovantes pour naviguer dans cette complexité.

Naviguer vers l'excellence opérationnelle : le rôle de l'analyse APQR
Dans le paysage complexe et en constante évolution de l'industrie moderne, où la quête de l'excellence opérationnelle est à la fois un impératif stratégique et une pierre angulaire du succès durable.
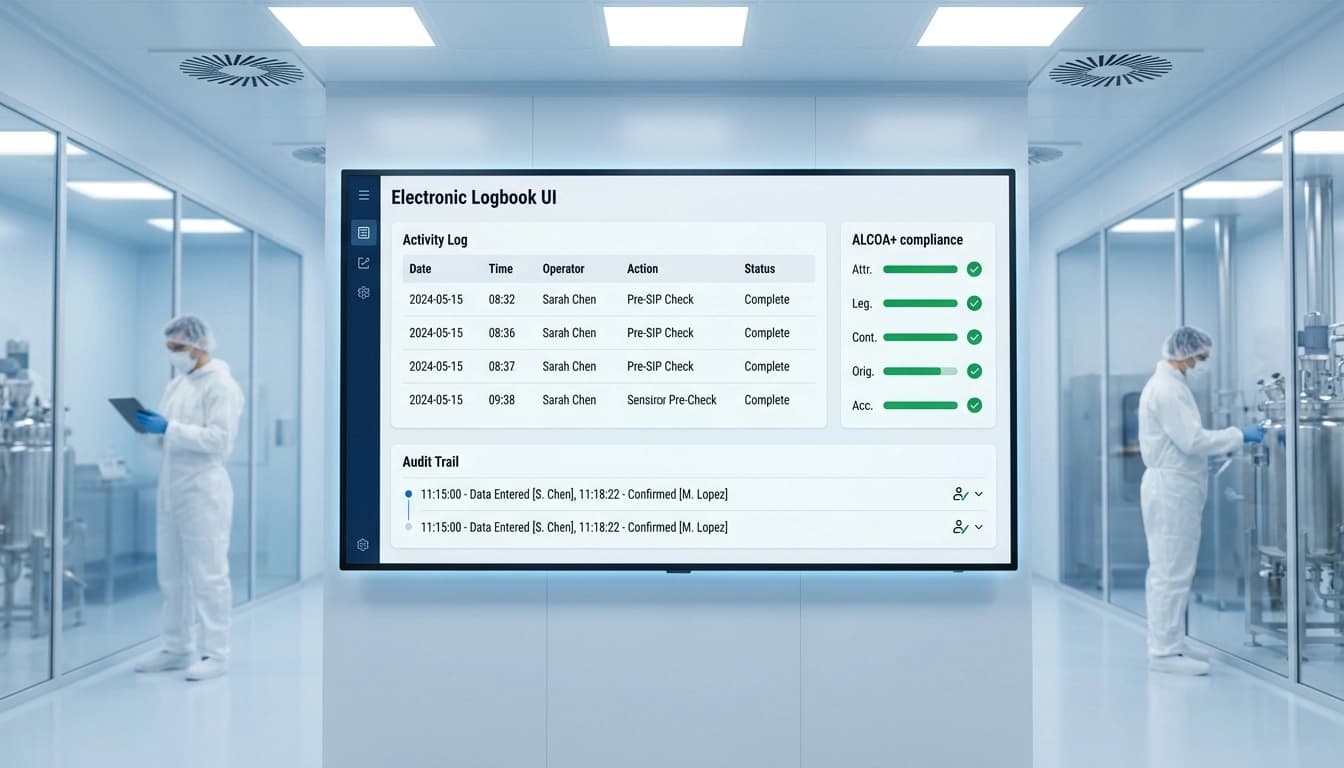
Garantir l'intégrité des données avec le journal électronique dans la fabrication pharmaceutique
Dans l'industrie pharmaceutique, maintenir l'intégrité des données est essentiel pour garantir la qualité des produits, la sécurité des patients et la conformité réglementaire. L'intégrité des données fait référence à l'exactitude et à la cohérence des données.
-Software-in-Deviation-Handling.webp&w=3840&q=75)
Rôle du logiciel de dossiers de lots électroniques (EBR) dans la gestion des déviations dans la fabrication pharmaceutique
L'efficacité, la précision et la conformité sont des composantes essentielles de l'industrie de la fabrication pharmaceutique. Tout écart par rapport aux procédures opérationnelles standard peut compromettre la qualité du produit.

Analyse des causes profondes avec exemple pour la technique des « 5 » Pourquoi
L'analyse des causes profondes (RCA) est une méthode utilisée pour traiter un problème ou une non-conformité dans le processus qualité afin d'identifier la « cause profonde » de la non-conformité. La RCA aide à corriger ou à éliminer la cause et à prévenir la récurrence du problème grâce à des actions préventives.

Avantages d'un système de gestion de la formation pour la conformité GMP pharmaceutique
Un système de gestion de la formation (TMS) pharmaceutique simplifie la formation à la conformité GMP, le suivi des compétences et la préparation aux audits réglementaires. Découvrez comment un LMS moderne réduit les coûts de formation jusqu'à 50 %, accélère la qualification des employés et garantit la conformité à la 21 CFR Part 11 dans les opérations mondiales.

Pourquoi l'adoption du système de gestion documentaire reste-t-elle intimidante ?
Le système de gestion électronique des documents (eDMS) a fondamentalement changé la façon dont les entreprises pharmaceutiques et de sciences de la vie gèrent leur documentation. Pourtant, malgré la validation FDA 21 CFR Part 11 et les avantages évidents en matière de conformité, de nombreuses organisations hésitent encore à adopter pleinement cette transformation numérique.

Adapter le modèle V pour accélérer les automatisations GMP et résoudre les problèmes d'intégrité des données
La longue liste d'avertissements relatifs à l'intégrité des données reçus par les entreprises pharmaceutiques les a amenées à concentrer leur attention sur la construction et le renforcement de leurs mécanismes de suivi. L'une des solutions est la numérisation — mais le défi actuel est que la transformation numérique progresse plus lentement que prévu.
Abonnez-vous à notre newsletter
Restez informé des dernières tendances en matière de fabrication pharmaceutique, de conformité et de transformation numérique.
Gardez une longueur d'avance dans les sciences de la vie
Recevez les dernières mises à jour produit, actualités de conformité et analyses du secteur directement dans votre boîte mail.
