Gérez les Études de Stabilité de Bout en Bout dans Votre LIMS
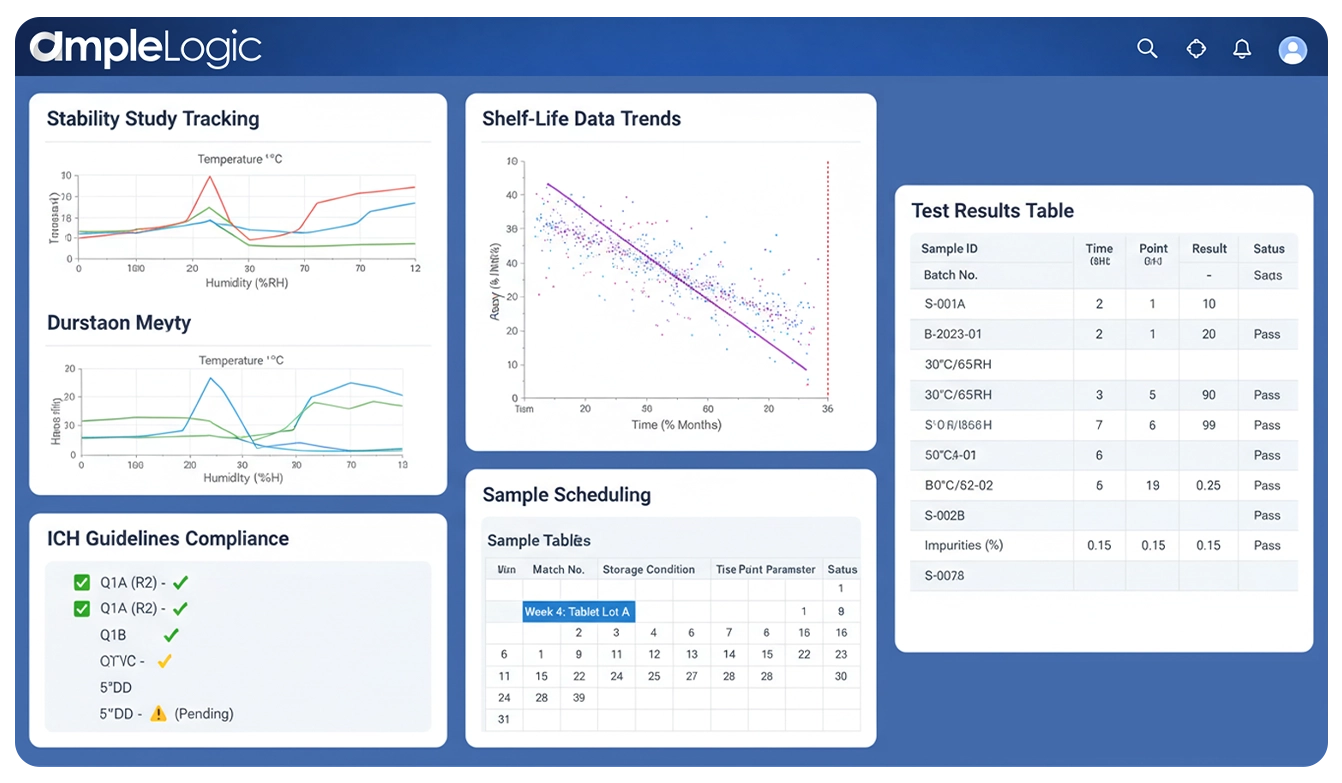
AmpleLogic offre une gestion complète du calendrier de stabilité — de la création du protocole de test de stabilité et de la planification du calendrier des études de stabilité jusqu'à la surveillance des enceintes, l'exécution des tests, l'analyse des tendances, la détermination de la durée de conservation et les rapports réglementaires conformes aux exigences ICH Q1A, FDA et GMP.
40%
Configuration d'Étude Plus Rapide
100%
Conformité ICH
30%
Réduction des Prélèvements Manqués
60%
Moins de Suivi Manuel
50%
Économies de Coûts
3–6
Mois de Déploiement
Qu'est-ce que la Gestion du Calendrier de Stabilité ?
La gestion du calendrier de stabilité est la planification systématique, l'exécution et le suivi des études de stabilité pharmaceutique. Elle garantit que chaque lot de produit est soumis aux conditions de stockage appropriées, aux points de prélèvement et aux tests analytiques définis par le protocole de test de stabilité — permettant une détermination précise de la durée de conservation et la conformité réglementaire avec ICH Q1A, FDA 21 CFR Part 211.166 et les exigences GMP.
Protocole de Test de Stabilité
Un protocole de test de stabilité définit la conception de l'étude — conditions de stockage, points temporels, paramètres de test, critères d'acceptation et configurations d'emballage. AmpleLogic automatise la création de protocoles avec des modèles conformes à ICH Q1A.
Calendrier des Études de Stabilité
Le calendrier des études de stabilité est une chronologie visuelle de toutes les dates de prélèvement, des allocations d'enceintes et des affectations d'analystes pour toutes les études actives. AmpleLogic génère et maintient automatiquement ce calendrier en temps réel.
Gestion du Calendrier de Stabilité
La gestion du calendrier de stabilité coordonne l'ensemble du cycle de vie — depuis l'approbation du protocole jusqu'aux prélèvements d'échantillons, l'exécution des tests, l'analyse des tendances et la détermination de la durée de conservation — sur une seule plateforme validée.
Défis de la Gestion du Calendrier de Stabilité sans Automatisation
Les organisations qui s'appuient sur des processus manuels pour la gestion des protocoles de test de stabilité et le suivi du calendrier des études de stabilité font face à des risques critiques.
Gestion Manuelle du Calendrier de Stabilité
Les équipes s'appuient sur des tableurs et des registres papier pour planifier les calendriers de stabilité, ce qui entraîne des prélèvements manqués, des conflits de planification et un manque de visibilité en temps réel sur les délais des études.
Protocoles de Test de Stabilité Inconsistants
Sans système standardisé, la création des protocoles de test de stabilité varie selon les équipes et les sites, entraînant des lacunes réglementaires, des résultats d'audit et des conceptions d'études inconsistantes.
Absence de Calendrier Centralisé des Études de Stabilité
L'absence d'un calendrier unifié des études de stabilité signifie que les analystes ne peuvent pas voir les prélèvements à venir, les allocations d'enceintes ou les études qui se chevauchent en un seul endroit.
Données Environnementales Déconnectées
Les données de température et d'humidité des enceintes sont suivies séparément des études de stabilité, créant des lacunes de traçabilité et des retards dans la réponse aux excursions.
Analyse des Tendances et Rapports Retardés
La compilation manuelle des données pour l'analyse des tendances de stabilité retarde la détermination de la durée de conservation, les soumissions réglementaires et les délais de lancement des produits.
Risque de Conformité lié à des Systèmes Fragmentés
L'utilisation de plusieurs outils déconnectés pour la gestion du programme de stabilité augmente les risques d'intégrité des données et rend difficile la préparation aux audits ICH Q1A et FDA.
Approche AmpleLogic pour l'Automatisation des Protocoles et Calendriers de Tests de Stabilité
Six étapes intégrées qui transforment la gestion manuelle du calendrier de stabilité en un flux de travail entièrement automatisé et conforme à l'ICH.
Définir le Protocole de Test de Stabilité
Créez des protocoles de test de stabilité conformes à ICH Q1A avec des conceptions d'études configurables, des conditions de stockage, des critères d'acceptation et des calendriers d'échantillonnage automatisés — le tout dans un seul système validé.
Construire le Calendrier des Études de Stabilité
Générez automatiquement un calendrier visuel des études de stabilité avec des dates de prélèvement aux points temporels, les affectations d'enceintes, l'allocation des analystes et des rappels automatisés — éliminant entièrement la planification manuelle.
Surveiller les Conditions des Enceintes
Surveillance en temps réel de la température et de l'humidité avec des alertes d'excursion automatisées, l'intégration des capteurs et les données environnementales liées directement aux dossiers des études de stabilité.
Exécuter et Capturer les Résultats
Effectuez des tests analytiques dans le flux de travail LIMS intégré avec la connectivité directe aux instruments, les calculs en ligne et la traçabilité complète de l'échantillon au résultat.
Analyser les Tendances et Déterminer la Durée de Conservation
Analyse des tendances de stabilité alimentée par l'IA avec modélisation de la dégradation, projection statistique de la durée de conservation, détermination de la date d'expiration et rapports d'intervalle de confiance.
Générer des Rapports Réglementaires
Produisez automatiquement des rapports de stabilité conformes à l'ICH, des dossiers de soumission à la FDA et la documentation du programme de stabilité GMP à partir de vos données de stabilité.
Hub de Données et Calendrier des Études de Stabilité AmpleLogic
Une plateforme centralisée qui unifie la gestion des protocoles de test de stabilité, le calendrier des études de stabilité, les analyses de tendances et la documentation de conformité en un seul endroit.
Tableau de Bord Unifié des Études
Vue unique de toutes les études de stabilité actives, terminées et planifiées avec le statut en temps réel, les dates de prélèvement à venir et les alertes de retard pour chaque produit et condition.
Moteur de Gestion du Calendrier de Stabilité
Gestion centralisée du calendrier de stabilité avec la planification automatique des prélèvements, la replanification dynamique, la gestion de la file d'attente basée sur les priorités et les vues basées sur le calendrier pour chaque étude.
Analyses de Tendances Interactives
Graphiques de superposition multi-lots, ajustement de courbes de dégradation, détection OOT/OOS et prévision prédictive de la durée de conservation — tous accessibles depuis une seule console d'analyse.
Piste d'Audit Complète
Chaque action — de la création du protocole de test de stabilité à la saisie des résultats et à la génération des rapports — est capturée avec des enregistrements d'audit horodatés, identifiés par l'utilisateur et conformes à ALCOA+.
Centre de Notifications Intelligent
Alertes configurables pour les prélèvements à venir, les tests en retard, les résultats OOT, les excursions d'enceintes et les déviations de protocole avec des flux de travail d'escalade à plusieurs niveaux.
Intégration Intersystèmes
Intégration bidirectionnelle avec LIMS, ERP, QMS et les systèmes d'instruments pour créer une source unique de vérité pour toutes les données de stabilité dans votre organisation.
Gestion Manuelle vs. Automatisée du Calendrier de Stabilité
Découvrez comment AmpleLogic transforme chaque aspect de la gestion des protocoles de test de stabilité et des opérations du calendrier des études de stabilité.
| Domaine | Avant (Manuel) | Après (AmpleLogic) |
|---|---|---|
| Planification des Études | Suivi manuel par tableur, conflits de planification | Calendrier des études de stabilité automatisé avec rappels |
| Création de Protocoles | Documents Word, formats inconsistants selon les sites | Modèles standardisés de protocoles de test de stabilité (ICH Q1A) |
| Gestion des Prélèvements | Prélèvements manqués, sans visibilité en temps réel | Zéro prélèvement manqué avec planification automatique et alertes |
| Surveillance des Enceintes | Capteurs déconnectés, réponse retardée aux excursions | Surveillance en temps réel avec alertes instantanées |
| Analyse des Tendances | Graphiques Excel manuels, semaines de compilation | Analyse alimentée par l'IA, projection instantanée de la durée de conservation |
| Rapports | Compilation manuelle, sujette aux erreurs | Rapports réglementaires ICH/FDA en un clic |
| Préparation aux Audits | Urgence pour rassembler les preuves | Toujours prêt pour les audits avec une piste ALCOA+ complète |
Fiable dans les Sciences de la Vie
Conformité Réglementaire pour la Gestion des Protocoles et Calendriers de Tests de Stabilité
Prêt à Automatiser la Gestion de Votre Calendrier de Stabilité ?
Découvrez comment AmpleLogic transforme la création de protocoles de test de stabilité, la planification du calendrier des études de stabilité et la détermination de la durée de conservation en un seul flux de travail automatisé et conforme à l'ICH.
Gardez une longueur d'avance dans les sciences de la vie
Recevez les dernières mises à jour produit, actualités de conformité et analyses du secteur directement dans votre boîte mail.