Gérez des Laboratoires CQ Plus Intelligents Avec un LIMS Alimenté par l'IA
Plateforme LIMS d'entreprise et système de gestion de l'information de laboratoire basé sur le cloud pour la pharmacie, la biotechnologie et les sciences de la vie réglementées — offrant l'automatisation des flux de travail de laboratoire, l'intégration des instruments et la conformité réglementaire avec l'IA intégrée, ISO 17025, déploiement Low-Code/No-Code, et le seul écosystème GxP numérique intégré de l'industrie.
20%
Délai d'Exécution Plus Rapide
25%
Plus d'Échantillons/Équipe
100%
Intégrité des Données
Fast
Déploiement 3-6 Mois
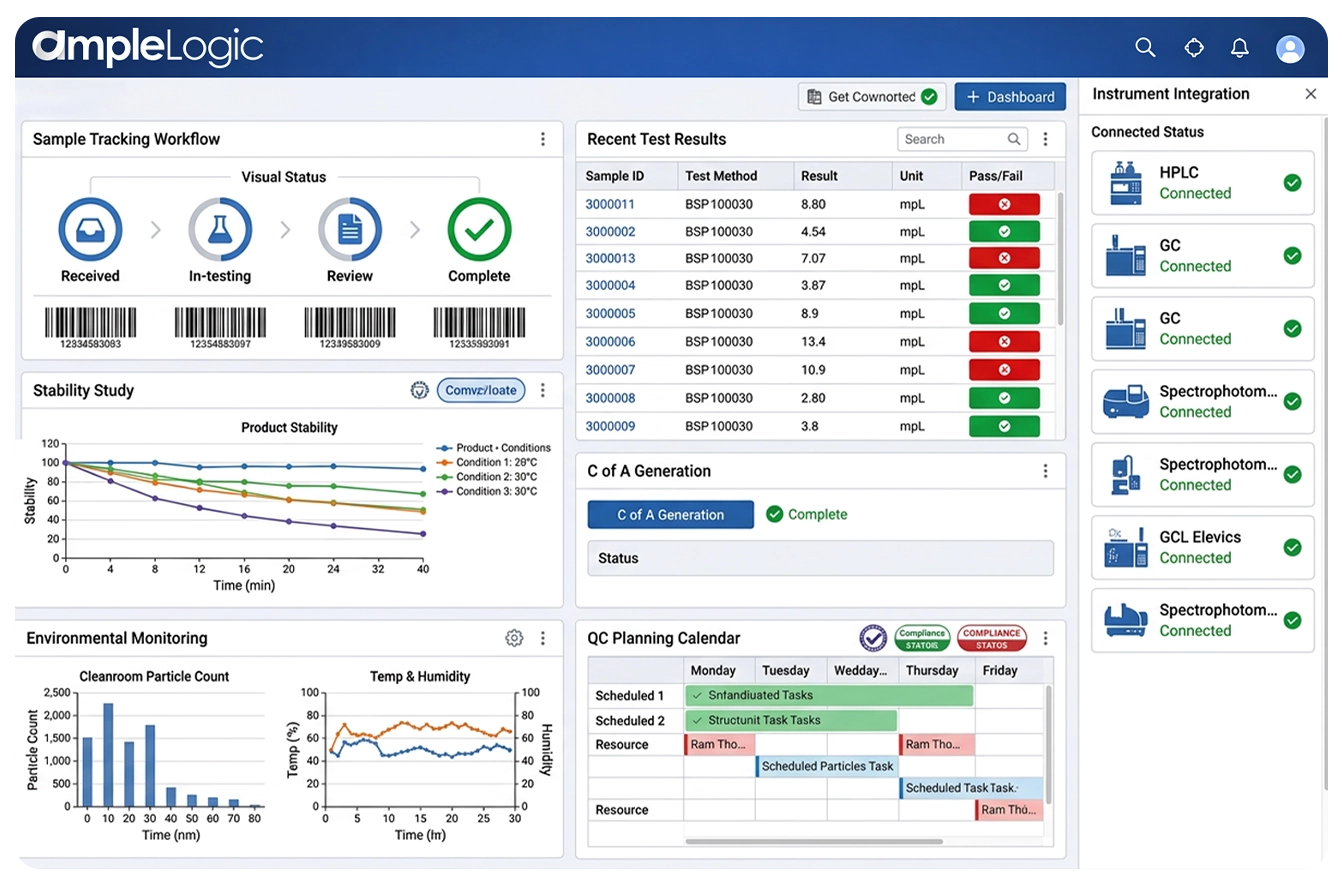
Écosystème de Laboratoire Connecté : Plateforme LIMS Numérique Unifiée
AmpleLogic LIMS crée une source unique de vérité pour les opérations de laboratoire — éliminant les silos de données, réduisant les erreurs de transcription et offrant une visibilité en temps réel à travers l'entreprise en tant que plateforme unifiée de LIMS cloud et de gestion des données scientifiques.
Instruments Analytiques
HPLC, GC, LC-MS, ICP-OES, UV-Vis, dissolution et analyseurs de particules connectés via des interfaces bidirectionnelles validées
Systèmes ERP
Intégration transparente avec SAP, Oracle et NetSuite pour la libération de lots, l'inventaire et la gestion des matières
Exécution de Fabrication
Échange de données en temps réel avec MES et eBMR pour les tests en cours de fabrication, les dossiers de lots et la planification de la production
Gestion de la Qualité
Intégration bidirectionnelle avec eQMS pour le déclenchement des déviations, la gestion CAPA et les investigations OOS
Systèmes de Données Chromatographiques
Connecteurs pré-construits pour Empower, Chromeleon, OpenLab et MassLynx avec importation automatisée des résultats
Gestion Documentaire
SOPs, méthodes analytiques et spécifications synchronisées avec DMS pour des opérations de laboratoire CQ avec contrôle de version
LIMS Conçu pour les Laboratoires Réglementés GxP
Enregistrement des Échantillons
Enregistrement automatisé des échantillons avec lecture de codes-barres/RFID, enregistrement au niveau du lot depuis ERP/MES, et plans d'échantillonnage configurables avec affectations de tests prédéfinies
Suivi des Échantillons
Chaîne de traçabilité en temps réel avec suivi de localisation, gestion du stockage, statut de mise en attente/libération et alertes automatisées à l'approche des délais SLA
Exécution des Tests
Exécution de méthodes analytiques basée sur des modèles avec capture de données instrumentales, vérification de l'aptitude du système et calculs en ligne avec règles d'arrondi configurables
Validation des Résultats
Détection automatisée OOS/OOT, évaluation conforme/non-conforme basée sur des règles, flux de révision et d'approbation multi-niveaux avec signatures électroniques
Certificat d'Analyse
COA/ROA générés automatiquement avec modèles configurables, agrégation au niveau du lot, formats spécifiques au client et distribution numérique
Rapports Réglementaires
Exports de données prêts pour l'inspection, rapports de tendances de stabilité, packages d'analyse statistique et sorties formatées pour les soumissions réglementaires FDA/EMA
Enregistrement des Échantillons
Enregistrement automatisé des échantillons avec lecture de codes-barres/RFID, enregistrement au niveau du lot depuis ERP/MES, et plans d'échantillonnage configurables avec affectations de tests prédéfinies
Suivi des Échantillons
Chaîne de traçabilité en temps réel avec suivi de localisation, gestion du stockage, statut de mise en attente/libération et alertes automatisées à l'approche des délais SLA
Exécution des Tests
Exécution de méthodes analytiques basée sur des modèles avec capture de données instrumentales, vérification de l'aptitude du système et calculs en ligne avec règles d'arrondi configurables
Validation des Résultats
Détection automatisée OOS/OOT, évaluation conforme/non-conforme basée sur des règles, flux de révision et d'approbation multi-niveaux avec signatures électroniques
Certificat d'Analyse
COA/ROA générés automatiquement avec modèles configurables, agrégation au niveau du lot, formats spécifiques au client et distribution numérique
Rapports Réglementaires
Exports de données prêts pour l'inspection, rapports de tendances de stabilité, packages d'analyse statistique et sorties formatées pour les soumissions réglementaires FDA/EMA
Paysage Actuel des Logiciels LIMS
Comprendre l'état de l'informatique de laboratoire et des plateformes LIMS dans la pharmacie aujourd'hui
La plupart des laboratoires ont déjà un LIMS
Présence généralisée d'un système de base
Les LIMS existants sont fortement personnalisés et difficiles à mettre à jour
Les intégrations sur mesure créent des frictions de mise à jour
Coûts de maintenance et de validation élevés
Dépenses continues pour l'entretien et la revalidation réglementaire
Coexistence de multiples solutions ponctuelles
L'outillage fragmenté augmente la charge d'intégration
Priorités du Directeur de Laboratoire CQ : Validation & Coût Total de Possession
Réduire la charge de validation LIMS + Consolider les solutions ponctuelles pour réduire le coût total de possession (TCO) à long terme
Défis Clés avec les Logiciels LIMS Existants
Flux de travail fragmentés, processus manuels et risques de conformité
Principalement Axé sur le Suivi des Échantillons
Limite la visibilité au-delà de l'entrée et la sortie des échantillons
- Limite la Visibilité de Bout en Bout
- Augmente les Transferts Manuels
- Accroît le Risque de Conformité
- Entraîne des Libérations de Produits Plus Lentes
Stabilité et EMS Gérés en Dehors du LIMS
Les opérations fragmentées augmentent la complexité et le risque
- Crée un Contrôle Opérationnel Fragmenté
- Limite la Couverture du Périmètre
- Complique la Validation
- Pousse à Évaluer des Remplacements
Dépendance aux Tableurs
Les processus manuels compromettent la conformité et l'efficacité
- Cause des Mises à Jour de Statut Manuelles
- Affaiblit les Tendances et les Pistes d'Audit
- Augmente les Taux d'Erreur
- Rend les Dirigeants Dépendants de Rapports Informels
Mauvaise Expérience Utilisateur
Les systèmes hérités ralentissent l'adoption et les flux de travail
- Réduit l'Adoption
- Ralentit les Flux de Travail Quotidiens
- Entraîne des Défis de Personnalisation
- Souligne le Besoin d'Améliorations d'Intégration
Défis d'Intégration des Instruments
Silos d'Instruments
Les systèmes HPLC, GC, LC-MS, Micro fonctionnent de manière déconnectée
Transfert Manuel de Données depuis CDS
Les systèmes de données chromatographiques nécessitent des saisies manuelles
Risques d'Intégrité des Données
Lacunes dans les pistes d'audit et violations potentielles de conformité
Charge de Validation Complexe
Chaque connexion nécessite des tests approfondis d'aptitude du système
Prioriser les Connecteurs Validés
Les intégrations d'instruments pré-construites et qualifiées réduisent le risque
Prioriser le Support de Piste d'Audit
Traçabilité complète de l'instrument au rapport
Prioriser la Minimisation des Transferts Manuels
Automatiser la capture de données pour réduire les erreurs et le temps de cycle
Capacités Principales du Logiciel LIMS
Fonctionnalités de logiciel LIMS pharmaceutique conçues pour la gestion moderne des opérations de laboratoire
Gestion du Cycle de Vie des Échantillons
Logiciel de suivi d'échantillons d'entreprise fournissant une gestion du cycle de vie des échantillons de bout en bout, de l'enregistrement à l'analyse, au rapport et à la disposition
Exécution des Tests et Méthodes
Définir et exécuter des procédures analytiques avec une traçabilité complète
Connectivité des Instruments
Logiciel d'intégration d'instruments pour une connectivité transparente avec les instruments de laboratoire CQ, les systèmes de données chromatographiques et l'intégration LIMS ELN
Gestion des Codes-Barres et RFID
Identification automatisée des échantillons et suivi de la gestion des stocks du laboratoire CQ
Flux de Travail de Contrôle Qualité
Vérifications CQ intégrées, approbations et vérification de conformité à travers la plateforme de laboratoire numérique
Signatures Électroniques et Pistes d'Audit
Logiciel de laboratoire conforme FDA avec 21 CFR Part 11 complet, LIMS conforme GxP et exigences LIMS conformes ISO 17025
Rapports Personnalisables
Plateforme d'analytique de laboratoire avec COA, ROA flexibles, analytique de performance de laboratoire et génération de rapports prêts pour la réglementation
Tableaux de Bord Intuitifs
Tableaux de bord de gestion des opérations de laboratoire en temps réel avec KPIs, analytique des données scientifiques et analytique de performance de laboratoire
Modules LIMS Avancés pour les Laboratoires Pharmaceutiques
Solutions LIMS conçues pour les opérations de laboratoire spécialisées
Gestion Avancée de la Stabilité
Logiciel de gestion des études de stabilité conforme ICH pour la pharmacie et la biotechnologie
La Gestion Avancée de la Stabilité d'AmpleLogic est un système de gestion des tests de stabilité conçu pour gérer le cycle de vie complet des études de stabilité — de la création de protocoles de stabilité et la planification des prélèvements à la gestion du stockage en chambre, l'exécution des tests, l'analyse des tendances de stabilité et les rapports réglementaires.
Fonctionnalités Clés
Création de Protocoles de Stabilité
Définir des protocoles de stabilité conformes ICH Q1A avec des conceptions d'études configurables, des conditions de stockage, des critères d'acceptation et des calendriers d'échantillonnage automatisés
Planification des Prélèvements de Stabilité
Planification automatisée des prélèvements avec rappels basés sur le calendrier, reprogrammation dynamique et pistes d'audit complètes
Surveillance des Chambres et de l'Environnement
Surveiller les conditions de stockage de stabilité telles que la température et l'humidité à travers les chambres de stabilité et les entrepôts
Exécution des Tests & Capture de Données
Exécuter des tests analytiques dans le même flux de travail LIMS avec intégration directe des instruments et traçabilité complète
Analyse des Tendances de Stabilité & Rapports
Analyse statistique automatisée des tendances avec ajustement des courbes de dégradation, cartes de contrôle et rapports de stabilité prêts pour la réglementation
Détermination de la Durée de Conservation par IA
Projection de la durée de conservation pilotée par l'apprentissage automatique avec intervalles de confiance, alertes précoces de risque d'expiration et prédiction de stabilité accélérée
Détermination de l'Expiration & Gestion des Dates de Retest
Détermination systématique de l'expiration basée sur les données de tendance de stabilité, calcul de la date de retest et support automatisé des allégations d'étiquetage
Conformité Réglementaire ICH Q1A
Alignement intégré avec les directives de stabilité ICH Q1A-Q1F pour les programmes de stabilité pharmaceutiques et biotechnologiques
Conformité aux Exigences de Stabilité FDA
Flux de travail pré-configurés répondant aux exigences de stabilité FDA incluant 21 CFR Part 211.166
Gestion du Programme de Stabilité GMP
Programmes de stabilité GMP complets avec engagements de stabilité continus et surveillance post-approbation
Analyse des Tendances de Stabilité et Prédiction de Durée de Conservation
L'IA analyse les résultats des tests de stabilité pour identifier les tendances de dégradation des produits et estimer la durée de conservation
Avantages Clés
Accélérer l'exécution des études de stabilité avec la planification automatisée et la gestion des protocoles
Réduire le temps de détermination de la durée de conservation de 40% avec l'analyse des tendances pilotée par l'IA
Assurer une conformité réglementaire complète avec les flux de travail alignés ICH Q1A, FDA et GMP
Éliminer les prélèvements manqués avec la planification automatisée des prélèvements
Centraliser la gestion du stockage en chambre avec la surveillance environnementale en temps réel
11 Fonctionnalités IA Transformant les Opérations LIMS Pharmaceutiques
De la vérification des standards de référence par IA et des assistants virtuels de laboratoire CQ à la maintenance prédictive et au traitement de documents OCR — AmpleLogic LIMS intègre l'automatisation intelligente dans chaque flux de travail de laboratoire
Vérification du Catalogue de Standards de Référence par IA pour les Laboratoires Pharma
L'IA vérifie automatiquement le catalogue de standards de référence et le compare avec les standards actuellement utilisés dans le laboratoire — identifiant les standards mis à jour, expirés, dont la version a changé et nouvellement disponibles pour assurer la conformité réglementaire.
- Assure l'utilisation correcte des standards de référence
- Empêche l'utilisation de standards obsolètes
- Mises à jour automatisées du catalogue et suivi des versions
Assistant de Laboratoire IA (LIMS-MAN) : Formateur LIMS Virtuel
Assistant virtuel intelligent intégré dans la plateforme LIMS. Les utilisateurs interagissent avec des requêtes en langage naturel comme 'Quel est le statut du lot B12345 ?' ou 'Afficher les résultats d'analyse pour le Produit X' — récupérant les données du laboratoire instantanément et agissant comme formateur virtuel pour les nouveaux utilisateurs.
- Accès plus rapide aux informations du laboratoire
- Temps de formation réduit pour les nouveaux utilisateurs
- Navigation et prise de décision LIMS simplifiées
Préparation Automatisée de Feuilles de Travail par IA pour les Laboratoires CQ
L'IA analyse les données STP (Procédure de Test Standard) — incluant les paramètres de test, les formules de calcul, les réactifs requis, les détails des instruments et les critères d'acceptation — pour générer dynamiquement des feuilles de travail numériques prêtes à l'emploi pour les analystes.
- Génération automatique de feuilles de travail de test à partir des données STP
- Remplissage intelligent des champs de calcul
- Élimination des erreurs de transcription
Moteur d'Optimisation des Ressources par IA pour les Opérations de Laboratoire
L'optimiseur de ressources alimenté par l'IA analyse les données de tests historiques et prédit les besoins futurs du laboratoire — estimant les réactifs nécessaires, les standards de référence, les consommables et le temps d'utilisation des instruments pour les lots à venir.
- Planification précise des achats et gestion des stocks
- Réduction des pénuries de réactifs et du gaspillage
- Utilisation optimisée des instruments et réduction des coûts
Revue Automatisée des Résultats par IA & Analyse des Tendances (Réviseur Virtuel)
Le réviseur virtuel piloté par l'IA analyse en continu les données analytiques — détectant les erreurs pendant l'analyse, révisant automatiquement les pistes d'audit, identifiant les tendances anormales, les problèmes d'intégrité des données, les résultats OOT et signalant les déviations de la méthode d'analyse.
- Revue des résultats plus rapide avec des insights pilotés par l'IA
- Détection précoce des problèmes de qualité et des tendances OOT
- Réduction de la charge de travail de revue manuelle
Évaluation de Chromatogrammes par IA pour HPLC, GC & UPLC
L'IA évalue les chromatogrammes des instruments HPLC, GC et UPLC — évaluant automatiquement les aires de pics, les temps de rétention, la symétrie des pics, la résolution et les écarts-types. Alerte immédiatement les analystes lorsque des déviations par rapport aux modèles standards sont détectées.
- Revue automatisée des données chromatographiques
- Détection des pics anormaux et des problèmes d'intégration
- Automatisation de la revue en cours de processus pour les séries d'échantillons
Prédiction de Stabilité & Prévision de Durée de Conservation par IA
Les algorithmes d'apprentissage automatique analysent les données historiques des études de stabilité pour prédire le comportement futur des produits — estimant la durée de conservation, les tendances de dégradation, les probabilités de variation de stabilité et le risque de défaillances de spécification.
- Identification précoce des problèmes potentiels de stabilité
- Prédictions de durée de conservation basées sur les données avec intervalles de confiance
- Documentation réglementaire améliorée pour les programmes de stabilité
Prédiction de Défaillance d'Instrument & Maintenance Prédictive par IA
L'IA surveille en continu les données de performance des instruments — registres de calibration, heures d'utilisation, journaux d'erreurs, historique de maintenance et tendances de performance — utilisant l'analytique prédictive pour estimer les niveaux de risque de défaillance et générer des scores de risque des instruments.
- Alertes de maintenance prédictive avant les défaillances
- Réduction des temps d'arrêt et des retards des instruments
- Planification optimisée de la maintenance
Estimation du Temps d'Échantillonnage par IA pour le CQ Pharma
Le moteur IA analyse les données d'échantillonnage historiques basées sur le type de produit, la catégorie de matériau, le nombre de conteneurs, la taille du lot et la complexité de la procédure d'échantillonnage pour estimer le temps d'échantillonnage prévu pour chaque lot.
- Planification améliorée du laboratoire et de la main-d'œuvre
- Réduction des retards d'échantillonnage
- Efficacité opérationnelle accrue
Traitement de Documents par OCR pour les Données de Laboratoire
La Reconnaissance Optique de Caractères (OCR) extrait automatiquement les informations des documents téléchargés — incluant PDFs, images, rapports scannés, certificats et enregistrements manuscrits — les convertissant en enregistrements numériques structurés intégrés dans la base de données LIMS.
- Extraction automatisée des données des documents scannés
- Élimination de la saisie manuelle des données
- Traitement plus rapide des documents et accessibilité améliorée
Prédiction du TAT de Test d'Échantillon par IA pour l'Efficacité du Laboratoire
L'IA analyse les durées de test historiques et prédit le temps d'achèvement prévu pour chaque échantillon — en tenant compte de la complexité de la méthode de test, de la disponibilité des instruments, de la charge de travail des analystes et des durées de test historiques pour une prévision précise du TAT.
- Prévision précise du temps d'exécution
- Planification et priorisation améliorées des échantillons
- Productivité de laboratoire améliorée
Architecture du Flux de Travail LIMS
Automatisation du flux de travail de laboratoire de bout en bout, de la réception des échantillons aux rapports réglementaires
Données de Référence
Produits, Méthodes, Instruments, Utilisateurs, Normes
Stabilité
Études & Durée de Conservation
Qualification
Validation IQ/OQ/PQ
COA/ROA
Réglementaire
Données de Référence
- •Produits
- •Méthodes
- •Instruments
- •Utilisateurs
- •Normes de Qualité
Gestion Auxiliaire
- •Gestion des Actifs
- •Suivi des Produits Chimiques & Réactifs
- •Gestion des Colonnes
- •Standards de Référence
- •Préparation des Solutions
- •Gestion des Milieux
- •Gestion des Cultures
Cycle de Vie des Échantillons
- •Enregistrement des Échantillons
- •Collecte & Réception
- •Connexion au Système
- •Affectation aux Tests
- •Exécution de l'Analyse
- •Révision & Approbation des Résultats
- •Certificat d'Analyse (COA)
Sortie Réglementaire
- •Certificat d'Analyse (COA)
- •Rapport d'Analyse (ROA)
- •Soumissions Réglementaires
Intégrité des Données LIMS & Conformité Réglementaire
Intégrité des données ALCOA+, 21 CFR Part 11, EU Annex 11, ISO 17025 et conformité GxP — intégrées dans la plateforme LIMS d'entreprise AmpleLogic
Cadre d'Intégrité des Données ALCOA+
Chaque point de données est Attribuable, Lisible, Contemporain, Original et Précis — avec les extensions Complet, Cohérent, Durable et Disponible intégrées dans la plateforme.
- Pistes d'audit immuables pour chaque modification de données
- Signatures électroniques avec intention et signification
- Sauvegarde automatisée avec validation de récupération des données
- Architecture de stockage de données inviolable
Conformité FDA 21 CFR Part 11
Enregistrements et signatures électroniques pré-validés avec contrôles de système fermé, vérifications d'autorité et vérification d'appareil pour les laboratoires réglementés FDA.
- Flux de travail de signature électronique configurables
- Vérifications d'autorité et contrôle d'accès basé sur les rôles
- Enregistrements d'audit horodatés et attribuables
- Architecture de sécurité de système fermé
Conformité EU Annex 11
Contrôles de systèmes informatisés pour la fabrication pharmaceutique européenne incluant les exigences de validation, le stockage de données, les impressions et la continuité d'activité.
- Support de validation des systèmes informatisés (IQ/OQ/PQ)
- Contrôles de migration et d'archivage des données
- Continuité d'activité et reprise après sinistre
- Documentation de qualification des fournisseurs
Conformité Réglementaire GxP
Conformité complète aux Bonnes Pratiques à travers les environnements GLP, GMP et GCP avec des contrôles intégrés pour ICH, WHO, PIC/S et plus de 16 autorités sanitaires mondiales.
- Modèles de flux de travail GLP, GMP, GCP
- Alignement avec les directives ICH Q2, Q7, Q10
- Packages de rapports prêts pour l'inspection
- Support de contrôle des changements et de revalidation
Écosystème GxP Numérique Intégré pour les Laboratoires Pharma & Biotech
Le LIMS pharmaceutique d'AmpleLogic s'intègre nativement avec 13 solutions GAMP — un avantage concurrentiel qu'aucun autre fournisseur ne peut égaler
Les résultats OOS déclenchent automatiquement les déviations ; les résultats CAPA mettent à jour les méthodes de test ; les contrôles de changement gèrent les mises à jour des procédures analytiques
Bidirectionnel : OOS → Déviations, CAPAs → Mises à Jour des Méthodes
Les données de stabilité et les COAs alimentent directement les soumissions réglementaires ; le statut d'enregistrement met à jour les exigences de test des échantillons
LIMS → Données de Stabilité → Soumissions RIMS
Les échantillons en cours de fabrication sont créés automatiquement à partir des dossiers de lots ; les résultats CQ déclenchent les décisions de libération de lots ; les données environnementales sont liées aux lots
Bidirectionnel : Échantillons de Lots ↔ Résultats CQ
Les données de tendances CQ, les résultats de stabilité et les statistiques OOS remplissent automatiquement les rapports de revue annuelle des produits sans compilation manuelle
LIMS → Tendances CQ + Statistiques OOS → Rapports APQR
SOPs, méthodes analytiques et spécifications contrôlées en version dans DMS ; documents effectifs auto-liés dans l'exécution des tests LIMS
DMS → Documents Contrôlés → Exécution des Méthodes LIMS
Les qualifications des analystes sont vérifiées avant l'exécution des tests ; la complétion de la formation active automatiquement l'accès aux méthodes analytiques
LMS → Statut de Formation → Qualification des Analystes LIMS
Les données de tests en cours de fabrication et de libération alimentent les modèles statistiques CPV pour la surveillance continue de la capabilité des processus
LIMS → Données de Processus → Analyse Statistique CPV
Les données de surveillance des salles blanches sont liées aux lots de production ; les excursions déclenchent des flux de travail automatisés de mise en attente/libération dans LIMS
EMS → Données Environnementales → Mise en Attente/Libération des Lots LIMS
Contrairement aux fournisseurs LIMS d'entreprise hérités, orientés R&D ou d'analytique modulaire — AmpleLogic est le seul fournisseur offrant un écosystème GxP complet et nativement intégré où les données LIMS circulent de manière transparente à travers les systèmes de qualité, réglementaires, de fabrication et de conformité sans middleware.
Intégration LIMS d'Entreprise : ERP, ELN & Connectivité Instruments
Connectez votre plateforme LIMS d'entreprise à l'ensemble de votre écosystème opérationnel
Instruments de Laboratoire
Connectivité transparente avec les équipements analytiques
- Spectrométrie de Masse (MS)
- HPLC
- GC
- ICP-OES
- UV-Vis
Systèmes d'Entreprise
Intégration avec les systèmes métier et de fabrication
- SAP
- Oracle
- NetSuite
- MES (Système d'Exécution de Fabrication)
- QMS (Système de Gestion de la Qualité)
- DMS (Système de Gestion Documentaire)
- ELN (Cahier de Laboratoire Électronique)
Données et Analytique
Connexion aux entrepôts de données et à l'intelligence d'affaires
- Entrepôts de Données
- Plateformes BI (Business Intelligence)
- Moteurs IA/ML
- Analytique Cloud
Options de Connectivité
Protocoles multiples pour une intégration flexible
- 100+ Connecteurs Pré-construits
- REST APIs
- SFTP
- Connexions Directes à la Base de Données
- HL7 (Protocoles de Santé)
Architecture API-First
Plateforme moderne et extensible pour les besoins d'intégration personnalisée
- APIs RESTful
- Support Webhook
- Connecteurs Personnalisés
- Frameworks d'Intégration Tiers
Conformité LIMS Automatisée : Éliminez les Vérifications Manuelles Répétitives
Plateforme axée sur l'automatisation réduisant la charge de vérification manuelle
Vérifications Automatisées Basées sur des Règles
Éliminer les vérifications CQ manuelles avec une logique métier configurable et des règles de conformité
Exécution de Méthodes Basée sur des Modèles
Les modèles pré-configurés assurent une exécution cohérente et réduisent la configuration manuelle
Statut de Qualification des Instruments en Temps Réel
Suivi automatique de l'aptitude du système et des calendriers de maintenance
Harmonisation des Données de Référence
Source unique de vérité pour les standards, méthodes et procédures à travers le laboratoire CQ
Revues Pilotées par les Exceptions
Concentrer l'attention des analystes sur les déviations et les résultats hors spécification
Flux de Processus de Bout en Bout
Routage automatisé des échantillons et des résultats à travers le flux de travail complet du laboratoire
ROI du Logiciel LIMS : Impact Commercial Mesurable pour les Laboratoires Qualité
Résultats concrets de la transformation LIMS
+25%
Impact sur le Temps de Cycle
-20%
Perte de Débit
+30%
Charge de Conformité
20%
Réduction du TAT
Temps d'exécution des résultats analytiques 20% plus rapide
25%
Augmentation de la Productivité
25% d'échantillons en plus traités par équipe d'analyste
90%
Préparation à l'Audit
Réduction de 90% du temps pour clôturer les observations
Le Coût Caché des LIMS Hérités
Temps d'Inactivité des Équipements
Les instruments restent inutilisés entre les changements manuels
Perte de capacité de 10-30%
Goulot d'Étranglement des Analystes
Les vérifications et approbations manuelles ralentissent la livraison des résultats
Retards dans le traitement des échantillons
Silos de Données Entre les Systèmes
ELN, MES et CDS fonctionnent indépendamment
Consolidation manuelle et risque d'erreur
Vérifications Manuelles Répétitives
Vérifications identiques effectuées à chaque étape
+25% d'inflation du temps de cycle
Surcharge de Validation et de Contrôle des Changements
Tests approfondis requis pour toute modification du système
+30% de charge de conformité
Comment le LIMS Intelligent Low-Code Surpasse les Plateformes Traditionnelles
Comparaison côte à côte des approches de déploiement
| Dimension | Monolithique Hérité | Modulaire Traditionnel | Low-Code Intelligent |
|---|---|---|---|
| Délai d'Implémentation | 18-24 mois | 12-18 mois | 3-6 mois |
| Coût Total de Possession (TCO) | $2.5-3.5M | $1.8-2.5M | $1.0-1.5M |
| IA & Analytique | Hérité, limité aux rapports | Capacités complémentaires, coût supplémentaire | IA intégrée, analytique prédictive native |
| Personnalisation & Flexibilité | Codé en dur, charge élevée de contrôle des changements | Modulaire mais nécessite des développeurs | Low-code/No-code, les utilisateurs métier peuvent configurer |
Délai d'Implémentation
Hérité : 18-24 mois
Traditionnel : 12-18 mois
Intelligent : 3-6 mois
Coût Total de Possession (TCO)
Hérité : $2.5-3.5M
Traditionnel : $1.8-2.5M
Intelligent : $1.0-1.5M
IA & Analytique
Hérité : Hérité, limité aux rapports
Traditionnel : Capacités complémentaires, coût supplémentaire
Intelligent : IA intégrée, analytique prédictive native
Personnalisation & Flexibilité
Hérité : Codé en dur, charge élevée de contrôle des changements
Traditionnel : Modulaire mais nécessite des développeurs
Intelligent : Low-code/No-code, les utilisateurs métier peuvent configurer
AmpleLogic LIMS : Positionnement sur le Marché & Avantage Concurrentiel
Comment AmpleLogic se compare aux fournisseurs LIMS établis
| Catégorie | Fournisseurs | Positionnement | Limitation |
|---|---|---|---|
| LIMS d'Entreprise Hérité | Fournisseurs Traditionnels | Hautement configurable, base client pharma établie, large support d'instruments | Déploiements de 18-24 mois, personnalisation importante requise, TCO élevé, pas d'écosystème GxP intégré |
| Plateformes R&D d'Entreprise | Fournisseurs Orientés R&D | Modélisation moléculaire + informatique de laboratoire, plateformes cloud, assistants IA/GenAI | Orienté R&D pas CQ, coûteux, dépendance au fournisseur dans des écosystèmes fermés, intégration fabrication limitée |
| Plateformes de Laboratoire Numérique Modernes | Startups Cloud-Native | Cloud-natif, UX moderne, API-first, déploiement rapide pour la R&D | Capacités CQ pharma limitées, conformité réglementaire faible, non validé GMP pour la fabrication |
| LIMS Analytique Modulaire | Fournisseurs Orientés Analytique | Analytique/ML intégrée, cloud-natif HTML5, pile intégrée LIMS+ELN+LES+SDMS | Implémentation complexe, écosystème GxP limité, les fonctionnalités IA nécessitent une surcharge de validation |
| Plateforme GxP Intégrée | AmpleLogic | Informatique de laboratoire pilotée par l'IA + écosystème GxP numérique complet (13 solutions GAMP), Low-Code/No-Code, déploiement 3-6 mois | Nouvel entrant développant une base de références d'entreprise |
LIMS d'Entreprise Hérité
Fournisseurs TraditionnelsPositionnement: Hautement configurable, base client pharma établie, large support d'instruments
Limitation: Déploiements de 18-24 mois, personnalisation importante requise, TCO élevé, pas d'écosystème GxP intégré
Plateformes R&D d'Entreprise
Fournisseurs Orientés R&DPositionnement: Modélisation moléculaire + informatique de laboratoire, plateformes cloud, assistants IA/GenAI
Limitation: Orienté R&D pas CQ, coûteux, dépendance au fournisseur dans des écosystèmes fermés, intégration fabrication limitée
Plateformes de Laboratoire Numérique Modernes
Startups Cloud-NativePositionnement: Cloud-natif, UX moderne, API-first, déploiement rapide pour la R&D
Limitation: Capacités CQ pharma limitées, conformité réglementaire faible, non validé GMP pour la fabrication
LIMS Analytique Modulaire
Fournisseurs Orientés AnalytiquePositionnement: Analytique/ML intégrée, cloud-natif HTML5, pile intégrée LIMS+ELN+LES+SDMS
Limitation: Implémentation complexe, écosystème GxP limité, les fonctionnalités IA nécessitent une surcharge de validation
Plateforme GxP Intégrée
AmpleLogicPositionnement: Informatique de laboratoire pilotée par l'IA + écosystème GxP numérique complet (13 solutions GAMP), Low-Code/No-Code, déploiement 3-6 mois
Limitation: Nouvel entrant développant une base de références d'entreprise
Reconnaissance des Analystes & Prix de l'Industrie pour les Logiciels LIMS
Reconnu par les organisations leaders et les analystes
Frost Radar - Quadrant Leader
Frost & Sullivan
Reconnu comme Leader dans l'espace LIMS Low-Code avec un déploiement 10x plus rapide
120+ Implémentations Mondiales
AmpleLogic
Bilan prouvé avec des clients d'entreprise et des sociétés Fortune 500
Évaluation Gartner 2024-2025
Gartner
Inclus dans le Magic Quadrant Gartner pour l'évaluation LIMS avec crédibilité tierce
2024-2025
"Facile à utiliser et interface conviviale pour la gestion de laboratoire. Réduction du travail manuel et nous aide à évoluer vers des flux de travail de laboratoire entièrement sans papier."
Responsable de Laboratoire
CQ Pharmaceutique
"Bon support fournisseur et réactivité pendant l'implémentation. Les capacités d'intégration des instruments ont considérablement rationalisé nos flux de travail de test CQ."
Analyste CQ
Sciences de la Vie
"Les modules de gestion de la stabilité et de planification des échantillons sont exceptionnels. La visibilité en temps réel des données à travers toutes les opérations de laboratoire a été transformatrice pour notre équipe."
Utilisateur G2 Vérifié
Directeur de Laboratoire
Gardez une longueur d'avance dans les sciences de la vie
Recevez les dernières mises à jour produit, actualités de conformité et analyses du secteur directement dans votre boîte mail.