当前状态:制药过程验证中的手动 CPV 挑战
延迟趋势检测、增加返工并在持续过程验证中提高审计风险的运营瓶颈
来自多系统的手动数据收集
CPP 和 CQA 数据分散在 LIMS、MES、ERP 和电子表格中。手动聚合耗时费力、易出错,且延误趋势识别。
被动响应而非主动监控
没有实时统计分析,过程漂移只能在批次失败后才能检测到。延迟干预增加了拒批量和法规风险。
统计方法不一致
不同分析师使用不同工具(Minitab、Excel)导致控制图方法不一致,能力评估不可靠。
无自动趋势检测
手动审查遗漏了细微的过程变化。Nelson 规则违规和早期能力下降在引发质量事件之前未被注意到。
与 APQR 工作流程脱节
CPV 数据和 APQR 报告各自为政。没有将持续监控数据自动馈入年度产品质量审查的机制。
过程阶段间关联薄弱
第一阶段(过程设计)、第二阶段(确认)和第三阶段(持续验证)之间的可追溯性有限,导致验证生命周期中存在空白。
报告工作量大
每季度每个产品手动准备 CPV 报告消耗 40-60 小时,使 QA 资源无法专注于主动质量改进。
审计准备不足
文档零散和静态快照使得在法规检查期间难以证明持续的受控状态。
FDA 过程验证生命周期:CPV 合规的三个阶段
CPV(第三阶段)确保过程在整个商业生产过程中保持已验证状态
第一阶段
过程设计
基于科学理解定义关键过程参数、质量属性和设计空间。
- 定义 CPP 和 CQA
- 建立设计空间和已验证可接受范围
- 风险评估和控制策略
- 定义第三阶段的监控计划
第二阶段
过程确认
证明过程设计可以在商业规模上一致地重复。
- 设备和设施确认(IQ/OQ/PQ)
- 过程性能确认(PPQ)批次
- 建立初始能力指数
- 确认控制策略有效性
第三阶段
持续过程验证
持续保证过程在例行商业生产中保持受控状态。
- 持续 CPP/CQA 监控和趋势分析
- 统计过程控制(SPC)制图
- Nelson 规则违规检测
- 能力指数(Cp、Cpk、Pp、Ppk)跟踪
- 过程漂移自动警报
- 馈入 APQR 进行全面质量审查
制药生产 CPV 软件
持续过程验证软件,具备实时过程性能监控、自动统计分析和检查就绪 CPV 报告功能
实时数据摄取
生产过程监控软件,能够自动从 LIMS、MES、ERP 和仪器中提取数据。所有 CPP 和 CQA 数据的单一真实来源,具备验证和审计追踪功能。
自动化 SPC 制图
为每个受监控参数自动生成控制图、趋势线和能力分析,无需手动干预。
智能警报
可配置的过程漂移、Nelson 规则违规和能力下降警报阈值,具备升级工作流程功能。
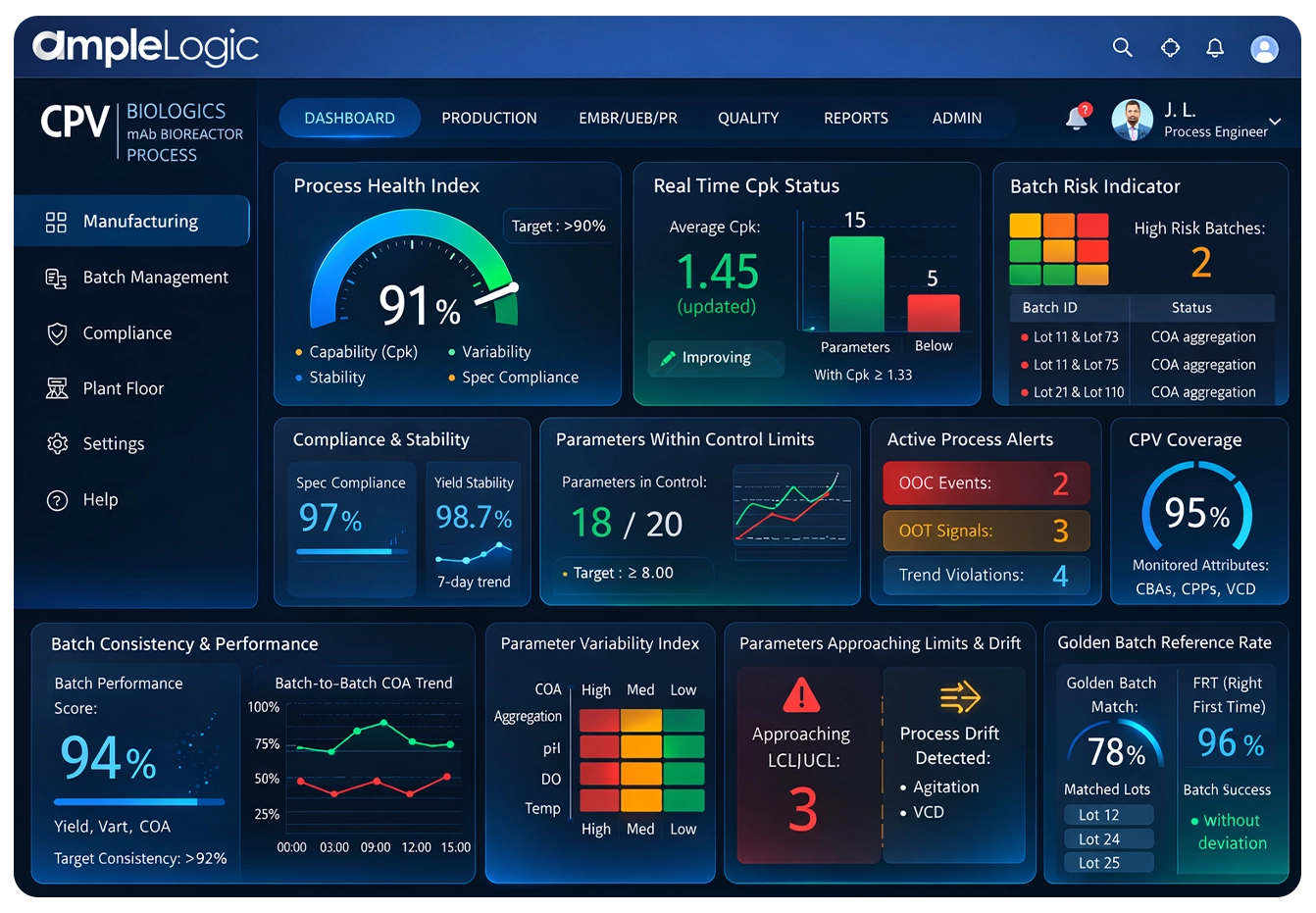
CPV 仪表板与批次过程监控
集中式实时批次过程监控系统,显示所有产品、参数和站点的过程状况,并具备向下钻取功能。
报告自动化
自动生成包含嵌入图表、统计摘要和结论的 CPV 报告。面向制药生产的 CPV 软件,带有用于法规提交的预格式化模板。
APQR 集成
CPV 监控数据无缝流入 APQR 工作流程。第三阶段证据自动填充年度产品质量审查。
持续过程验证的实时 CPP 和 CQA 监控
对每个批次的关键过程参数和质量属性进行全面监控
关键过程参数(CPP)
- 温度曲线和保温时间
- 混合速度和持续时间
- 压缩力和片剂硬度
- 干燥终点和水分含量
- 制粒参数和粒径
- 包衣厚度和喷雾速率
关键质量属性(CQA)
- 含量测定和效价值
- 含量均匀度和混合均匀度
- 溶出曲线和释放速率
- 杂质水平和相关物质
- pH、粘度和粒径分布
- 无菌和内毒素水平
过程性能指标
- 批次收率和物料平衡
- 中间控制结果
- 周期时间和吞吐量
- 环境监测数据
- 设备性能指标
- 供应链和原材料数据
逐批次趋势分析
过程性能监控软件,为所有受监控参数的 CPP、CQA、生产收率和包装收率生成逐批次趋势。
自动警报系统
可配置的 OOS、OOT 和过程漂移警报,自动升级至 QA 和生产团队。
黄金批次基准
识别和对标黄金批次进行比较,实现一流生产性能跟踪。
多产品监控
同时监控多个产品的 CPP 和 CQA,提供汇总视图和单独视图。
AmpleLogic CPV 用于 GMP 生产的统计过程控制(SPC)工具
为每个 CPP 和 CQA 自动生成控制图、能力指数和高级统计分析
控制图(I-MR、X-bar R)
为每个 CPP/CQA 自动生成 I 图、移动极差图、X-bar 图和 R 图,包含控制限、规格限和中心线。
能力指数
自动计算 Cp、Cpk、Pp、Ppk 和过程西格玛。随时间追踪能力趋势,及早检测下降。
六合一报告
综合六合一报告,结合 I 图、移动极差图、直方图、正态概率图和能力分析。
Nelson 规则检测
自动检测所有 8 条 Nelson 规则违规。标记的违规触发调查工作流程和纠正措施。
基于 R 的统计引擎
内置 R 统计引擎,用于高级分析,包括方差分析、回归、多变量分析和自定义统计检验。
单变量与多变量分析
支持单变量和多变量过程分析。检测 CPP 和 CQA 之间的相关性,加深过程理解。
CPV 的 AI 驱动过程智能平台
预测分析、异常检测和自动化洞察,实现主动过程控制
预测过程分析
AI 模型分析历史批次数据,在影响产品质量之前预测过程漂移。对能力下降的早期预警。
自动趋势解释
AI 生成的摘要解释统计趋势,识别根本原因,并为过程偏差推荐纠正措施。
OCR 数据提取
从扫描文件、手写记录本和遗留纸质记录中提取数据。自动化数据录入并确保一致性。
AI 聊天机器人用于过程洞察
通过自然语言交互查询历史过程数据、询问趋势并获得过程性能的即时答案。
异常检测
机器学习算法检测传统统计方法可能遗漏的过程数据中的异常模式。减少假阴性。
自动报告叙述
AI 为 CPV 报告生成逐章节摘要和结论,将手动叙述写作减少 90%。
CPV 软件与 APQR、LIMS、eQMS、eBMR 和企业应用的集成
CPV 数据在所有质量和生产系统之间无缝流转
APQR
将 CPV 数据直接馈入 APQR 工作流程和报告
eQMS
与 CPV 发现关联的偏差、CAPA、OOS/OOT
LIMS
分析结果、稳定性数据和实验室事件
eBMR
过程中数据、批次记录和收率数据
DMS
SOP、规程和验证文件
eLOG
设备、区域和过程记录本数据
CAPS
仪器校准和设备维护状态
CVS
清洁验证和确认数据
ERP
原材料数据和供应链可追溯性
RIMS
法规提交和合规数据
数字化 CPV 软件用于制药质量监控的优势
通过自动化生产过程监控软件实现主动质量控制、更快审查和审计准备就绪
主动质量控制
在导致批次失败之前检测过程漂移。持续过程验证软件用于主动生产质量监控和管理。
工作量减少 75%
自动化数据收集、图表生成和报告写作。让 QA 团队专注于调查和改进。
实时过程可视性
实时仪表板显示所有产品和站点的过程状况。从概览向下钻取到单个参数图表。
消除手动 Minitab
用自动化、可审计且始终最新的统计分析替代手动 CSV 导出和 Minitab 制图。
无缝 APQR 集成
CPV 发现自动馈入年度产品质量审查。第三阶段和 APQR 之间的数据和方法一致。
更快批次放行
实时监控和自动化审查实现更快的批次处置。显著缩短审查到放行的周期时间。
审计就绪文档
不可变审计追踪、电子签名和预格式化报告确保随时处于检查准备就绪状态。
多站点协调
在所有生产站点标准化 CPV 方法和报告。在本地灵活性的基础上实现全球一致性。
多站点 CPV/OPV 实施,具备自动趋势分析、统计分析和无缝 APQR 集成功能。协调全球模板,同时支持站点特定的数据模型、工作流程和法规要求。
在各生产站点实施数字化 CPV,具备自动统计分析、实时仪表板和集成 APQR 报告功能。采用与客户 SOP 和法规期望对齐的动态模板。
专为全球 GxP 法规合规构建的 CPV 软件
针对 FDA、EMA、MHRA、WHO 和 ICH 要求的预构建控制和文档
FDA 过程验证指南
完全符合 FDA 2011 年过程验证指南,涵盖第三阶段持续过程验证要求。
ICH Q8 / Q9 / Q10
符合 ICH 制药开发、质量风险管理和制药质量体系指南。
EU GMP 附件 15
符合 EU 确认和验证要求,包括持续过程验证。
21 CFR 第 11 部分
电子记录和签名、审计追踪、访问控制和全面的数据完整性保障。
MHRA 数据完整性
ALCOA+ 原则贯穿所有数据收集、存储和报告活动。
WHO 技术报告系列
符合 WHO 制药生产中过程验证和持续过程验证的指南。
为何选择 AmpleLogic CPV 软件进行持续过程验证
统一的 APQR + CPV 平台
生命周期过程验证软件,为年度产品质量审查和持续过程验证提供单一平台,共享数据和分析。
符合主要监管机构要求
针对 USFDA、EMA、MHRA、WHO 和 ICH Q8-10 验证要求的预构建控制和文档。
部署速度提升 10 倍
预验证模板和可配置工作流程将部署时间从数月缩短到数周。
200+ 人专业团队
专注于集成、验证、实施和持续产品更新的专属资源。
持续产品升级
定期更新,包含验证就绪的变更控制、新统计方法和增强的 AI 能力。
我们服务的行业
受制药、生物技术、API 制造商、CDMO 等行业的广泛信赖
制药
面向药品生产的 GMP 合规过程验证软件,具备 CPP/CQA 趋势分析和批次分析功能
生物技术
生物制品和生物类似药 CPV,具备复杂分析趋势和过程表征功能
API 制造商
活性药物成分 CPV,具备过程能力跟踪和杂质趋势功能
CDMO
多客户 CPV 管理,具备产品特定监控和报告模板
生命科学
QC 实验室持续过程验证软件,具备高级多变量分析和用于研发及商业生产的过程优化功能
CRO
合同研究 CPV,具备多客户数据管理和分析趋势功能
医疗器械
设备生产 CPV,具备性能趋势和设计控制集成功能
食品与饮料
食品加工 CPV,具备安全参数监控和 HACCP 合规功能
引领生命科学前沿
获取最新产品更新、合规动态及行业洞察,直接发送至您的邮箱。