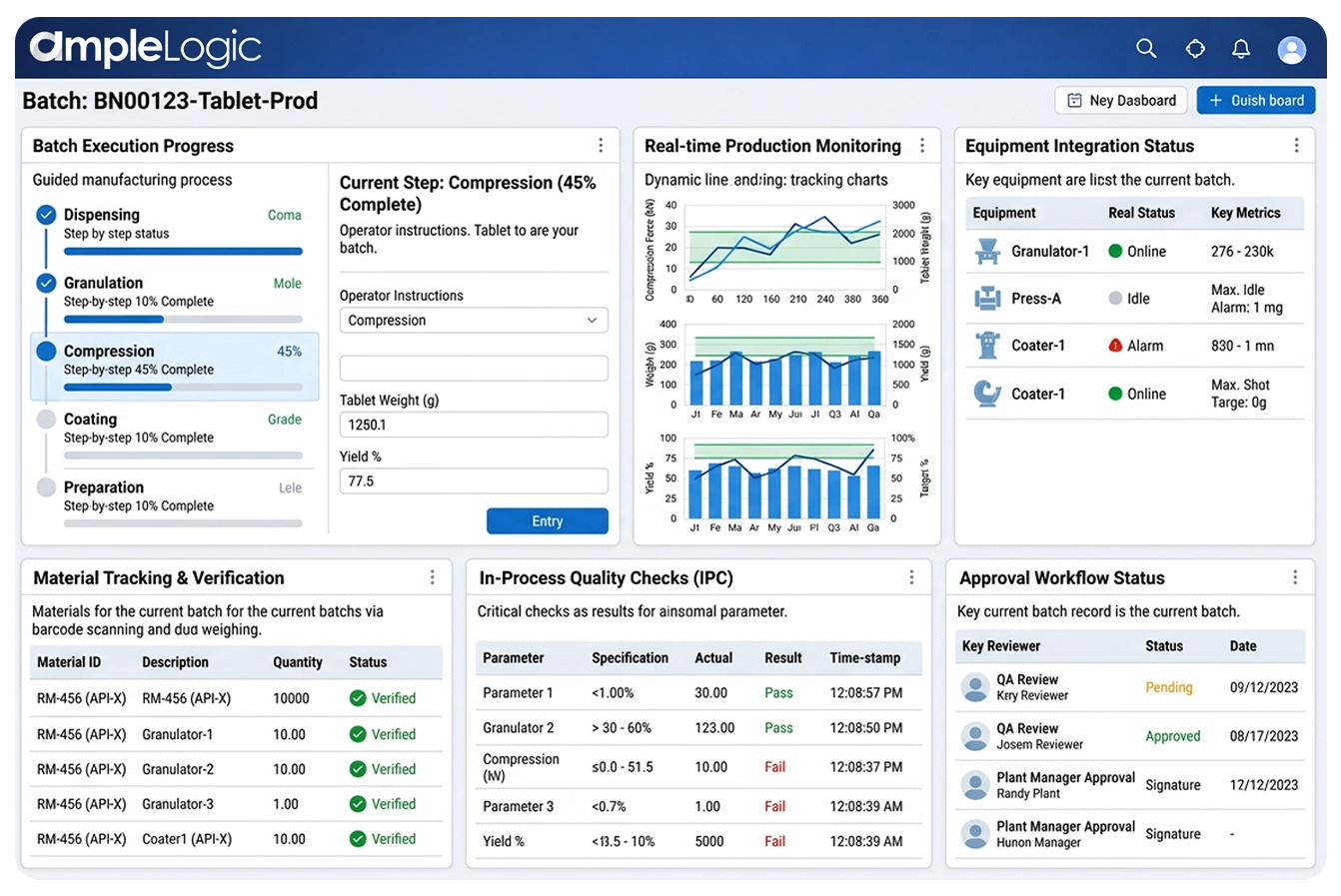
为何纸质批次记录阻碍了制药生产合规
手动批次记录和遗留 MES 系统在整个生产操作中造成系统性 GMP 风险——从合规风险到生产延误。
人为错误和操纵风险
手动纸质记录容易出现转录错误、遗漏条目和数据操纵——制药 MES 软件和电子批次生产消除了这些风险,通过批次生产自动化实现。
批次数据易出错
纸质记录的产品和批次数据缺乏实时生产监控,导致规格失败和返工,而制药生产软件可以防止这种情况。
缺乏实时可视性
基于纸张的系统无法提供实时生产状态——带有实时生产监控和 EE 监控的数字制造平台取代了延迟报告和现场巡视。
审计和检查困难
在 FDA/MHRA 检查期间检索、编制和核实纸质记录耗时费力——符合 GxP 的 MES 和 GMP 制造软件确保即时审计准备就绪。
合规与安全漏洞
纸质记录缺乏 21 CFR 第 11 部分所要求的强健访问控制、防篡改审计追踪和电子签名——这个生命科学 MES 平台弥补了所有合规差距。
协作受限和延误
部门间顺序纸质交接减慢了批次执行——自动化制药法规工作流程和车间执行系统能力消除了瓶颈。
物料追踪不可靠
手动物料记录导致差异——带有条形码验证的称量衡器集成确保准确的配料记录和收率对账。
标准维护困难
保持纸质 SOP 和主记录的现行性在操作上成本高昂——低代码制造应用的配方管理简化了跨产品和站点的更新。
完整的电子批次生产记录和 MES——一个 GMP 合规平台
从主批次配方创建到批次执行、质量检查和放行——每个 eBMR 模块在单一 GMP 数据层上协同工作。
执行与实时生产监控
车间执行系统,具备实时生产监控、逐步引导流程、实时生产仪表板、EE 监控和从设备自动数据采集功能,基于此制药 MES 软件。
企业级制药生产执行能力
生产监控、设备集成和 GMP 合规工作流程——无纸化制药生产现场所需的每项能力。
实时数据采集与生产监控
制药 MES 软件,具备从设备、PLC 和仪器自动数据采集功能——实时生产监控和 EE 监控消除了此数字制造平台上的手动转录。
设备集成(PLC/HMI/SCADA)
车间执行系统,通过 OPC、历史数据库和标准 PLC 协议直接集成,在此智能工厂平台上获取实时过程数据。
电子签名与审计追踪
符合 GxP 的 MES,具备符合 21 CFR 第 11 部分的电子签名、不可变的时间戳审计追踪,记录此 GMP 制造软件中的每个操作、变更和审批。
自动化工作流程管理
批次生产自动化,具备可配置的多级审批工作流程、自动路由、升级和在此制药生产软件上的并行/顺序处理。
基于例外的审查
AI 驱动的制造洞察,仅突出显示例外情况和偏差供 QA 审查,大幅加速此生命科学 MES 平台上的批次放行。
提醒与升级警报
云 MES 平台,具备针对待处理任务、批次审批阶段、逾期活动和管理升级的自动电子邮件警报。
产品标签管理
数字制造平台,具备集中标签管理,确保所有产品标签的一致性、版本控制和法规合规。
包装组件
制药生产软件,具备可配置物料清单、组件追踪和对账功能,处理每个产品的多样化包装需求。
低代码制造应用
低代码制造应用,具备直观的拖放界面用于定制流程——实现无需自定义编码的制药生产数字化。
高级生产计划
智能工厂平台,具备工业 4.0 制造计划算法,优化资源分配、最小化换产时间并最大化吞吐量。
可扩展的云 MES 平台
云 MES 平台,100% 可定制——可从单一生产线扩展到企业级多站点部署,满足生物制药生产平台需求。
完整生产生命周期可视性
数字制造转型,在整个生产生命周期(从计划到批次放行和归档)实现端到端可视性和控制。
药品批次放行简化
结构化的端到端 eBMR 流程,引导您的制药生产过程从配方创建到最终批次审批。
主数据设置
- 创建主数据(产品、物料、设备、房间)
- 产品和阶段映射
- 原材料与产品的映射
- 房间和设备映射
- 顺序和并行流程定义
配方与计划
- 主配方创建(拖放方式)
- 生产计划与资源分配
- 批次计划和发放
批次执行
- 带条形码验证的原材料配料
- 逐步引导批次执行
- 设备集成和自动数据采集
- 过程中质量检查和检验结果
- 房间和设备记录条目
审查与放行
- 例外处理和偏差管理
- 电子签名和多级审批
- 基于例外的审查以加快批次放行
- 完整审计追踪和批次谱系
分步迁移:从纸质到完整 eBMR
BIMS(批次记录发放管理)
- 主副本版本管理和文档发放
- 自动打印以消除手动错误
- 母批次、协同包装和双层逻辑
- 数量管理(借记和贷记)
- 控制手动记录错误、附加页面请求和批准
电子批次记录
- 发放流程转换为在线工作流程
- 在线记录批次信息(从纸质移至电子)
- 确认记录仅在设备处完成的措施
- 与 eQMS 系统集成
完整 eBMR
- 从手动记录转变为从设备自动填充数据
- 与 PLC、HMI 和 SCADA 的实时数据集成
- 完整的无纸化生产现场
- 完整的 21 CFR 第 11 部分 / EU 附件 11 合规
通过电子批次记录简化制药车间执行
专为 GMP 生产现场的制药操作员打造——100% 合规,自动验证。
引导流程
车间执行系统,具备用户友好的逐步指令用于执行生产步骤——操作员遵循直观的提示确保在此制药 MES 软件上的一致性。
实时生产监控
实时生产监控,具备动态视觉提示和状态图标,帮助操作员在此数字制造平台上通过 EE 监控一眼了解当前活动状态。
自动验证
批次生产自动化,具备针对错误输入、规格外值和遗漏步骤的系统警告,在错误到达电子批次生产记录之前予以预防。
屏幕显示 SOP
GMP 制造软件,在使用点直接在屏幕上显示标准操作规程,供执行期间即时参考。
活动指引与下一步
智能工厂平台,为每项任务的下一步提供明确指示,确保操作员在此生命科学 MES 平台上始终知道过程中的下一步是什么。
条形码与 QR 扫描
称量衡器集成,以及集成的条形码/QR 扫描,用于物料验证、设备识别和工业 4.0 制造车间的防错数据录入。
在整个制药操作中无缝集成 eBMR/MES
跨质量、实验室、培训、设备和企业系统的原生 eBMR/MES 集成——全部在一个符合 21 CFR 第 11 部分的平台上。
质量系统
- eQMS(CAPA、偏差、变更控制)
- OOS/OOT 管理
- 审计管理
- 投诉处理
实验室
- LIMS(过程中检验、CoA)
- 稳定性研究
- 环境监测(EMS)
文档与培训
- DMS(SOP、主记录)
- LMS(操作员培训、能力)
- 电子记录本(eLogs)
设备与自动化
- PLC / HMI / SCADA 集成
- OPC 服务器连接
- 历史数据库
- 称量和配料系统
企业系统
- SAP / Oracle ERP
- 仓库管理(WMS)
- 供应链管理
- 财务系统
校准与维护
- CAPS(校准计划)
- 预防性维护
- 设备确认
- 资产生命周期
AmpleLogic eBMR/MES 与传统制药 MES 解决方案的比较
了解 AmpleLogic eBMR 与传统、企业级和以自动化为核心的制药 MES 解决方案相比如何。
| 功能 | AmpleLogic | 云 MES | 企业 MES | 自动化 MES |
|---|---|---|---|---|
| 部署速度 | 数周(低代码 aPaaS) | 数月(云 SaaS) | 6-18 个月(本地/云) | 6-12 个月(本地/云) |
| 定制化 | 100% 拖放,无需编码 | 基于模板的配置 | 需要专业服务 | 需要系统集成商 |
| 配方管理 | 可视化拖放构建器 | 基于模板的 EBR | 配方驱动的 ISA-88 引擎 | 配方管理模块 |
| 设备集成 | PLC/HMI/SCADA 通过 OPC | 有限(以 QMS 为主) | 深度 ISA-95 / OPC-UA | 供应商锁定的 PLC 生态系统 |
| 质量系统集成 | 原生(同一平台) | 原生 QMS + EBR | 第三方集成 | 第三方集成 |
| 统一平台 | 单一 aPaaS 上的 14+ 应用 | 仅 QMS + 生产 | 仅 MES(封闭生态系统) | 仅 MES(供应商生态系统) |
| 基础设施成本 | 降低最多 70%(开源) | 云订阅模式 | 高(企业许可证) | 高(平台 + 集成商) |
| 持续产品升级 | 包含,定期发布 | 云自动更新 | 版本升级(基于项目) | 主要版本发布 |
通过低代码实现 100% 可定制
低代码制造应用——每个工作流程、表单和流程均可完全配置以匹配您的确切生产要求,无需在此制药 MES 软件上进行自定义编码。
拖放式配方构建器
配方管理,具备可视化配方创建工具,让工艺工程师无需 IT 参与即可在此数字制造平台上构建和修改主配方。
持续升级的云 MES 平台
云 MES 平台,定期发布新版本、新功能、法规更新和性能改进——包含在您的订阅中,实现数字制造转型。
更快部署实现工业 4.0
智能工厂平台和生命科学 MES 平台,实现数周内部署——而非传统 MES 实施通常需要的 6-18 个月——加速制药生产数字化。
无纸化制药生产的商业案例
量化成果——部署 AmpleLogic 电子批次生产记录软件后加速批次放行、降低纸张成本并提高生产准确性。
批次放行速度提升
基于例外的审查和自动化工作流程将批次放行时间缩短了一半,相比基于纸张的流程。
纸张成本降低
消除整个生产操作中的纸质批次记录、打印、存储和检索成本。
数据录入错误减少
自动验证、设备集成和引导流程几乎完全消除了手动转录错误。
基础设施成本降低
开源基础设施堆栈(Linux、PostgreSQL)显著降低了 IT 基础设施支出。
投资回报率
客户通常在部署后 18 个月内通过运营效率实现 3-5 倍的 ROI。
审计准备速度提升
即时访问具有完整审计追踪的不可变电子记录,加快检查准备速度。
eBMR/MES 符合 16+ 个全球制药监管机构的要求
从第一天起就为制药法规合规而构建——FDA 21 CFR 第 11 部分、EU 附件 11、GAMP 5 等。
合规标准
监管机构
USFDA
美国
MHRA
英国
TGA
澳大利亚
CDSCO
印度
Health Canada
加拿大
MCC
南非
ANVISA
巴西
EMEA
欧盟
SFDA
中国
MPA
瑞典
Swissmedic
瑞士
MCAZ
津巴布韦
MEDSAFE
新西兰
MHLW
日本
NAFDAC
尼日利亚
KFDA
韩国
专为受监管制造业打造
制药生产
- 口服固体制剂
- 液体和半固体
- 无菌注射剂
- API 生产
- 制药生产数字化
生物制药生产平台
- 生物制品生产
- 细胞培养
- 纯化
- 灌装与封口
- 生物技术制造执行
医疗器械
- 器械组装
- 包装与标签
- 灭菌记录
- DHR 管理
CDMO / CMO
- 多客户批次记录
- 批量生产
- 技术转让
- 快速站点上线
- 数字制造转型
引领生命科学前沿
获取最新产品更新、合规动态及行业洞察,直接发送至您的邮箱。