RIMS挑战:为何手动法规管理难以为继
阻碍合规、申报和市场准入的关键挑战
不断变化的全球法规
跟踪FDA、EMA、MHRA、CDSCO、WHO、Health Canada、TGA等100多个区域监管机构的最新动态,需要持续关注并快速适应。
法规数据分散
关键法规信息分散在电子邮件、电子表格、共享驱动器和遗留系统中,形成监管盲区和合规漏洞。
复杂的申报格式
跨不同地区管理eCTD、ACTD、NeeS及纸质申报,需要专业知识和容易出错的人工协调。
可见性和追踪不足
缺乏统一仪表盘,无法实时监控各市场全球申报、审批、问询和续期的状态。
人工且容易出错的流程
过度依赖电子邮件沟通、手动数据录入和分散的电子表格,增加了错过截止日期和受到法规处罚的风险。
系统集成挑战
QMS、DMS、ERP和安全系统的割裂导致数据重复、不一致,以及跨职能法规工作流程迟缓。
可扩展性问题
跨地区不断增长的产品组合以指数级方式增加法规复杂性,使手动追踪方式不堪重负。
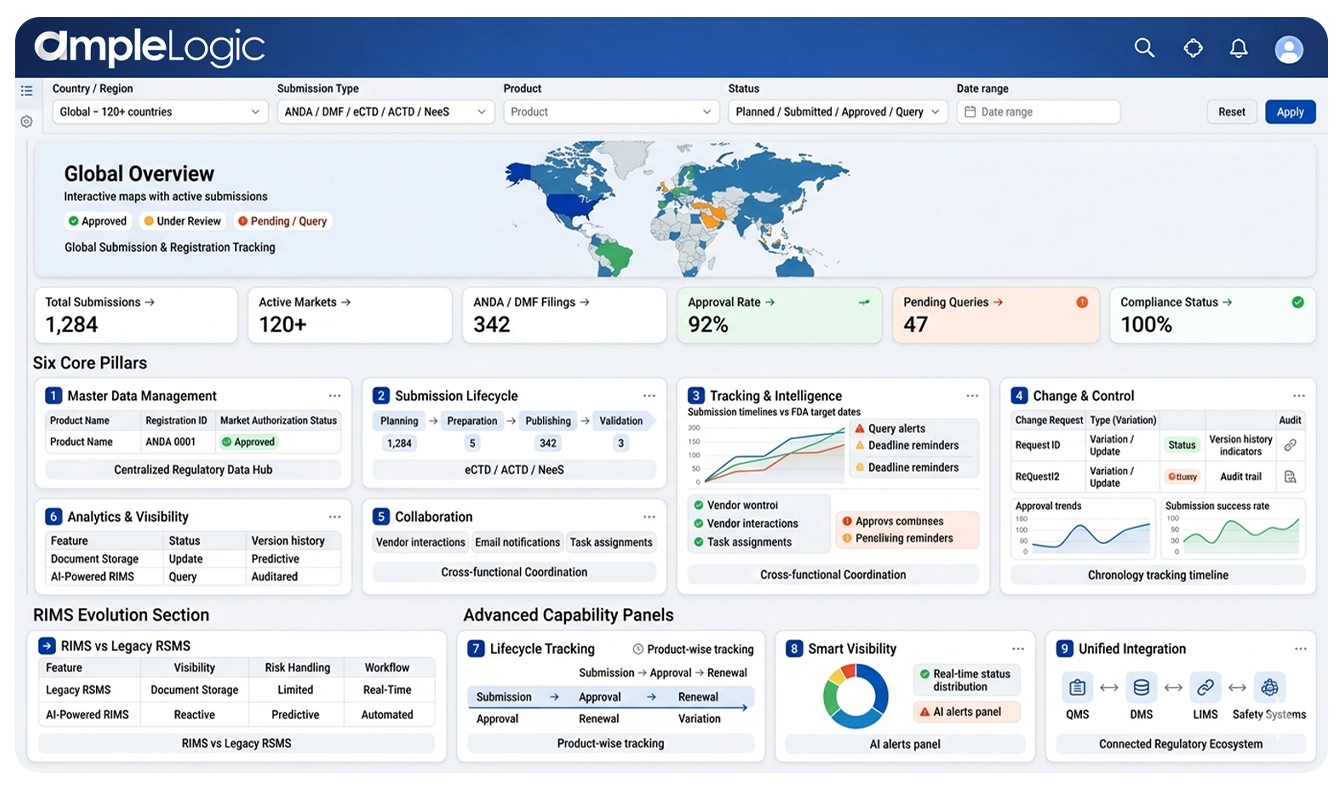
AmpleLogic RIMS软件概述
支持端到端法规全生命周期管理的六大支柱
主数据管理
集中化产品注册、全球市场授权及跨所有监管机构的全生命周期追踪。
申报全生命周期
用于规划、准备、发布和验证eCTD、ACTD及NeeS申报的自动化工作流程,支持ANDA和DMF追踪。
追踪与智能分析
实时申报状态、审批与问询管理、FDA目标日期,以及对所有市场截止日期的主动监控。
变更与控制
变更控制、变更管理和持续改进流程(CIP),具备完整审计跟踪和版本历史。
协作
供应商协调、客户通知和自动电子邮件提醒,确保跨职能法规工作流程顺畅运行。
分析与可视化
图形化仪表盘、时间轴追踪、生命周期分析及合规就绪情报,支持明智的法规决策。
RIMS:RSMS的下一代演进
传统RSMS平台只是被动的文档存储库,而RIMS是智能化、AI驱动的法规管理生态系统,能够主动推动合规、预测风险并加速产品上市。
数据管理
在具有主数据治理和全生命周期追踪的集中化系统中,完整管理产品注册和全球法规数据。
全生命周期追踪
监控审批、变更和续期,确保所有市场持续符合法规要求。
智能可视化
通过智能提醒和合规仪表盘实现全球实时可见性和主动监控。
统一集成
与QMS、DMS、LIMS和安全系统无缝集成,构建统一的法规管理生态系统。
RIMS工作流程模块:申报全生命周期管理
八个相互关联的模块,引导法规流程从策略制定到持续合规
法规数据基础
全球市场设置和DMF、CEP、LOA及产品全生命周期追踪的主数据存储库,覆盖所有监管机构。
申报规划
全球法规申报的策略制定、时间管理、里程碑追踪和资源分配。
申报准备
用于eCTD/ACTD/NeeS就绪的档案汇编、版本控制和文件组装,配备自动化验证检查。
申报执行
向卫生机构进行验证、发布、网关提交、ANDA追踪及实时机构状态监控。
审查管理
跨所有市场的问询追踪、缺陷管理、机构沟通日志和回复时间监控。
药品全生命周期管理
变更、续期、批准后变更和标签更新,具备完整的全生命周期追踪和自动提醒。
合规监控
自动提醒、承诺追踪、检查就绪状态及主动法规变更情报。
分析与报告
实时仪表盘、图形报告、全球申报洞察及GDUFA/机构专项分析。

端到端编排
每个工作流程模块与QMS、DMS、LIMS和安全系统无缝集成,消除数据孤岛和整个法规生命周期中的手动交接。
AmpleLogic RIMS软件核心功能
推动法规卓越的十二项关键能力
产品注册追踪
跨120多个国家追踪产品注册,配备自动状态更新、截止日期提醒及完整药品全生命周期管理。
申报准备与发布
审批与拒绝监控
ANDA追踪器与FDA目标日期
DMF追踪器与变更控制
承诺与变更管理
供应商与利益相关方管理
图形报告与仪表盘
制药法规自动化工作流程
电子签名与审计跟踪
集中化文档存储库
申报验证引擎
AI驱动的RIMS:智能法规分析
加速法规工作流程并降低风险的六项AI驱动能力
AI合规追踪
持续监控并适应不断变化的地方和全球法规标准,自动更新流程以确保合规,无需人工干预。
预测性分析
分析历史和实时数据,在潜在风险和合规漏洞升级之前加以识别,帮助主动缓解问题并避免处罚。
自动化报告
AI自动生成法规报告和文件,确保其准确、及时、审计就绪,且只需最少的人工参与。
风险缓解引擎
AI算法评估数据模式,标记潜在合规风险,提供预测性洞察并推荐纠正措施。
法规变更情报
实时追踪和处理法规变更,自动将其纳入系统,确保持续符合最新标准。
工作流程优化
AI优化工作流程,降低运营成本,加速法规流程,并确保所有业务层面的一致合规。
全球法规追踪器:FDA、EMA及世界其他地区监控
三个区域追踪模块,实现全面的市场授权管理
美国FDA法规追踪器
ANDA追踪器和DMF追踪器,涵盖FDA生命周期里程碑,包括IND、NDA、ANDA、BLA目标行动日期、GDUFA费用及505(b)(2)申报。
欧盟及英国法规追踪器
管理EMA和MHRA程序、集中/分散/相互认可变更、PSUR时间表及脱欧后英国申报,配备自动化工作流程。
全球其他地区法规追踪器
简化亚太、拉丁美洲、中东北非及非洲地区申报,支持Health Canada、TGA、CDSCO、WHO PQ等100多个监管机构的国家专项全生命周期追踪。
RIMS合规:全球法规标准
全面支持全球法规框架和合规标准
主要监管机构支持
全面覆盖美国FDA、EMA、MHRA、WHO、Health Canada、TGA、CDSCO、ANVISA、PMDA及100多个全球卫生机构。
多区域格式管理
原生支持eCTD、ACTD、NeeS及纸质格式,配备自动续期监控和格式专项验证。
21 CFR Part 11与欧盟附录11
完全符合要求的控制措施,包括电子签名、审计跟踪、数据完整性保障和安全版本控制。
主动监控与提醒
针对截止日期、承诺到期日、续期窗口和法规变更的自动提醒,实时降低风险。
IDMP就绪
支持ISO IDMP标准,涵盖物质、产品、组织和参考数据,为EMA的识别要求做好准备。
ICH eCTD 4.0就绪
为下一代eCTD 4.0数据模型进行前瞻性布局,支持结构化内容规划、元数据管理和机构申报功能。
AmpleLogic RIMS与竞争对手对比
AmpleLogic如何超越传统RIMS和单点解决方案
| 功能 | AmpleLogic RIMS | 竞争对手 |
|---|---|---|
| 架构 | 统一aPaaS上的低代码/无代码 | 架构僵化,需要大量定制化 |
| 数据方式 | 统一主数据存储库 | 数据分散于各模块和数据孤岛 |
| 生命周期覆盖 | 端到端(从规划到批准后追踪) | 通常需要单独的附加模块 |
| 集成 | 无缝集成(QMS、DMS、ERP、安全系统、LIMS) | 独立系统,集成成本和工作量高 |
| 自动化与AI | AI驱动的提醒、预测分析、自动报告 | 自动化有限,工作流程静态且手动 |
| 总拥有成本 | 较低TCO,快速部署,按需付费 | 高额许可费和持续维护成本 |
| 部署速度 | 使用预验证模板,数周内完成 | 实施需数月乃至数年 |
| eCTD 4.0就绪 | 采用结构化数据模型进行前瞻性布局 | 依赖路线图,时间表不确定 |
RIMS企业集成
连接法规、质量和生产系统的十个集成模块
eQMS
双向变更控制、CAPA和偏差关联
DMS
版本受控的法规文件和SOP
LMS
培训记录和能力管理
LIMS
申报用分析数据和CoA集成
eLogbook
与法规记录关联的GxP日志本数据
eBMR/MES
用于法规申报的批记录数据
CVS
用于法规备案的清洁验证数据
CAPS
合规用设备校准记录
SAP/Oracle
物料主数据和供应链数据同步
PV
不良事件数据和PSUR/PBRER集成
RIMS投资回报:可量化的法规影响
AI辅助法规全生命周期管理的量化影响
申报准备
快50-60%手动流程
8-12周
使用AmpleLogic RIMS
3-5周
法规数据录入
减少75%手动流程
每周40+小时
使用AmpleLogic RIMS
每周8-10小时
截止日期合规
几乎零错过截止日期手动流程
按时率85-90%
使用AmpleLogic RIMS
按时率99%以上
问询响应时间
响应速度快70%手动流程
5-10个工作日
使用AmpleLogic RIMS
1-3个工作日
审计准备
节省90%时间手动流程
2-4周
使用AmpleLogic RIMS
数小时(随时就绪)
报告生成
快95%手动流程
每份报告3-5天
使用AmpleLogic RIMS
数分钟(自动生成)
入选Gartner报告
AmpleLogic RIMS已被认定为Gartner®生命科学法规信息管理解决方案市场指南中的代表性供应商,发布于2024年9月(ID G00769345)。
AmpleLogic RIMS服务的行业
八大行业垂直领域借助AmpleLogic RIMS实现法规卓越
制药
符合GMP的法规软件,用于药品注册、NDA/ANDA申报及全球市场授权,具备完整的全生命周期管理
生物技术
BLA申报、生物类似药注册及复杂生物产品的全生命周期管理
医疗器械
510(k)、PMA、CE标志、EUDAMED/UDI申报及器械分类管理
基因治疗
先进治疗产品的IND/BLA申报,具备专项法规路径追踪
API制造商
CEP申请的DMF追踪器及跨监管机构的全球API注册
食品与饮料
食品添加剂注册、新食品申请及健康声明申报
大麻与烟草
大麻许可证及烟草产品申报的专项法规追踪
化妆品
化妆品产品通知、CPNP/FDA注册及成分合规追踪
准备好变革您的法规运营了吗?
用AI驱动的、审计就绪的法规智能替代分散的电子表格和手动追踪。
引领生命科学前沿
获取最新产品更新、合规动态及行业洞察,直接发送至您的邮箱。