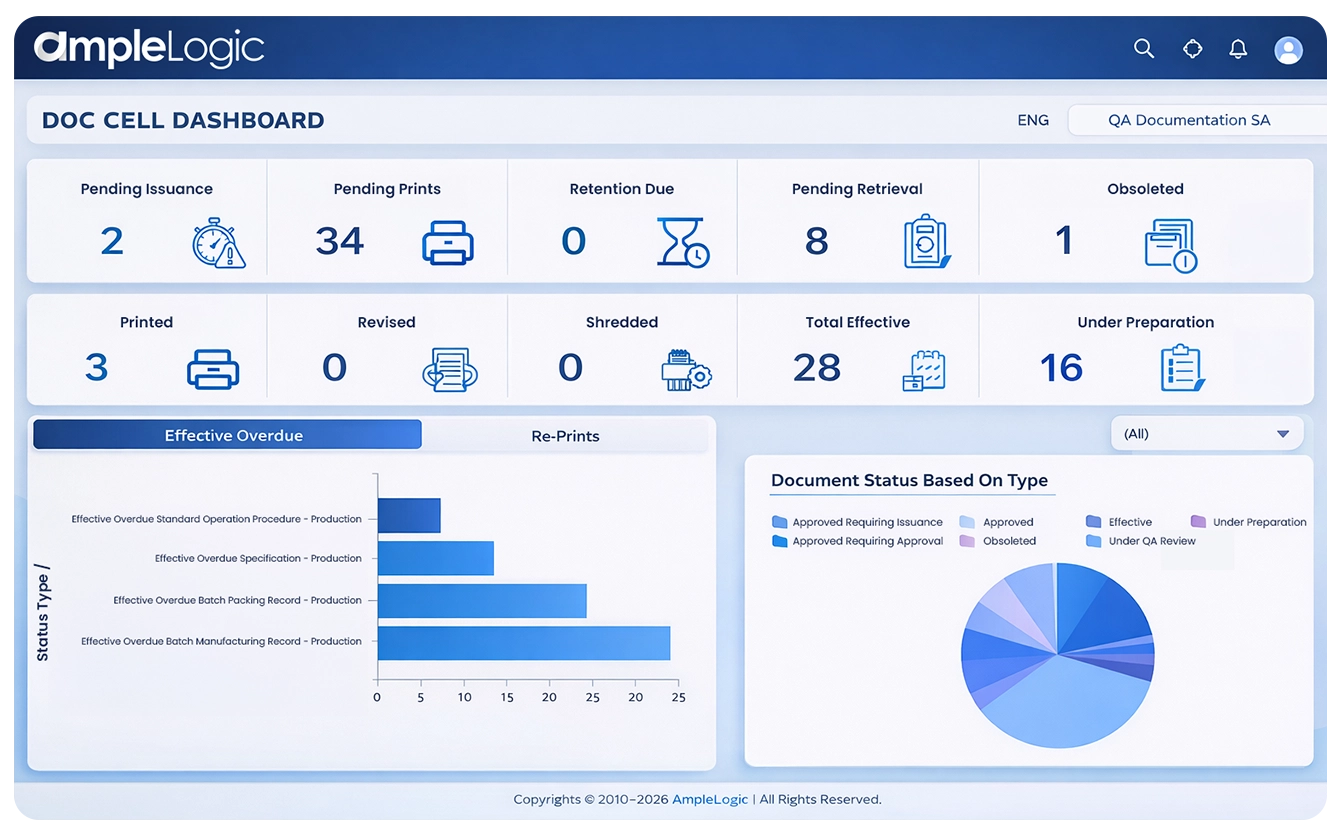
缺乏制药文档控制软件的关键 GMP 挑战
影响制药文档管理中合规性、效率和可追溯性的关键痛点
基于纸质或部分数字化的制药文档系统仍然普遍存在
没有合规文档管理系统,手动文档追踪每周消耗 15-20 小时,增加了错误和检索时间。
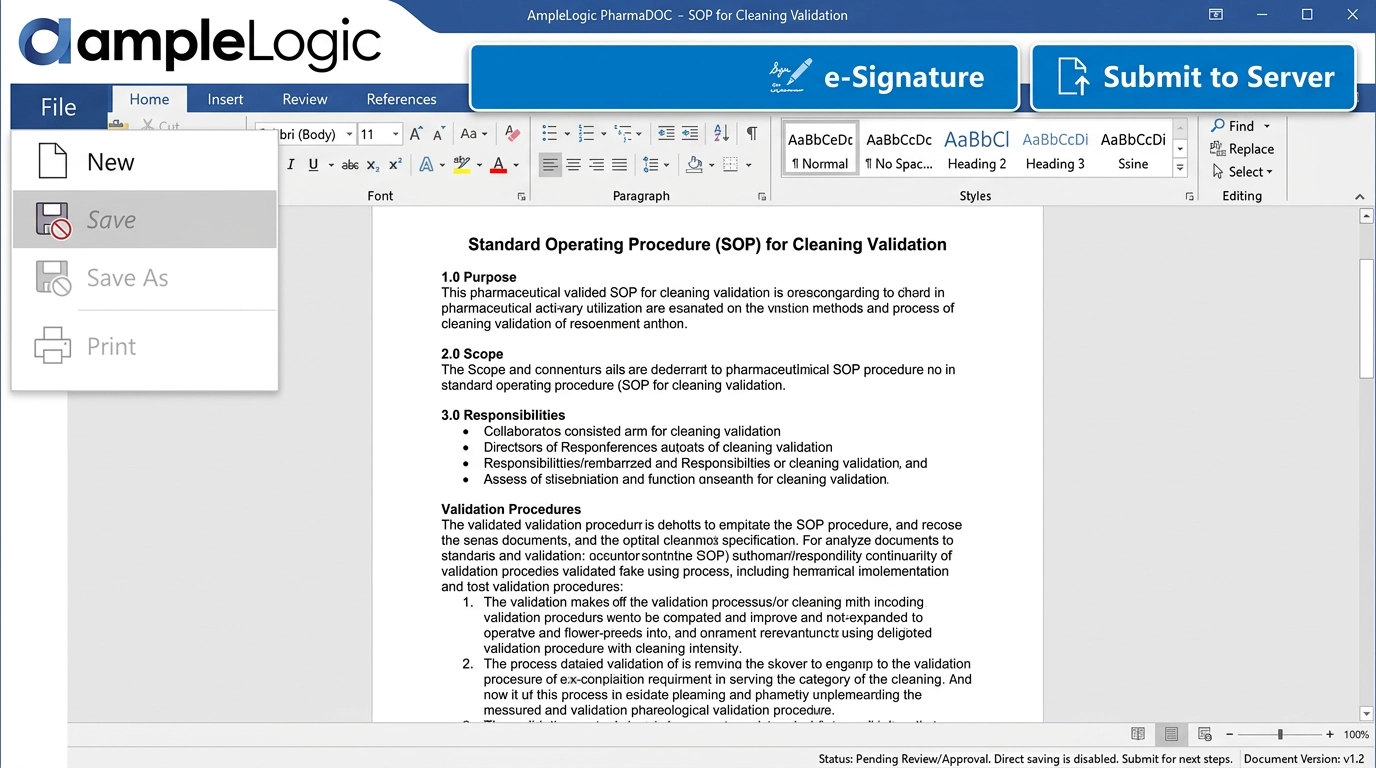
EDMS 功能缺口:SOP 版本控制薄弱且打印发放功能有限
由于缺乏文档版本控制软件,操作员使用过时的 SOP,导致审计发现和合规违规。
无基于条形码的文档追踪和替换管理薄弱
废弃文档继续流通,无受控副本追踪或自动撤销机制。
DMS 与 LMS、eQMS、LIMS 和 MES 系统的集成困难
系统断开破坏了可追溯性,增加了审计准备工作量和响应时间。
制药级 EDMS 必须满足的 GMP 合规要求
文档生命周期管理、法规合规、受控 SOP 管理和已验证自动化
文档生命周期管理
完整的文档生命周期管理软件,涵盖从起草到审查、审批、发布到归档,具备受控替换和废弃功能。
验证与控制
已验证的文档审批工作流程软件,具有映射到法规要求和数字文档控制系统能力的控制措施。
集成与自动化
无缝系统集成、高级搜索和 AI 驱动的自动化,减少手动协调工作。
21 CFR 第 11 部分和 EU 附件 11 法规合规
符合 FDA、EU 附件 11 和 GxP 文档管理系统要求的 21 CFR 第 11 部分合规文档管理系统,具有映射控制。
可追溯性和安全性
强健的文档版本控制软件、审计追踪、电子签名以及受控副本打印和检索追踪。
制药文档管理软件中管理的核心 GMP 文档类型
具备审计追踪和元数据的文档生命周期管理软件,实现 GMP 就绪
质量文档
- 带版本控制的标准操作规程(SOP)
- 带审批工作流程的变更控制记录
- 用于合规可追溯性的关联培训记录
- 废弃副本管理和替换控制
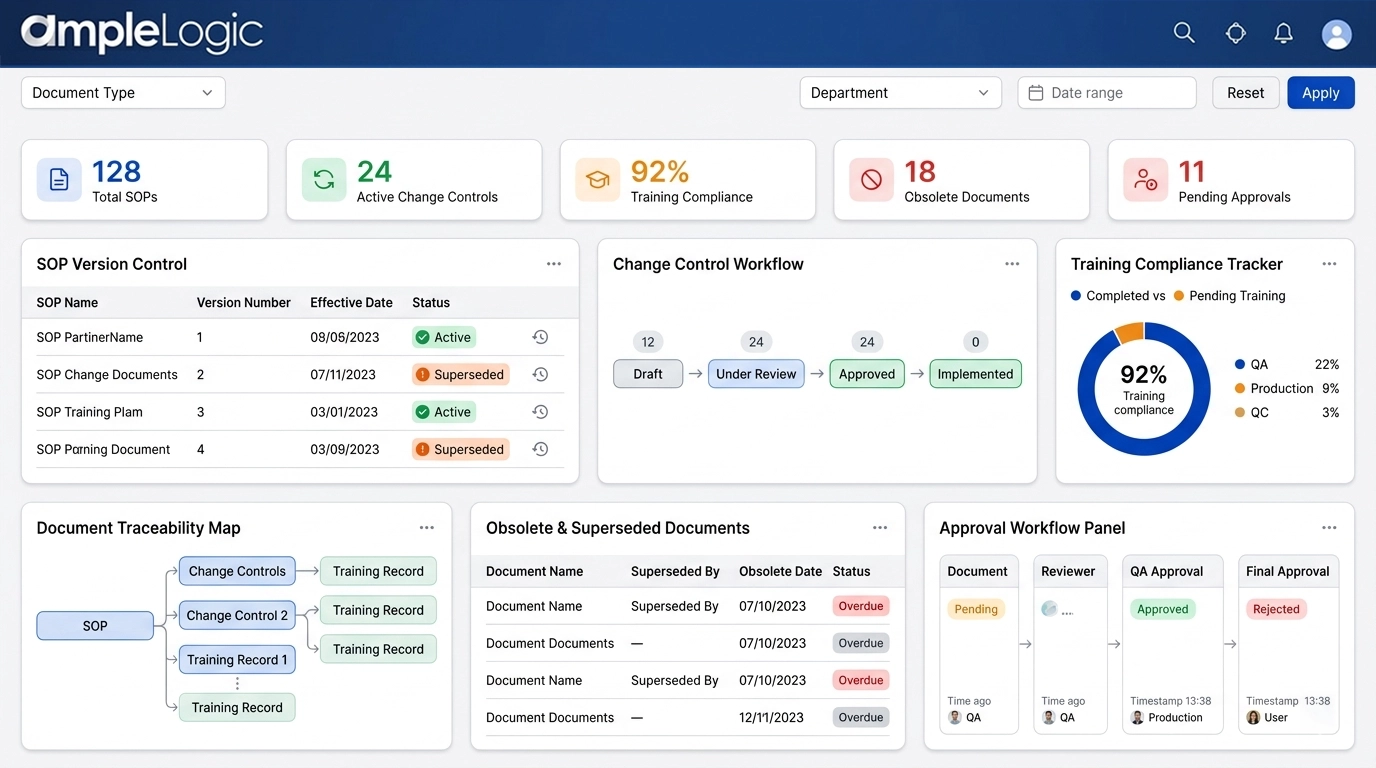
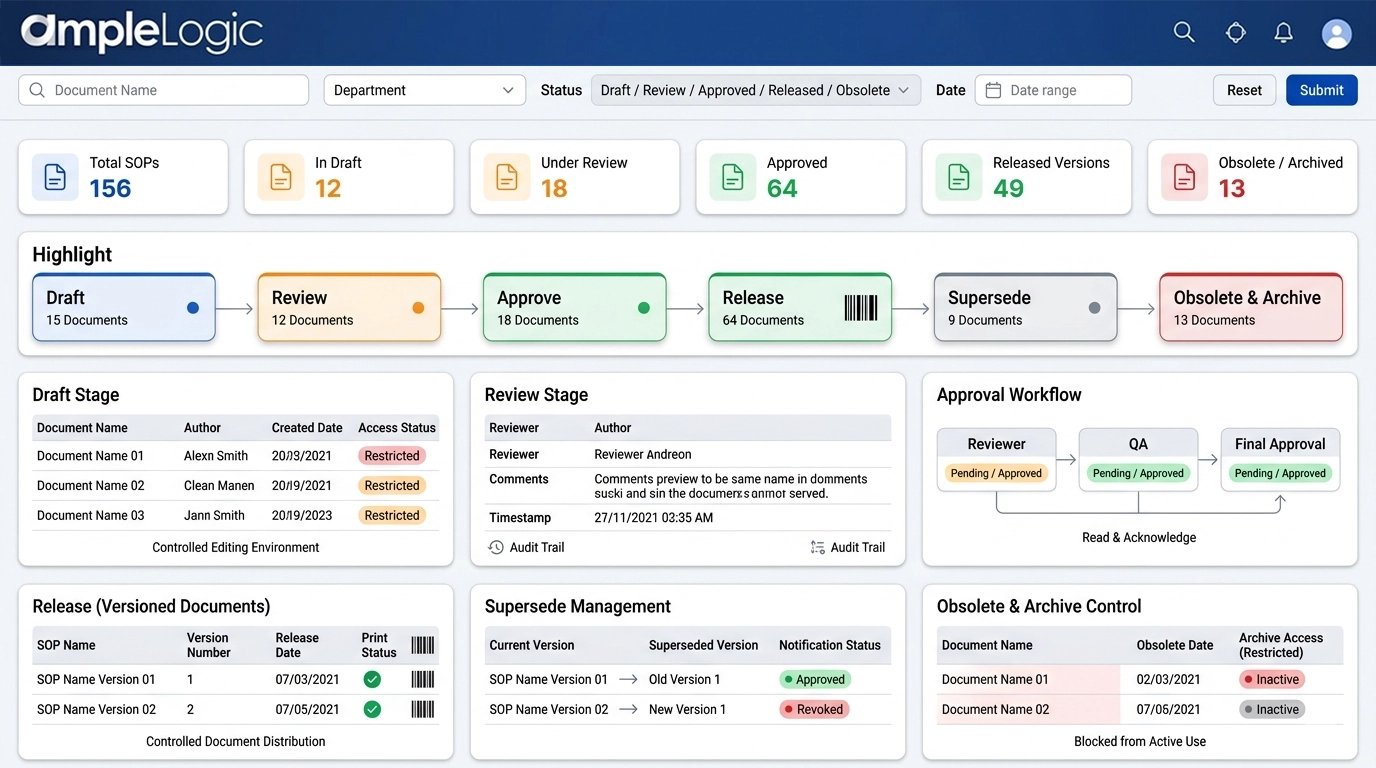
SOP 版本控制软件:替换、废弃副本和生命周期控制
确保只有当前文档驱动受监管过程,实现数字文档控制
草稿
具有明确草稿状态和受限访问的受控文档编辑。
审查
跨职能团队并行审查,具有带日期时间戳的完整审查者意见审计追踪。
审批
正式审批工作流程,具有强制执行的阅读和确认步骤。
发布(已版本化)
版本编号、打印管理和打印件条形码分配。
替换
自动替换旧版本并通知用户。
废弃和归档
明确撤销废弃文档、受控归档访问以及阻止在活跃过程中使用。
草稿
具有明确草稿状态和受限访问的受控文档编辑。
审查
跨职能团队并行审查,具有带日期时间戳的完整审查者意见审计追踪。
审批
正式审批工作流程,具有强制执行的阅读和确认步骤。
发布(已版本化)
版本编号、打印管理和打印件条形码分配。
替换
自动替换旧版本并通知用户。
废弃和归档
明确撤销废弃文档、受控归档访问以及阻止在活跃过程中使用。
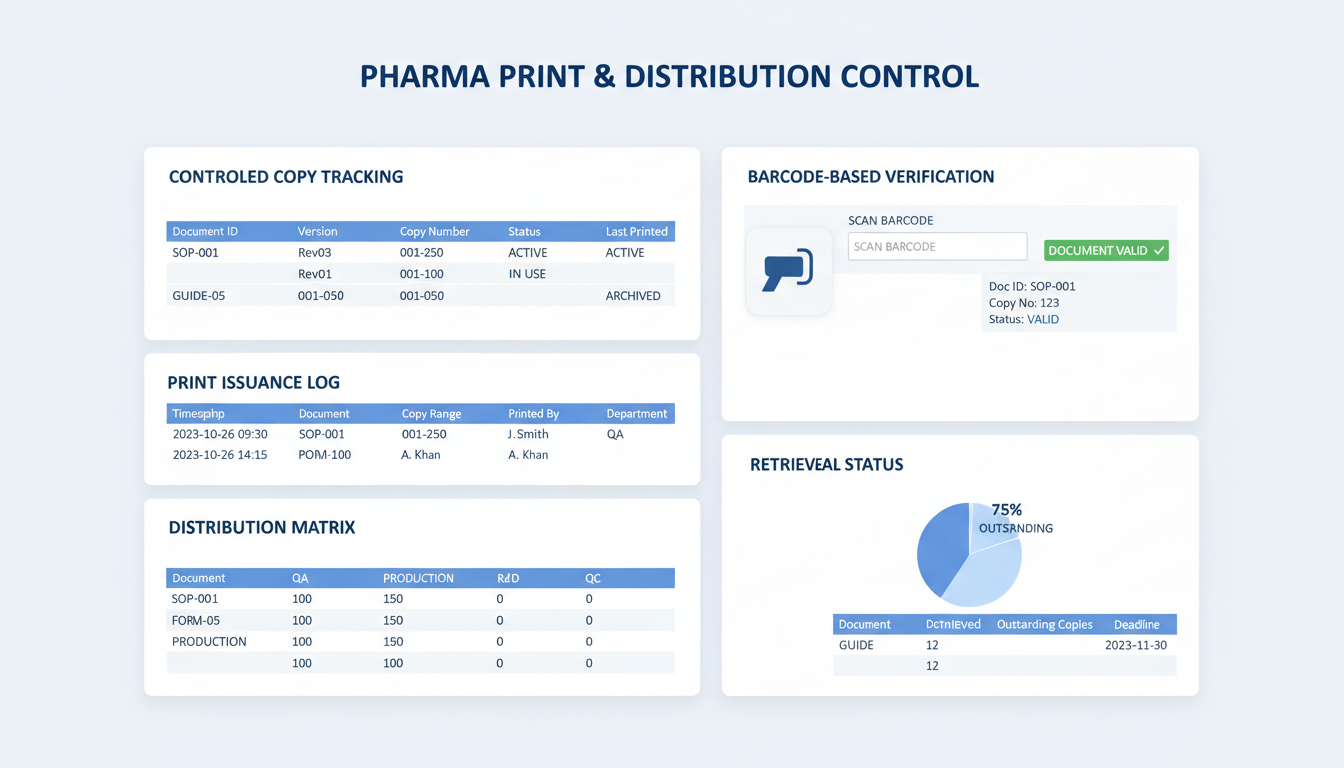
打印发放、受控副本分发和检索追踪
确保只有当前的、经授权的文档到达生产现场——包括非受控、培训和草稿副本
审批
通过文档审批工作流程软件完成带版本和审批元数据的文档定稿。
锁定版本
冻结已审批版本;使用数字文档控制系统保护措施防止编辑并标记替换状态。
打印发放
按角色/站点授予打印权限,生成受控副本、非受控副本、培训副本和草稿副本等水印。在各站点启用受控副本打印和检索。
分发
发布到受控站点和基于角色的列表,附带条形码标签和移交时的确认。
对账和审计追踪
追踪打印详情,并通过审计对已发放纸质副本进行核对,实现完整的制药文档控制系统可追溯性。
打印控制和验证
通过基于条形码的追踪弥合数字系统和实体现场副本之间的差距
动态条形码生成
为每个打印的实体副本自动生成水印和唯一条形码。
使用点验证
在生产现场进行实时条形码扫描,验证文档审批状态和版本。
全面打印审计
对已分发实体副本进行完整追踪,包括每用户打印日志和位置数据。
适用于 GxP 合规文档管理系统的智能 OCR 和 AI 搜索
使受监管文档在您的数字文档控制系统中可搜索、可审查和可访问
AI 驱动的 OCR
将扫描件和图像转换为可搜索、可编辑的文本。
减少手动转录,实现更快的检索。
智能搜索
以上下文相关性呈现受监管内容。
提高跨文档库的检索准确性。
语音激活搜索
加快免提检索和审查。
在审计和团队工作流程中更快访问。
电子取证和审计支持
支持更快的文档审查、证据检索和审计响应。
辅助合规、可追溯性和受监管审计。
全团队可访问性
为各职能部门提供对受控文档的一致访问。
在受监管环境中实现可追溯性和协作。
与 eQMS、LMS、LIMS 和 MES 的 GMP 合规 DMS 集成
与您的企业 GxP 文档管理系统生态系统无缝连接,实现端到端文档可追溯性
LMS
来自新 SOP 引入、版本变更的培训需求。培训完成检查。
eQMS
来自变更控制、审计发现、CAPA 的版本变更。
RIMS
来自法规发现的版本变更。
LIMS
带实验室结果和记录的检验方法和 STP。
电子记录本
记录本模板参考。
清洁验证
清洁规程的 SOP 访问。
eBMR/MES
BMR/BPR 文档管理和访问。
CAPS
用于校准规程的设备手册/SOP。
SAP
企业资源规划集成。
UMS
用户管理系统集成。
AmpleLogic 低代码 DMS 平台优势和 AI 赋能价值
面向生命科学的低代码灵活性、合规就绪性和受控自动化
LCNC 拖放设计器
可视化构建器减少自定义代码,加速交付,实现快速应用组合。
制药云文档管理
面向制药的云文档管理软件,具有加速时间表和快速业务影响——最短 3 个月内实现 ROI。
受监管行业文档管理
面向受监管行业的文档管理软件,专为文档记录和审计设计。符合 USFDA、MHRA、ISO 要求。
18+ COTS 应用程序
面向常见生命科学工作流程的预构建应用程序——随时可部署。
超过 100 家生命科学客户
客户基础展示了强劲的行业牵引力和经验证的平台采用率。
AI 赋能自动化
AI 辅助自动化、提取和应用组合,加速组合和处理。
DMS 软件投资回报率:数字制药文档管理的业务效益
合规性、速度、准确性和可扩展的数字质量
25%
审计发现减少
部署后发现减少的目标百分比。
30%
发布时间改善
文档发布时间预计减少量。
50%
手动工作量节省
手动处理时间预计减少量。
引领生命科学前沿
获取最新产品更新、合规动态及行业洞察,直接发送至您的邮箱。