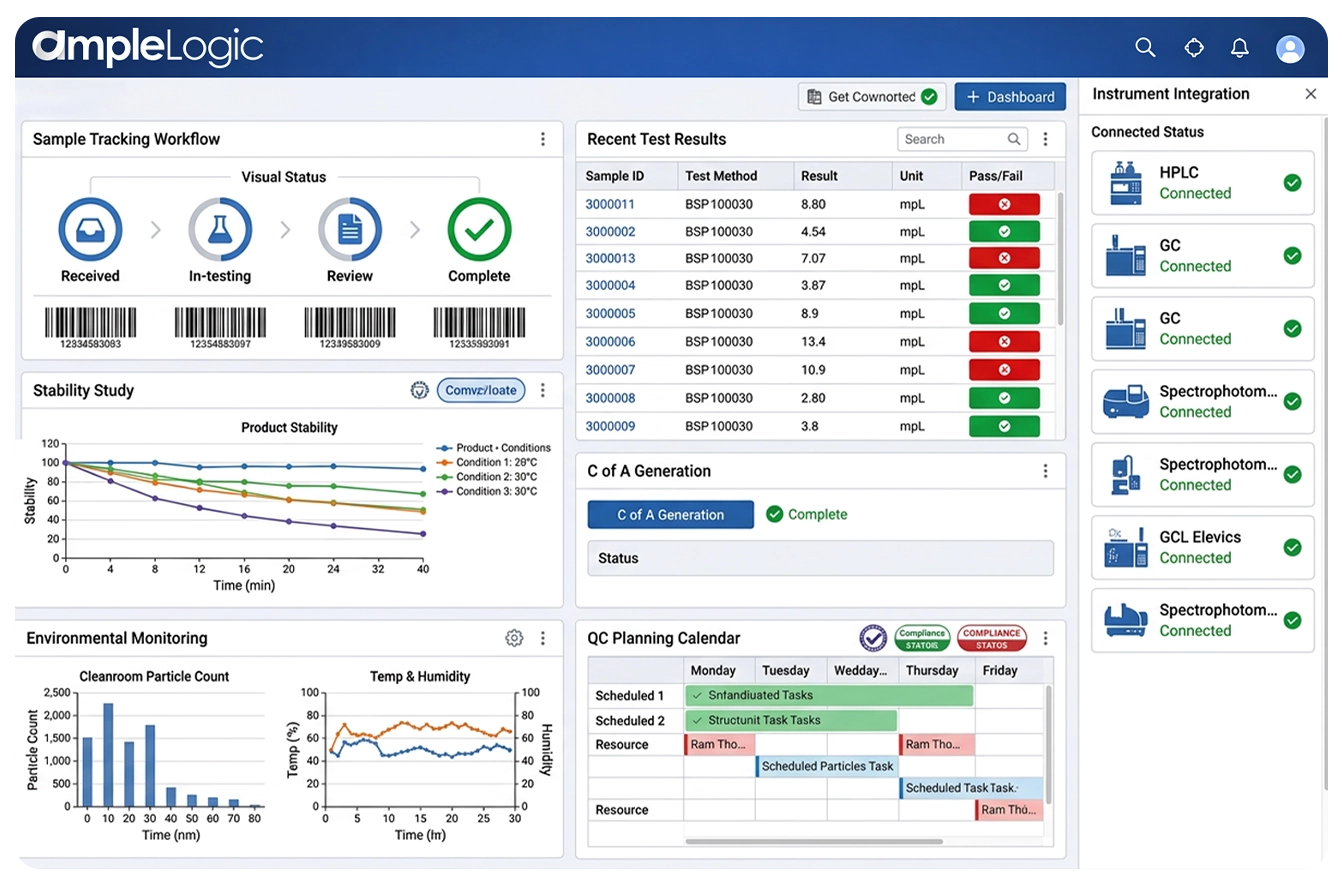
互联实验室生态系统:统一LIMS数字化平台
AmpleLogic LIMS为实验室运营创建单一事实来源——消除数据孤岛,减少转录错误,并作为统一的云LIMS和科学数据管理平台,实现企业范围内的实时可视化。
分析仪器
HPLC、GC、LC-MS、ICP-OES、UV-Vis、溶出度仪和粒度分析仪,通过经验证的双向接口连接
ERP系统
与SAP、Oracle和NetSuite无缝集成,用于批次放行、库存和物料管理
制造执行
与MES和eBMR实时数据交换,用于过程检测、批记录和生产排程
质量管理
与eQMS双向集成,用于偏差触发、CAPA管理和OOS调查
色谱数据系统
Empower、Chromeleon、OpenLab和MassLynx的预建连接器,自动导入结果
文件管理
SOP、分析方法和规格与DMS同步,实现版本受控的实验室运营
专为GxP受管制实验室构建的LIMS
样品登记
使用条形码/RFID扫描自动样品登录,来自ERP/MES的批次级登记,以及带预定义检测分配的可配置样品计划
样品跟踪
实时保管链,包含位置跟踪、存储管理、暂停/放行状态,以及接近SLA截止日期的自动预警
检测执行
模板驱动的分析方法执行,包含仪器数据采集、系统适用性验证和带可配置舍入规则的在线计算
结果验证
自动OOS/OOT检测、基于规则的通过/失败评估、带电子签名的多级审查和审批工作流程
分析证书
自动生成COA/ROA,包含可配置模板、批次级汇总、客户特定格式和数字分发
法规报告
可供检查的数据导出、稳定性趋势报告、统计分析包和FDA/EMA申报的法规提交格式输出
样品登记
使用条形码/RFID扫描自动样品登录,来自ERP/MES的批次级登记,以及带预定义检测分配的可配置样品计划
样品跟踪
实时保管链,包含位置跟踪、存储管理、暂停/放行状态,以及接近SLA截止日期的自动预警
检测执行
模板驱动的分析方法执行,包含仪器数据采集、系统适用性验证和带可配置舍入规则的在线计算
结果验证
自动OOS/OOT检测、基于规则的通过/失败评估、带电子签名的多级审查和审批工作流程
分析证书
自动生成COA/ROA,包含可配置模板、批次级汇总、客户特定格式和数字分发
法规报告
可供检查的数据导出、稳定性趋势报告、统计分析包和FDA/EMA申报的法规提交格式输出
当前LIMS软件格局
了解当今制药行业实验室信息学软件和LIMS平台的现状
大多数实验室已有LIMS
普遍存在的基线系统
现有LIMS高度定制化且难以升级
定制集成造成升级阻力
高维护和验证成本
持续的维护和法规再验证支出
多个单点解决方案并存
碎片化工具集增加集成负担
实验室总监优先事项:验证与总拥有成本
减少LIMS验证负担 + 整合单点解决方案以降低长期总拥有成本(TCO)
现有LIMS软件的主要挑战
碎片化工作流程、手动流程和合规风险
主要专注于样品跟踪
限制了样品进出以外的可视化
- 限制端到端可视化
- 增加手动交接
- 提高合规风险
- 导致产品放行更慢
稳定性和EMS在LIMS外处理
碎片化运营增加复杂性和风险
- 造成运营控制碎片化
- 限制范围覆盖
- 使验证复杂化
- 推动评估替代方案的需求
电子表格依赖
手动流程削弱合规性和效率
- 造成手动状态更新
- 削弱趋势分析和审计跟踪
- 增加错误率
- 使管理者依赖非正式报告
用户体验差
传统系统减慢采用和工作流程
- 降低采用率
- 减慢日常工作流程
- 带来定制化挑战
- 凸显集成改进需求
仪器集成挑战
仪器数据孤岛
HPLC、GC、LC-MS、微生物系统各自独立运行
来自CDS的手动数据传输
色谱数据系统需要手动录入步骤
数据完整性风险
审计跟踪缺口和潜在合规违规
复杂的验证负担
每个连接都需要大量系统适用性测试
优先经验证的连接器
预建的合格仪器集成降低风险
优先审计跟踪支持
从仪器到报告的完整可追溯性
优先减少手动交接
自动化数据采集以减少错误和周期时间
LIMS软件核心能力
专为现代实验室运营管理而构建的制药LIMS软件功能
样品生命周期管理
企业级样品跟踪软件,提供从登记到分析、报告和处置的端到端样品生命周期管理
检测与方法执行
以完整可追溯性定义和执行分析程序
仪器连接
仪器集成软件,与实验室仪器、色谱数据系统无缝连接,以及LIMS ELN集成
条形码和RFID处理
自动化样品识别和实验室库存管理跟踪
质量控制工作流程
数字化实验室平台内置QC检查、审批和合规验证
电子签名和审计跟踪
FDA合规实验室软件,满足完整的21 CFR Part 11、GxP合规LIMS和ISO 17025合规LIMS要求
可定制报告
实验室分析平台,具有灵活的COA、ROA、实验室绩效分析和法规就绪报告生成
直观仪表板
带KPI、科学数据分析和实验室绩效分析的实时实验室运营管理仪表板
面向制药实验室的高级LIMS模块
专为特定实验室运营而构建的LIMS解决方案
高级稳定性管理
面向制药和生物技术的符合ICH标准的稳定性研究管理软件
AmpleLogic高级稳定性管理是专为管理完整稳定性研究生命周期而构建的稳定性检测管理系统——从稳定性方案创建和样品取样排程,到储存条件管理、检测执行、稳定性趋势分析和法规就绪报告。
主要功能
稳定性方案创建
使用可配置研究设计、储存条件、验收标准和自动取样计划,制定符合ICH Q1A的稳定性方案
稳定性样品排程
带日历提醒、动态重新排程和完整审计跟踪的自动化样品取样排程
储存条件和环境监测
监控稳定性储存箱和仓库中的温度和湿度等环境参数
检测执行与数据采集
在同一LIMS工作流程中执行分析检测,具有直接仪器集成和完整可追溯性
稳定性趋势分析与报告
自动统计趋势分析,包含降解曲线拟合、控制图和法规就绪稳定性报告
AI驱动的有效期确定
机器学习驱动的有效期预测,包含置信区间、早期到期风险预警和加速稳定性预测
到期确定与复检日期管理
基于稳定性趋势数据的系统性到期确定、复检日期计算和自动化标签声明支持
ICH Q1A法规合规
内置与ICH Q1A-Q1F稳定性指南对齐,适用于制药和生物技术稳定性项目
FDA稳定性要求合规
满足FDA稳定性要求(包括21 CFR Part 211.166)的预配置工作流程
GMP稳定性项目管理
全面的GMP稳定性项目,包含持续稳定性承诺和批准后监控
稳定性趋势分析与有效期预测
AI分析稳定性检测结果,以识别产品降解趋势并估计产品有效期
主要优势
通过自动化排程和方案管理加速稳定性研究执行
利用AI驱动的趋势分析将有效期确定时间缩短40%
确保完全符合ICH Q1A、FDA和GMP对齐工作流程的法规要求
通过自动化样品取样排程消除错过的取样点
通过实时环境监测集中管理储存条件
AI驱动的LIMS软件分析
预测性质量分析、异常检测和智能排程,将实验室数据转化为可行洞察——将AmpleLogic与传统LIMS供应商区分开来
预测性质量分析
机器学习模型分析历史QC数据、稳定性趋势和工艺参数,在检测完成前预测质量结果。
- 来自趋势数据的早期OOS预测
- 带置信区间的有效期预测
- 过程能力分析和Cpk监控
异常检测
AI持续监控仪器输出、环境数据和分析员模式,实时标记统计异常值和潜在数据完整性问题。
- 仪器漂移检测(在故障前)
- 异常结果模式识别
- 环境偏差早期预警
智能QC排程
智能工作量平衡,根据实时实验室产能优化样品到仪器分配、分析员排程和活动排序。
- 动态优先级排程
- 仪器利用率优化
- 分析员技能匹配分配
自动化偏差预警
OOS/OOT结果、趋势违规和合规差距触发AI预警,自动在eQMS中启动调查工作流程。
- 带背景信息的即时OOS/OOT通知
- 自动生成调查包
- 根本原因推荐引擎
自然语言实验室查询
用于查询实验室数据的对话式AI界面——用日常语言提问,如“显示本周到期的产品X待处理稳定性样品”。
- 即时实验室状态查询
- 跨系统数据检索
- 高管仪表板生成
智能方法选择
AI根据样品类型、历史性能数据、仪器可用性和法规要求推荐最优分析方法。
- 方法性能基准测试
- 缩短方法开发时间
- 合规意识的方法选择
AI-Driven Stability Prediction & Shelf-Life Forecasting
Machine learning algorithms analyze historical stability study data to predict future product behavior — estimating shelf-life, degradation trends, stability variation probabilities, and risk of specification failures.
- Early identification of potential stability issues
- Data-driven shelf-life predictions with confidence intervals
- Improved regulatory documentation for stability programs
AI Instrument Failure Prediction & Predictive Maintenance
AI continuously monitors instrument performance data — calibration records, usage hours, error logs, maintenance history, and performance trends — using predictive analytics to estimate failure risk levels and generate instrument risk scores.
- Predictive maintenance alerts before failures
- Reduced instrument downtime and delays
- Optimized maintenance scheduling
AI-Powered Sampling Time Estimation for Pharma QC
AI engine analyzes historical sampling data based on product type, material category, number of containers, batch size, and sampling procedure complexity to estimate expected sampling time for each batch.
- Improved laboratory scheduling and workforce planning
- Reduced sampling delays
- Increased operational efficiency
OCR-Enabled Document Processing for Laboratory Data
Optical Character Recognition (OCR) automatically extracts information from uploaded documents — including PDFs, images, scanned reports, certificates, and handwritten records — converting them into structured digital records integrated into the LIMS database.
- Automated data extraction from scanned documents
- Elimination of manual data entry
- Faster document processing and improved accessibility
AI Sample Testing TAT Prediction for Laboratory Efficiency
AI analyzes historical testing durations and predicts expected completion time for each sample — considering test method complexity, instrument availability, analyst workload, and historical test durations for accurate TAT forecasting.
- Accurate turnaround time forecasting
- Improved sample scheduling and prioritization
- Enhanced laboratory productivity
LIMS工作流程架构
从样品接收到法规报告的端到端实验室工作流程自动化
主数据
产品、方法、仪器、用户、标准
稳定性
研究与有效期
确认
IQ/OQ/PQ验证
COA/ROA
法规
主数据
- •产品
- •方法
- •仪器
- •用户
- •质量标准
辅助管理
- •资产管理
- •化学品与试剂跟踪
- •色谱柱管理
- •对照标准品
- •溶液配制
- •培养基管理
- •菌种管理
样品生命周期
- •样品登记
- •采集与接收
- •系统登录
- •检测分配
- •分析执行
- •结果审查与审批
- •分析证书(COA)
法规输出
- •分析证书(COA)
- •分析报告(ROA)
- •法规申报
LIMS数据完整性与法规合规
ALCOA+数据完整性、21 CFR Part 11、EU Annex 11、ISO 17025和GxP合规——内置于AmpleLogic企业级LIMS平台
ALCOA+数据完整性框架
每个数据点均可归因、清晰、同步、原始且准确——完整性、一致性、持久性和可用性扩展内置于平台。
- 每次数据变更的不可变审计跟踪
- 带意图和含义的电子签名
- 带数据恢复验证的自动备份
- 防篡改数据存储架构
FDA 21 CFR Part 11合规
预验证的电子记录和签名,具有封闭系统控制、权限检查和设备验证,适用于FDA受管制实验室。
- 可配置电子签名工作流程
- 权限检查和基于角色的访问控制
- 带时间戳的可归因审计记录
- 封闭系统安全架构
EU Annex 11合规
欧洲制药生产的计算机化系统控制,包括验证要求、数据存储、打印输出和业务连续性。
- 计算机化系统验证支持(IQ/OQ/PQ)
- 数据迁移和归档控制
- 业务连续性和灾难恢复
- 供应商资质文件记录
GxP法规合规
GLP、GMP和GCP环境下的全面良好规范合规,内置ICH、WHO、PIC/S和16个以上全球卫生当局控制。
- GLP、GMP、GCP工作流程模板
- ICH Q2、Q7、Q10指南对齐
- 可供检查的报告包
- 变更控制和再验证支持
面向制药及生物技术实验室的集成数字化GxP生态系统
AmpleLogic制药LIMS原生集成13个GAMP解决方案——这是其他供应商无法比拟的竞争优势
OOS结果自动触发偏差;CAPA结果更新检测方法;变更控制管理分析程序更新
双向:OOS→偏差,CAPA→方法更新
稳定性数据和COA直接输入法规申报;注册状态更新样品检测要求
LIMS→稳定性数据→RIMS申报
过程样品从批记录自动创建;QC结果触发批次放行决策;环境数据关联至批次
双向:批次样品↔QC结果
QC趋势数据、稳定性结果和OOS统计自动填充年度产品回顾报告,无需手动汇编
LIMS→QC趋势+OOS统计→APQR报告
SOP、分析方法和规格在DMS中版本受控;有效文件在LIMS检测执行中自动关联
DMS→受控文件→LIMS方法执行
检测执行前验证分析员资质;培训完成自动激活分析方法访问权限
LMS→培训状态→LIMS分析员资质
过程检测和放行检测数据输入CPV统计模型,用于持续过程能力监控
LIMS→过程数据→CPV统计分析
洁净室监控数据关联至生产批次;偏差在LIMS中触发自动暂停/放行工作流程
EMS→环境数据→LIMS批次暂停/放行
与传统企业级、R&D导向或模块化分析LIMS供应商不同——AmpleLogic是唯一一家提供完整原生集成GxP生态系统的供应商,LIMS数据可在质量、法规、生产和合规系统之间无缝流动,无需中间件。
企业级LIMS集成:ERP、ELN与仪器连接
将您的企业级LIMS平台连接至整个运营生态系统
实验室仪器
与分析设备无缝连接
- 质谱(MS)
- HPLC
- GC
- ICP-OES
- UV-Vis
企业系统
与业务和生产系统集成
- SAP
- Oracle
- NetSuite
- MES(制造执行系统)
- QMS(质量管理系统)
- DMS(文件管理系统)
- ELN(电子实验室记录本)
数据与分析
连接数据仓库和商业智能
- 数据仓库
- BI(商业智能)平台
- AI/ML引擎
- 云分析
连接选项
灵活集成的多种协议
- 100+预建连接器
- REST API
- SFTP
- 直接数据库连接
- HL7(医疗协议)
API优先架构
用于定制集成需求的现代可扩展平台
- RESTful API
- Webhook支持
- 自定义连接器
- 第三方集成框架
自动化LIMS合规:消除重复性手动检查
自动化优先平台减少手动验证开销
自动化规则验证
通过可配置业务逻辑和合规规则消除手动QC检查
模板驱动方法执行
预配置模板确保一致执行并减少手动配置
实时仪器资质状态
系统适用性和维护计划的自动跟踪
主数据协调
实验室标准、方法和程序的单一事实来源
异常驱动审查
将分析员注意力集中在偏差和超标结果上
端到端流程
样品和结果通过完整实验室工作流程的自动化路由
LIMS软件ROI:质量实验室的可量化业务影响
LIMS转型的真实成果
+25%
周期时间影响
-20%
产能损失
+30%
合规工作量
20%
TAT减少
分析结果周转时间缩短20%
25%
生产效率提升
每分析员班次处理样品增加25%
90%
审计就绪
关闭观察项时间减少90%
传统LIMS的隐性成本
设备闲置时间
仪器在手动切换之间闲置
产能损失10-30%
分析员瓶颈
手动验证和审批减慢结果交付
样品周转延迟
跨系统数据孤岛
ELN、MES和CDS独立运行
手动整合和错误风险
重复手动检查
每个步骤执行相同验证
+25%周期时间膨胀
验证和变更控制开销
任何系统修改都需要大量测试
+30%合规工作量
智能低代码LIMS如何超越传统平台
部署方法的横向对比
| 维度 | 传统单体式 | 传统模块式 | 智能低代码 |
|---|---|---|---|
| 实施周期 | 18-24个月 | 12-18个月 | 3-6个月 |
| 总拥有成本(TCO) | 250-350万美元 | 180-250万美元 | 100-150万美元 |
| AI与分析 | 传统,仅限报告 | 附加功能,额外费用 | 内嵌AI,原生预测分析 |
| 定制化与灵活性 | 硬编码,变更控制负担重 | 模块化但需要开发人员 | 低代码/无代码,业务用户可配置 |
实施周期
传统: 18-24个月
常规: 12-18个月
智能: 3-6个月
总拥有成本(TCO)
传统: 250-350万美元
常规: 180-250万美元
智能: 100-150万美元
AI与分析
传统: 传统,仅限报告
常规: 附加功能,额外费用
智能: 内嵌AI,原生预测分析
定制化与灵活性
传统: 硬编码,变更控制负担重
常规: 模块化但需要开发人员
智能: 低代码/无代码,业务用户可配置
AmpleLogic LIMS:市场定位与竞争优势
AmpleLogic与成熟LIMS供应商的比较
| 类别 | 供应商 | 定位 | 局限性 |
|---|---|---|---|
| 传统企业级LIMS | 传统供应商 | 高度可配置,成熟的制药客户群,广泛的仪器支持 | 18-24个月部署,需要大量定制,TCO高,无集成GxP生态系统 |
| 企业级R&D平台 | R&D导向供应商 | 分子建模+实验室信息学,云平台,AI/生成式AI助手 | R&D导向而非QC,价格昂贵,封闭生态系统供应商锁定,制造集成有限 |
| 现代数字化实验室平台 | 云原生初创企业 | 云原生,现代UX,API优先,R&D快速部署 | 制药QC能力有限,法规合规薄弱,未经GMP验证用于生产 |
| 模块化分析LIMS | 分析优先供应商 | 内置分析/ML,云原生HTML5,集成LIMS+ELN+LES+SDMS技术栈 | 实施复杂,GxP生态系统有限,AI功能需要验证开销 |
| 集成GxP平台 | AmpleLogic | AI驱动实验室信息学+完整数字化GxP生态系统(13个GAMP解决方案),低代码/无代码,3-6个月部署 | 新进入者正在建立企业参考基础 |
传统企业级LIMS
传统供应商定位: 高度可配置,成熟的制药客户群,广泛的仪器支持
局限性: 18-24个月部署,需要大量定制,TCO高,无集成GxP生态系统
企业级R&D平台
R&D导向供应商定位: 分子建模+实验室信息学,云平台,AI/生成式AI助手
局限性: R&D导向而非QC,价格昂贵,封闭生态系统供应商锁定,制造集成有限
现代数字化实验室平台
云原生初创企业定位: 云原生,现代UX,API优先,R&D快速部署
局限性: 制药QC能力有限,法规合规薄弱,未经GMP验证用于生产
模块化分析LIMS
分析优先供应商定位: 内置分析/ML,云原生HTML5,集成LIMS+ELN+LES+SDMS技术栈
局限性: 实施复杂,GxP生态系统有限,AI功能需要验证开销
集成GxP平台
AmpleLogic定位: AI驱动实验室信息学+完整数字化GxP生态系统(13个GAMP解决方案),低代码/无代码,3-6个月部署
局限性: 新进入者正在建立企业参考基础
LIMS软件分析师认可与行业奖项
受领先机构信赖,获分析师认可
Frost Radar领导者象限
Frost & Sullivan
在低代码LIMS领域被评为领导者,部署速度提升10倍
120+全球实施案例
AmpleLogic
与企业客户和财富500强企业有成熟的合作记录
2024-2025年Gartner评估
Gartner
纳入Gartner LIMS魔力象限评估,获第三方认可
2024-2025
引领生命科学前沿
获取最新产品更新、合规动态及行业洞察,直接发送至您的邮箱。