KI-gestützte Unternehmensplattform für Biowissenschaften
DigitalisierenQualität, Labor und Fertigung
APQR | CPV | LIMS | QMS | Einhaltung
Entdecken Sie KI-gestützte Lösungen beiPHARMAP 2026
AmpleLogic nimmt an der PHARMAP 2026, dem Kongress für Pharmaherstellung und -verpackung, am 20.–21. April 2026 in Amsterdam teil.
Besuchen Sie uns am Stand Nr. 11 und entdecken Sie unsere aPaaS-basierten Lösungen für Digitalisierung, Compliance und Qualitätsmanagement in der Life Sciences.
Lernen Sie unsere Expert:innen kennen

Prashant Nookala
Leiter Vertrieb

Shaury Gupta
Verkaufsleiter
Besuchen Sie unseren Stand #11 Sprechen Sie mit unseren Expert:innen während der PHARMAP 2026.
Jahre
Innovation in der Pharma-Digitalisierung
Kunden
Weltweit zufrieden
GAMP-Lösungen
COTS-Anwendungen
Qualifizierte Ingenieure
Spezielles Validierungsteam
Glückliche Benutzer
Globaler Fußabdruck
Warum isolierte Pharma-Software ist Kostet Sie mehr Als Sie denken
Die meisten Pharmaunternehmen betreiben 5–10 voneinander unabhängige Plattformen für Qualität, Labor, Herstellung und Compliance. Die versteckten Kosten summieren sich schnell.
Isolierte Qualitätssicherungs-, Qualitätskontroll- und Fertigungsabläufe verzögern die Chargenfreigabe
Getrennte Systeme erzwingen manuelle Übergaben zwischen Qualität, Labor und Produktion – was jeden Chargenzyklus um Tage verlängert.
Bis zu 30 % längere Chargenfreigabezeiten
Die QA/QC-Arbeitsbelastung steigt trotz bestehender eQMS, DMS und LIMS weiter an
Punktlösungen sprechen nicht miteinander. Teams geben Daten erneut ein, holen Genehmigungen ein und erstellen Berichte manuell.
Mehr als 40 % der Zeit werden für wertlose Arbeit aufgewendet
Ältere Plattformen machen jede Prozessänderung langsam und teuer
Starre Architekturen erfordern selbst für kleinere Workflow-Updates Anbietertickets und bezahlte Berater.
6–12-monatige Wechselzyklen
Wachsende Nachfrage nach Rückverfolgbarkeit, Auditbereitschaft und Datenintelligenz
Regulierungsbehörden erwarten Transparenz in Echtzeit. Tabellenkalkulationen und fragmentierte Datenbanken können dies nicht liefern.
Wiederkehrende Prüfungsfeststellungen
Zunehmende Produktkomplexität – Biologika, CGT und globale Lieferketten
Neue Modalitäten erfordern flexible, vernetzte Systeme, für die ältere COTS-Plattformen nicht entwickelt wurden.
Höheres Compliance-Risiko
Wir stellen vorAPQR und CPVfür die GMP-Herstellung
AmpleLogic bietet jetzt APQR-Software (Annual Product Quality Review) und CPV-Software (Continued Process Verification) auf einer einheitlichen Plattform und ersetzt damit manuelle PQR-Prozesse, Minitab-Diagramme und getrennte Tabellenkalkulationen durch automatisierte, KI-gesteuerte Qualitätsinformationen.
Jährliche Software zur Überprüfung der Produktqualität
Cloudbasierte APQR-Software, die automatisch Herstellungs-, Qualitäts- und Labordaten über LIMS, eQMS, MES, ERP und DMS hinweg aggregiert, um konforme PQR-Berichte, Qualitätsmanagement-Bewertungen (QMR) und behördliche Dossiers zu erstellen – und so Echtzeit-Einblicke in die Qualitätsprüfung pharmazeutischer Produkte und Prozessfähigkeitsanalysen liefert.
70–80 %
APQR-Vorbereitungszeitverkürzung
Null
Manuelle Datenerfassung
6σ
Statistische Berichte
- Automatisierte PQR-Berichterstellung mit konfigurierbaren APQR-Vorlagen nach Produkttyp, Standort und regulatorischem Markt
- Integrierte Six-Pack-Berichte, Cp/Cpk/Pp/Ppk-Analyse und Nelson-Regelerkennung – ersetzt Minitab, SAS und SPSS
- KI-gestützte zusammenfassende Erzählungen, OCR-Datenextraktion und 5-Warum-Ursachenanalyse für eine schnellere Berichterstellung
- Systemübergreifende Datenaggregation aus LIMS-, eQMS-, MES-, DMS-, ERP-, Stabilitäts- und Kalibrierungssystemen
- Chargenbezogene Trends, visuelle CPK-Indikatoren und Prozessparameter-Vergleichsberichte für eine kontinuierliche Qualitätsüberwachung
- GMP-konform mit FDA, EMA, MHRA, WHO, ICH Q7 und ICH Q10 – 21 CFR Part 11 und Annex 11 bereit
Fortsetzung der Prozessverifizierungssoftware
Digitale CPV-Software für die pharmazeutische Herstellung, die die kontinuierliche Prozessüberprüfung von der manuellen statistischen Überwachung in eine KI-gesteuerte Manufacturing-Intelligence-Plattform umwandelt – Abweichungen vorhersagt, Prozesse optimiert und eine gleichbleibende Produktqualität über den gesamten Validierungslebenszyklus (Stufe 1, 2 und 3) gewährleistet.
Echtzeit
CPP/CQA-Überwachung
75 %
Aufwandsreduzierung
100 %
Audit-Trail-Abdeckung
- Echtzeitüberwachung kritischer Prozessparameter (CPPs) und kritischer Qualitätsattribute (CQAs) in allen Fertigungsabläufen
- Automatisierte SPC-Diagrammerstellung – I-MR, X-bar R, Kontrollkarten mit Erkennung von Verstößen gegen die Nelson-Regel und Verfolgung des Fähigkeitsindex
- R-basierte Statistik-Engine für Six-Pack-Berichte, ANOVA, Regression und multivariate Analyse – keine manuellen Minitab-Exporte
- Prädiktive KI-Analysen, die Prozessabweichungen vor Chargenausfällen erkennen, mit automatischer Trendinterpretation und Anomalieerkennung
- Nahtlose APQR-Integration – CPV-Nachweise der Stufe 3 werden automatisch in jährliche Produktqualitätsüberprüfungen eingetragen
- Konform mit den FDA Process Validation Guidance, ICH Q8/Q9/Q10, EU GMP Annex 15 und 21 CFR Part 11
Einheitliche APQR + CPV-Plattform
Im Gegensatz zu eigenständigen Tools bietet AmpleLogic sowohl die jährliche Überprüfung der Produktqualität als auch die kontinuierliche Prozessüberprüfung auf einer einzigen Plattform mit gemeinsamen Daten, gemeinsamen Analysen und gemeinsamer Compliance – wodurch Datensilos zwischen der Überwachung der Stufe 3 und den jährlichen Qualitätsüberprüfungen beseitigt werden.
Eine Low-Code-Pharma-Plattform ersetzt Über 14 isolierte GMP-Softwareanbieter
Anstatt separate LIMS, eQMS, MES, DMS und LMS von verschiedenen Anbietern zu kaufen, stellen Sie sie alle auf einer einzigen erweiterbaren Plattform mit gemeinsamen Daten, gemeinsamen Arbeitsabläufen und gemeinsamer Compliance bereit.
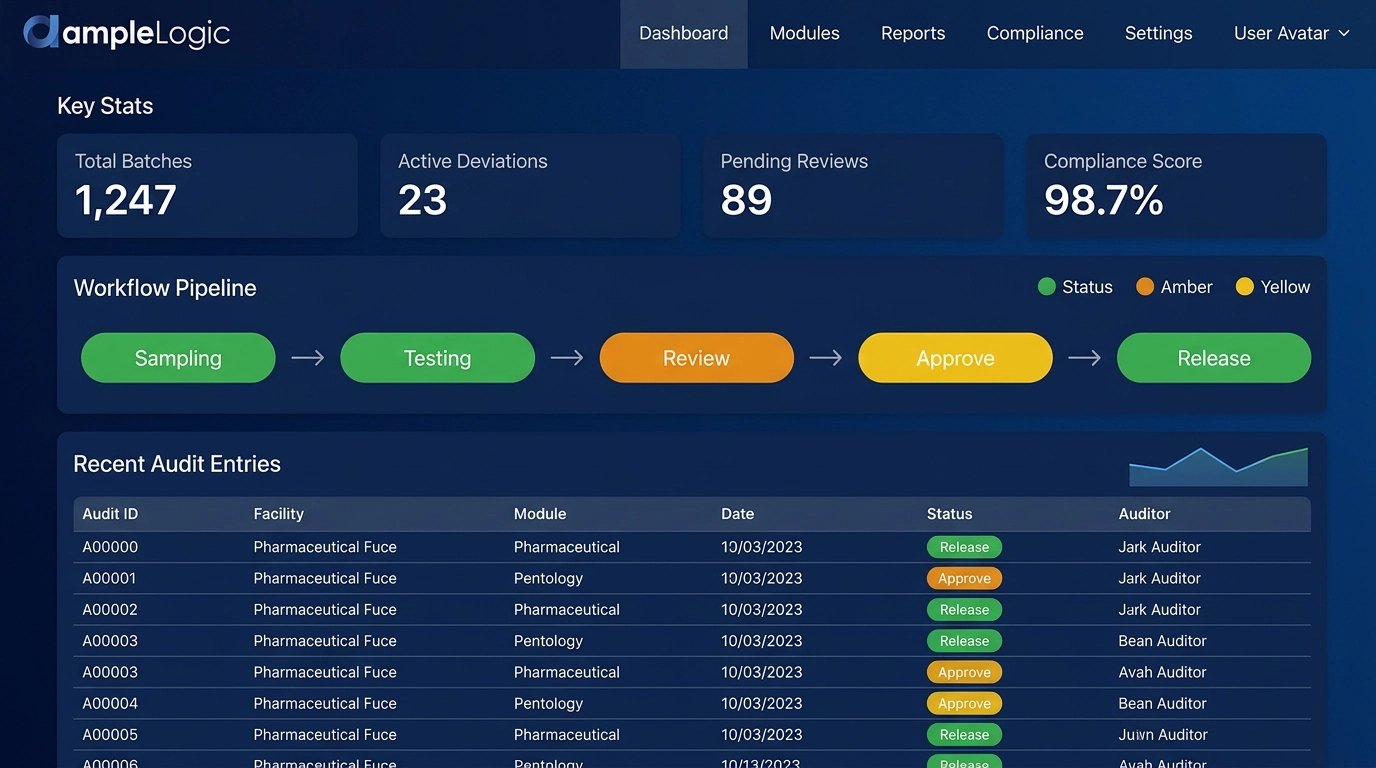
Visueller Low-Code-Builder
Drag-and-Drop-Tools zum Erstellen, Anpassen und Bereitstellen von GxP-Anwendungen – keine benutzerdefinierte Programmierung erforderlich.
Konfigurierbare Workflow-Engine
Mehrstufige Genehmigungen, elektronische Signaturen und Audit-Trails sind sofort einsatzbereit. Ändern Sie Arbeitsabläufe in Stunden, nicht in Monaten.
Einzelne einheitliche Datenschicht
Eine Datenbank, die alle über 14 Module unterstützt. Keine Punkt-zu-Punkt-Integrationen. Datenaustausch in Echtzeit zwischen Qualität, Labor und Werk.
Integrierte GxP-Konformität
Vom ersten Tag an vorvalidiert gemäß 21 CFR Part 11, Annex 11, GAMP 5 und EU-GMP-Richtlinien.
Jedes Gerät, überall
Reaktionsfähige Schnittstellen, die auf Tablets in der Werkstatt, Labor-Desktops und Telefonen von Führungskräften funktionieren.
Öffnen Sie das Integration Framework
REST-APIs, HL7, SAP und über 50 vorgefertigte Konnektoren zum Einbinden in Ihr bestehendes ERP- und Instrumenten-Ökosystem.
KI-Lösungen für Pharma-Digitalisierung
Automatisieren Sie Prozesse und stärken Sie die Compliance in den Bereichen Dokumentenmanagement, Reporting, SOPs und CAPA.
KI-gestütztes Dokumentenmanagement
Chatbot-Benutzeroberfläche, automatisierte Indizierung und behördliche Prüfprotokolle für schnelleren Abruf und konsistente Aufzeichnungen.
Schnellerer Abruf, konsistente Aufzeichnungen und Prüfungsbereitschaft
Agentischer AI Report Builder
Automatisierte Berichtserstellung und kontextbezogene Zusammenfassungen für QC- und Führungsteams.
Reduzieren Sie den Zeitaufwand für die manuelle Berichterstattung und verbessern Sie die Übersicht
KI-Empfehlungs-Engines
Ursachenvorschläge für Abweichungen und CAPA mit priorisierten Maßnahmen für eine schnellere Lösung.
Datengesteuerte Priorisierung zur Verkürzung der Lösungszyklen
SOP-Podcast und Mitarbeiterbewertung
Automatisierte Fragengenerierung und SOP-Podcast in mehrsprachiger Sprache für Schulung und Engagement.
Generieren Sie MCQs mit plausiblen Ablenkern und detaillierten Erklärungen für eine effektive Wissensbewertung
Vom Konzept bis zur Compliance in Drei Schritte
Beraten und definieren
Unsere Domänenexperten bilden Ihre Arbeitsabläufe, Compliance-Anforderungen und Integrationsanforderungen ab, um einen maßgeschneiderten Bereitstellungsentwurf zu erstellen.
Konfigurieren und validieren
Mit unserem Low-Code-aPaaS konfigurieren wir vorvalidierte Module genau nach Ihren Vorgaben. Keine benutzerdefinierte Codierung, keine Compliance-Lücken.
Bereitstellen und skalieren
Gehen Sie in Wochen, nicht in Monaten, live. Unser Team kümmert sich um Schulungen, Datenmigration und Post-Go-Live-Support, um einen nahtlosen Übergang zu gewährleisten.
Ergebnisse, die sprechen für sich selbst
Beschleunigung der Markteinführung
Schnelle Einführung von QA-, QC-, Herstellungs- und Regulierungssystemen unter Verwendung von Low-Code-Pharmakomponenten.
Reduzierung der Integrationskosten
Alle auf einer einzigen Plattform erstellten Anwendungen bieten fertige Integrationen, wodurch die Integrationskosten erheblich gesenkt werden.
Einsparungen bei den Infrastrukturkosten
Durch die Einführung von Open-Source-Servern wie Linux und PostgreSQL werden die Infrastrukturkosten drastisch gesenkt.
Einhaltung gesetzlicher Vorschriften
Einhaltung der US-amerikanischen FDA und MHRA; CFR Part 11 und Annex 11 sind vom ersten Tag an in jedes Modul integriert.
Projekterfolgsquote
Gegenüber 54 % im IT-Branchendurchschnitt, was eine überlegene Lieferkonsistenz über mehr als 500 Implementierungen hinweg zeigt.
Domänenexpertise
In jedem Produkt sind fundierte Kenntnisse der Biowissenschaften verankert. Wir verstehen GxP, 21 CFR Part 11 und Annex 11.
Verpflichtungen, die die Akzeptanz fördern
Zwei Säulen, die das Lernen beschleunigen, Wiederholungsgeschäfte ermöglichen und die Betriebskosten senken
Technologie und Talent
Proaktive Einführung neuer Technologien, um das Lernen der Mitarbeiter zu ermöglichen und die Marktführerschaft zu sichern.
Produktinnovation und TCO
Kontinuierliche Produktaktualisierungen, die Integrationen optimieren und die Gesamtbetriebskosten minimieren.
Von über 120 Pharmakunden bis hin zu bewährten Stammkunden
Ausgewählte Wiederholungsaufträge beweisen Vertrauen, Compliance und einen schnelleren ROI in der Pharma- und Biotechnologiebranche.














































ISO 9001:2015
Qualitätsmanagement
ISO 27001:2022
Informationssicherheit
SOC 2
Konform
Von Branchenanalysten anerkannt
Verifizierte G2-Bewertung 4,8/5 aus Über 300 Bewertungen
Frost & Sullivan
Leader-Quadranten-Anerkennung 2025
AmpleLogic im Leader-Quadranten für Life Sciences LIMS 2025 positioniert.
Gartner
RIMS 2024-Evaluierungszyklus
Validiert die Lebensfähigkeit des Anbieters und die Produktreife für Unternehmenskäufer.
Märkte & Märkte
Top 16 des globalen QMS 2025
Gelistet in 16 der weltweit führenden pharmazeutischen Qualitätsmanagementsoftware (QMS).
Gartner
LIMS 2025-Evaluierungszyklus
AmpleLogic im Leader-Quadranten für Life Sciences LIMS 2025 positioniert.
"Die schnelle Implementierung und der intuitive Drag-and-Drop-Builder sorgten für eine beschleunigte, konforme App-Bereitstellung mit einem ROI innerhalb von Monaten."
"Der reaktionsschnelle Kundenservice und vorab validierte Komponenten beschleunigten unsere Prüfungsbereitschaft und reduzierten das Compliance-Risiko bei allen Implementierungen."
"Kunden berichten von einer schnelleren Validierung, einer stärkeren Compliance und einem messbaren ROI nach der Einführung."
89 G2-Abzeichen. 291+ verifizierte Bewertungen.
AmpleLogic gilt auf G2 – der weltweit größten Software-Review-Plattform – als führender Anbieter und Leistungsträger in den Bereichen medizinisches QMS, Dokumentenmanagement, LMS im Gesundheitswesen und mehr.
Highlights des G2-Abzeichens – Sommer 2024
Was Kunden zu G2 sagen
"Das QMS-System von Amplelogic verfügt über alle erforderlichen qualitätsbezogenen Module und alle Abweichungen, Änderungskontrollen und CAPAs werden effektiv verwaltet und verfolgt. Alle Module sind super einfach zu bedienen."
Kandikattu K.
Qualitätsprofi
"Es lässt sich nahtlos in unsere anderen Tools integrieren. Sie haben die meisten unserer individuellen Anpassungswünsche berücksichtigt und es für uns sehr benutzerfreundlich gemacht."
Qualitätssicherungsmanager
Mittelständische Pharmaindustrie
"Eine benutzerfreundliche und einfach zu bedienende Software. Auch das Auffinden alter Datensätze ist ein Kinderspiel, was definitiv dazu beiträgt, Zeit zu sparen und den Prozess effektiver zu gestalten."
Nirogya D.
Dy. Manager
"Das System entspricht den Anforderungen von 21 CFR Part 11 und EU Annex 11. Die Unterstützung durch das Team bei der Ersteinrichtung war wirklich hilfreich und hat den Übergang reibungslos gestaltet."
Krishna C.
Compliance-Leiter
Gebaut für die meisten Regulierte Branchen
Umfangreiches Fachwissen im gesamten Life-Sciences-Ökosystem mit speziell entwickelten Compliance-Frameworks für jede Branche.
Arzneimittel
Durchgängige Chargenfertigung, Qualitätskontrolle und Einhaltung gesetzlicher Vorschriften für Wirkstoff- und Fertigdosierungsanlagen.
Biotechnologie
Flexible Arbeitsabläufe für die Herstellung von Biologika, die Entwicklung von Zelllinien und Biosimilar-Programme.
Medizinische Geräte
ISO 13485-konforme Qualitätssysteme, Gerätehistorienaufzeichnungen und CAPA-Management für Geräte der Klassen I–III.
Gen- und Zelltherapie
Spezielle Chargenprotokolle, Chain-of-Custody-Verfolgung und Rückverfolgbarkeit von Vene zu Vene für fortschrittliche Therapien.
CROs und CDMOs
Multi-Client-Projektmanagement, flexible Methodenvalidierung und schnelles Site-Onboarding für Vertragslabore.
Nutrazeutika
Formulierungsmanagement, Stabilitätsstudien und Unterstützung bei der Einreichung von Zulassungsanträgen für Nahrungsergänzungsmittel und funktionelle Lebensmittel.
Echte GxP-Compliance-Ergebnisse von echten Pharmakunden
Erfahren Sie, wie führende Pharmaunternehmen ihre Abläufe mit AmpleLogic transformiert haben.

Bharat-Serum
60 % schnellere APQR-Berichte mit vollständiger Compliance
Bharat Serum hat seinen jährlichen Produktqualitätsprüfungsprozess umgestaltet und den manuellen Aufwand durch eine automatisierte, revisionssichere Berichtserstellung ersetzt.
AmpleLogic automatisierte, wofür unser Team früher wochenlange manuelle Kompilierung benötigte.

Cipla
Zentralisierter Benutzerzugriff auf mehr als 15 Standorte
Cipla implementierte eine zentralisierte Benutzerzugriffsverwaltung in seinen weltweiten Betrieben und sorgte so für Datenschutz und kontinuierliche Prüfungsbereitschaft.
Eine einzige Plattform für den Benutzerzugriff auf alle unsere Produktionsstandorte war bahnbrechend.

P&G
Von Papier-Logbüchern bis hin zu vollständig digitalen Abläufen
P&G verzichtet vollständig auf papierbasierte Logbücher und stellt in allen Produktionsstätten auf elektronische Logbücher um, die vollständig 21 CFR Part 11 entsprechen.
Der Übergang von Papier zu Digital verlief nahtlos – unsere Betreiber haben ihn innerhalb weniger Tage übernommen.
Hören Sie auf, 10 Pharmalösungsanbieter zu verwalten. Nutzen Sie eine einzige21 CFR Part 11-konforme Life-Sciences-Plattform.
Schließen Sie sich über 120 Pharmaunternehmen an, die Qualität, Labor und Fertigung auf AmpleLogic vereinheitlicht haben. Sehen Sie den Unterschied in 30 Minuten.
Oder erreichen Sie uns direkt unter info@amplelogic.com · Gebührenfrei: 1800-2023-269
Bleiben Sie in den Biowissenschaften an der Spitze
Erhalten Sie die neuesten Produktaktualisierungen, Compliance-News und Brancheneinblicke in Ihren Posteingang.
