Verfolgen Sie jede Einreichung und Registrierung weltweit
Speziell entwickeltes System zur Verwaltung regulatorischer Informationen für Arzneimittel – automatisieren Sie Einreichungen, verfolgen Sie ANDA- und DMF-Anträge und verwalten Sie die Lebenszyklen von Arzneimittelprodukten in über 120 Ländern mit KI-gestützter Software zur Einhaltung gesetzlicher Vorschriften.
120+
Unterstützte Länder
50%
Schnellere Einreichungen
100%
Audit-bereit
24/7
Compliance-Überwachung
RIMS-Herausforderungen: Warum das manuelle Regulierungsmanagement zu kurz kommt
Kritische Herausforderungen, die Compliance, Einreichungen und Marktzugang behindern
Sich ständig weiterentwickelnde globale Vorschriften
Um mit FDA, EMA, MHRA, CDSCO, WHO, Health Canada, TGA und über 100 regionalen Behörden Schritt zu halten, sind kontinuierliche Wachsamkeit und schnelle Anpassung erforderlich.
Fragmentierte regulatorische Daten
Kritische regulatorische Informationen, die über E-Mails, Tabellenkalkulationen, freigegebene Laufwerke und Altsysteme verstreut sind, schaffen blinde Flecken und Compliance-Lücken.
Komplexe Einreichungsformate
Die Verwaltung von eCTD, ACTD, NeeS und papierbasierten Einreichungen in verschiedenen Regionen erfordert spezielles Fachwissen und eine fehleranfällige manuelle Koordination.
Schlechte Sichtbarkeit und Nachverfolgung
Kein einheitliches Dashboard für den Echtzeitstatus globaler Einreichungen, Genehmigungen, Abfragen und Verlängerungszeitpläne in allen Märkten.
Manuelle und fehleranfällige Prozesse
Die starke Abhängigkeit von E-Mail-Kommunikation, manueller Dateneingabe und nicht verbundenen Tabellenkalkulationen erhöht das Risiko von Fristüberschreitungen und behördlichen Strafen.
Integrationsherausforderungen
Nicht verbundene QMS-, DMS-, ERP- und Sicherheitssysteme führen zu Datenduplizierung, Inkonsistenzen und langsamen funktionsübergreifenden Regulierungsabläufen.
Probleme mit der Skalierbarkeit
Wachsende Produktportfolios in verschiedenen Regionen erhöhen die regulatorische Komplexität exponentiell und überfordern manuelle Nachverfolgungsansätze.
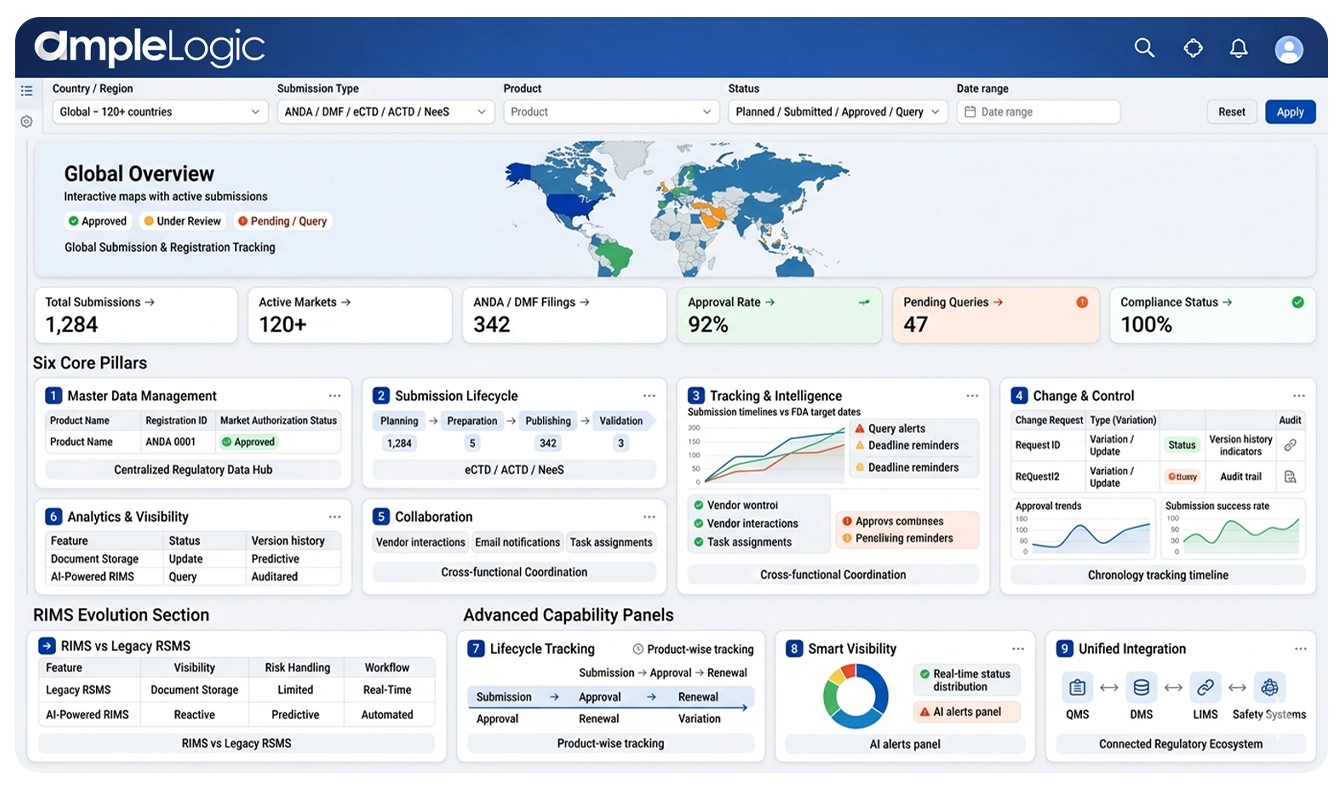
Übersicht über die AmpleLogic RIMS-Software
Sechs Säulen ermöglichen ein durchgängiges regulatorisches Lebenszyklusmanagement
Stammdatenverwaltung
Zentralisierte Produktregistrierung, globale Marktzulassung und Lebenszyklusverfolgung über alle Regulierungsbehörden hinweg.
Einreichungslebenszyklus
Automatisierte Arbeitsabläufe für die Planung, Vorbereitung, Veröffentlichung und Validierung von eCTD-, ACTD- und NeeS-Einreichungen mit ANDA- und DMF-Tracking.
Tracking und Intelligenz
Echtzeit-Einreichungsstatus, Genehmigungs- und Anfragemanagement, FDA-Zieltermine und proaktive Fristenüberwachung in allen Märkten.
Veränderung und Kontrolle
Änderungskontrolle, Variationsmanagement und kontinuierlicher Verbesserungsprozess (KVP) mit vollständigen Audit-Trails und Versionsverlauf.
Zusammenarbeit
Lieferantenkoordination, Kundenbenachrichtigung und automatisierte E-Mail-Benachrichtigungen für nahtlose funktionsübergreifende regulatorische Arbeitsabläufe.
Analytik und Sichtbarkeit
Grafische Dashboards, Chronologieverfolgung, Lebenszyklusanalysen und Compliance-fähige Informationen für fundierte regulatorische Entscheidungen.
RIMS: Die nächste Entwicklung von RSMS
Während ältere RSMS-Plattformen passive Dokumentenspeicher waren, ist RIMS ein intelligentes, KI-gestütztes Ökosystem für das Regulierungsmanagement, das aktiv die Einhaltung von Vorschriften vorantreibt, Risiken vorhersagt und die Markteinführungszeit beschleunigt.
Datenmanagement
Vollständige Produktregistrierung und globale Regulierungsdaten in einem zentralen System mit Stammdatenverwaltung und Lebenszyklusverfolgung.
Lebenszyklusverfolgung
Überwachung von Genehmigungen, Änderungen und Erneuerungen, um die kontinuierliche Einhaltung gesetzlicher Vorschriften auf allen Märkten sicherzustellen.
Intelligente Sichtbarkeit
Globale Transparenz in Echtzeit und proaktive Überwachung durch intelligente Warnungen und Compliance-Dashboards.
Einheitliche Integration
Nahtlose Integration mit QMS-, DMS-, LIMS- und Sicherheitssystemen zum Aufbau eines einheitlichen Ökosystems für das Regulierungsmanagement.
RIMS-Workflow-Module: Submission Lifecycle Management
Acht miteinander verbundene Module leiten regulatorische Prozesse von der Strategie bis zur laufenden Compliance
Regulatorische Datenstiftung
Globaler Marktaufbau und Stammdaten-Repository für DMF, CEP, LOA und Produktlebenszyklusverfolgung über alle Behörden hinweg.
Einreichungsplanung
Strategieentwicklung, Zeitplanung, Meilensteinverfolgung und Ressourcenzuweisung für globale Zulassungsanträge.
Vorbereitung der Einreichung
Dossierkompilierung, Versionskontrolle und Dokumentenzusammenstellung für eCTD-/ACTD-/NeeS-Bereitschaft mit automatisierten Validierungsprüfungen.
Einreichungsausführung
Validierung, Veröffentlichung bei Gesundheitsbehörden, Gateway-Einreichung, ANDA-Verfolgung und Überwachung des Behördenstatus in Echtzeit.
Bewertungsmanagement
Anfrageverfolgung, Mängelmanagement, behördliche Kommunikationsprotokolle und Überwachung des Reaktionszeitplans in allen Märkten.
Lebenszyklusmanagement von Arzneimitteln
Variationen, Erneuerungen, Änderungen nach der Genehmigung und Etikettenaktualisierungen mit vollständiger Lebenszyklusverfolgung und automatischen Warnungen.
Compliance-Überwachung
Automatisierte Warnungen, Verpflichtungsverfolgung, Inspektionsbereitschaft und proaktive Informationen zu regulatorischen Änderungen.
Analysen und Berichte
Echtzeit-Dashboards, grafische Berichte, Einblicke in globale Einreichungen und GDUFA-/behördenspezifische Analysen.

End-to-End-Orchestrierung
Jedes Workflow-Modul lässt sich nahtlos in QMS-, DMS-, LIMS- und Sicherheitssysteme integrieren, wodurch Datensilos und manuelle Übergaben über den gesamten regulatorischen Lebenszyklus hinweg vermieden werden.
Hauptmerkmale der AmpleLogic RIMS-Software
Zwölf entscheidende Funktionen ermöglichen regulatorische Exzellenz
Verfolgung der Produktregistrierung
Verfolgen Sie Produktregistrierungen in über 120 Ländern mit automatischen Statusaktualisierungen, Fristwarnungen und einem vollständigen Lebenszyklusmanagement für Arzneimittel.
Vorbereitung und Veröffentlichung der Einreichung
Genehmigungs- und Ablehnungsüberwachung
ANDA Tracker und FDA-Zieldaten
DMF-Tracker und Änderungskontrolle
Commitment- und Variationsmanagement
Lieferanten- und Stakeholder-Management
Grafische Berichte und Dashboards
Automatisierte Arbeitsabläufe bei der Pharmaregulierung
Elektronische Signaturen und Prüfprotokolle
Zentralisiertes Dokumenten-Repository
Einreichungsvalidierungs-Engine
KI-gestütztes RIMS: Intelligente regulatorische Analysen
Sechs KI-gestützte Funktionen beschleunigen regulatorische Arbeitsabläufe und reduzieren Risiken
KI-Compliance-Tracking
Überwacht kontinuierlich die Entwicklung lokaler und globaler regulatorischer Standards und passt sich diesen an. Dabei werden Prozesse automatisch aktualisiert, um die Einhaltung ohne manuelle Eingriffe sicherzustellen.
Prädiktive Analytik
Analysiert historische und Echtzeitdaten, um potenzielle Risiken und Compliance-Lücken zu identifizieren, bevor sie eskalieren, und hilft so, proaktiv Probleme zu entschärfen und Strafen zu vermeiden.
Automatisierte Berichterstattung
KI automatisiert die Erstellung von Regulierungsberichten und Dokumentationen und stellt sicher, dass diese mit minimalem menschlichen Eingriff korrekt, zeitnah und revisionssicher sind.
Risikominderungs-Engine
KI-gestützte Algorithmen bewerten Datenmuster, um potenzielle Compliance-Risiken zu erkennen, bieten prädiktive Erkenntnisse und empfehlen Korrekturmaßnahmen.
Informationen zu regulatorischen Änderungen
Verfolgt und verarbeitet regulatorische Änderungen in Echtzeit und implementiert sie automatisch in Ihre Systeme, um eine kontinuierliche Einhaltung der neuesten Standards sicherzustellen.
Workflow-Optimierung
KI optimiert Arbeitsabläufe, minimiert Betriebskosten, beschleunigt regulatorische Prozesse und stellt eine konsistente Compliance auf allen Geschäftsebenen sicher.
Global Regulatory Tracker: FDA-, EMA- und RoW-Überwachung
Drei regionale Trackingmodule für eine umfassende Marktzulassung
USA FDA Regulatory Tracker
ANDA-Tracker und DMF-Tracker mit FDA-Lebenszyklusmeilensteinen, einschließlich IND-, NDA-, ANDA-, BLA-Zielaktionsterminen, GDUFA-Gebühren und 505(b)(2)-Einreichungen.
EU- und UK-Regulierungs-Tracker
Verwalten Sie EMA- und MHRA-Verfahren, zentralisierte/dezentrale/gegenseitige Anerkennungsvarianten, PSUR-Zeitpläne und Post-Brexit-Einreichungen im Vereinigten Königreich mit automatisierten Arbeitsabläufen.
Globaler RoW Regulatory Tracker
Optimieren Sie APAC-, LATAM-, MENA- und Afrika-Einreichungen mit länderspezifischer Lebenszyklusverfolgung für Health Canada, TGA, CDSCO, WHO PQ und über 100 Behörden.
RIMS-Konformität: Globale Regulierungsstandards
Volle Unterstützung für globale Regulierungsrahmen und Compliance-Standards
Unterstützung durch große Behörden
Vollständige Abdeckung für die US-amerikanische FDA, EMA, MHRA, WHO, Health Canada, TGA, CDSCO, ANVISA, PMDA und über 100 globale Gesundheitsbehörden.
Multiregionales Formatmanagement
Native Unterstützung für eCTD, ACTD, NeeS und papierbasierte Formate mit automatischer Verlängerungsüberwachung und formatspezifischer Validierung.
21 CFR Part 11 & EU Annex 11
Vollständig konforme Kontrollen, einschließlich elektronischer Signaturen, Prüfpfade, Datenintegritätsschutz und sichere Versionskontrolle.
Proaktive Überwachung und Warnungen
Automatisierte Benachrichtigungen zu Fristen, Fälligkeitsterminen von Verpflichtungen, Verlängerungsfenstern und regulatorischen Änderungen mit Risikominderung in Echtzeit.
IDMP-Bereitschaft
Unterstützt ISO-IDMP-Standards für Stoff-, Produkt-, Organisations- und Referenzdaten zur Vorbereitung auf die Identifizierungsanforderungen der EMA.
Bereit für ICH eCTD 4.0
Zukunftssicher für das eCTD 4.0-Datenmodell der nächsten Generation mit strukturierter Inhaltsplanung, Metadatenverwaltung und Funktionen zur Einreichung von Behörden.
AmpleLogic RIMS im Vergleich zu Mitbewerbern
Wie AmpleLogic ältere RIMS- und Punktlösungen übertrifft
| Fähigkeit | AmpleLogic-FELGEN | Konkurrentinnen |
|---|---|---|
| Architektur | Low-Code/No-Code auf einheitlichem aPaaS | Starre Architektur, umfangreiche Anpassung erforderlich |
| Datenansatz | Einheitliches Stammdaten-Repository | Fragmentierte Daten über Module und Silos hinweg |
| Lebenszyklusabdeckung | End-to-End (Verfolgung von der Planung bis zur Nachverfolgung der Genehmigung) | Erfordert oft separate Zusatzmodule |
| Integration | Nahtlos (QMS, DMS, ERP, Sicherheit, LIMS) | Eigenständig, hoher Integrationsaufwand |
| Automatisierung und KI | KI-gestützte Warnungen, prädiktive Analysen, automatische Berichte | Begrenzte Automatisierung, statische manuelle Arbeitsabläufe |
| Gesamtbetriebskosten | Niedrigere Gesamtbetriebskosten, schnelle Bereitstellung, Pay-as-you-grow | Hohe Lizenzgebühren und laufende Wartungskosten |
| Bereitstellungsgeschwindigkeit | Wochen mit vorab validierten Vorlagen | Monate bis Jahre der Umsetzung |
| eCTD 4.0-Bereitschaft | Zukunftssicher mit strukturiertem Datenmodell | Roadmap-abhängiger, ungewisser Zeitplan |
RIMS Enterprise-Integrationen
Zehn Integrationsmodule, die Regulierungs-, Qualitäts- und Fertigungssysteme verbinden
eQMS
Bidirektionale Änderungskontrolle, CAPA und Abweichungsverknüpfung
DMS
Versionskontrollierte Regulierungsdokumente und SOPs
LMS
Schulungsaufzeichnungen und Kompetenzmanagement
LIMS
Analytische Daten und CoA-Integration für Einreichungen
eLogbuch
GxP-Logbuchdaten verknüpft mit behördlichen Aufzeichnungen
eBMR/MES
Batch-Datensatzdaten für behördliche Einreichungen
CVS
Reinigungsvalidierungsdaten für behördliche Einreichungen
KAPPEN
Aufzeichnungen zur Gerätekalibrierung zur Gewährleistung der Konformität
SAP/Oracle
Synchronisierung von Materialstamm- und Lieferkettendaten
PV
Daten zu unerwünschten Ereignissen und PSUR/PBRER-Integration
ROI von RIMS: Messbare regulatorische Auswirkungen
Quantifizierte Auswirkungen des KI-gestützten regulatorischen Lebenszyklusmanagements
Vorbereitung der Einreichung
50-60 % schnellerManueller Prozess
8-12 Wochen
Mit AmpleLogic RIMS
3-5 Wochen
Eingabe behördlicher Daten
75 % ErmäßigungManueller Prozess
40+ Stunden/Woche
Mit AmpleLogic RIMS
8-10 Stunden/Woche
Fristeneinhaltung
Nahezu null verpasste FristenManueller Prozess
85-90 % Pünktlichkeit
Mit AmpleLogic RIMS
Über 99 % pünktlich
Antwortzeit der Abfrage
70 % schnellere ReaktionManueller Prozess
5-10 Werktage
Mit AmpleLogic RIMS
1-3 Werktage
Audit-Vorbereitung
90 % ZeitersparnisManueller Prozess
2-4 Wochen
Mit AmpleLogic RIMS
Stunden (immer bereit)
Berichtserstellung
95 % schnellerManueller Prozess
3-5 Tage pro Bericht
Mit AmpleLogic RIMS
Minuten (automatisch generiert)
Im Gartner-Bericht vorgestellt
AmpleLogic RIMS wurde im Gartner® Market Guide for Life Science Regulatory Information Management Solutions, September 2024 (ID G00769345) als repräsentativer Anbieter anerkannt.
Von AmpleLogic RIMS bediente Branchen
Acht Branchenvertikale nutzen AmpleLogic RIMS für regulatorische Exzellenz
Arzneimittel
GMP-konforme Regulierungssoftware für die Arzneimittelregistrierung, NDA/ANDA-Anträge und globale Marktzulassung mit vollständigem Lebenszyklusmanagement
Biotechnologie
BLA-Einreichungen, Biosimilar-Registrierungen und komplexes Lebenszyklusmanagement biologischer Produkte
Medizinische Geräte
510(k), PMA, CE-Kennzeichnung, EUDAMED/UDI-Einreichungen und Geräteklassifizierungsmanagement
Gentherapie
IND/BLA-Einreichungen für neuartige Therapien mit spezieller Verfolgung regulatorischer Pfade
API-Hersteller
DMF-Tracker für CEP-Anwendungen und globale API-Registrierung über Behörden hinweg
Lebensmittel und Getränke
Registrierung von Lebensmittelzusatzstoffen, Anträge auf neuartige Lebensmittel und Einreichung gesundheitsbezogener Angaben
Cannabis und Tabak
Spezialisierte behördliche Verfolgung von Cannabis-Lizenzen und Einreichungen für Tabakprodukte
Kosmetika
Benachrichtigungen zu kosmetischen Produkten, CPNP/FDA-Registrierungen und Verfolgung der Einhaltung der Inhaltsstoffe
Sind Sie bereit, Ihre regulatorischen Abläufe zu transformieren?
Ersetzen Sie fragmentierte Tabellenkalkulationen und manuelle Nachverfolgung durch KI-gestützte, revisionssichere regulatorische Informationen.
Bleiben Sie in den Biowissenschaften an der Spitze
Erhalten Sie die neuesten Produktaktualisierungen, Compliance-News und Brancheneinblicke in Ihren Posteingang.