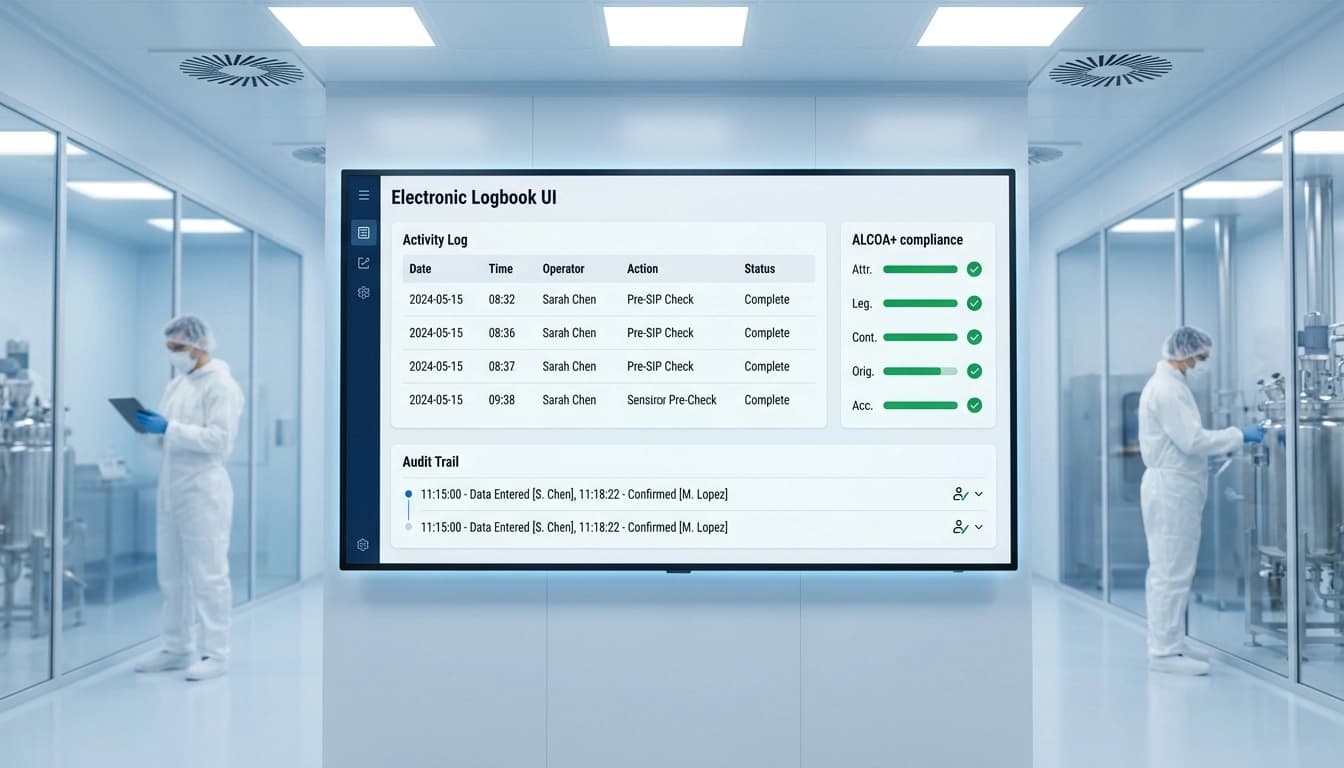
Dans l'industrie pharmaceutique, le maintien de l'intégrité des données est crucial pour garantir la qualité des produits, la sécurité des patients et la conformité réglementaire. L'intégrité des données désigne l'exactitude et la cohérence des données tout au long de leur cycle de vie. Les cahiers de bord électroniques sont devenus des outils essentiels pour maintenir la conformité ALCOA+.
Les cahiers de bord électroniques remplacent les cahiers de bord papier utilisés dans l'ensemble des opérations pharmaceutiques — des journaux d'utilisation des équipements et des registres de nettoyage aux relevés de surveillance environnementale et aux journaux d'accès aux zones. Le format numérique garantit que les entrées sont automatiquement horodatées, attribuées à des utilisateurs spécifiques et protégées contre toute modification non autorisée.
Les fonctionnalités clés en matière d'intégrité des données comprennent les signatures électroniques avec vérification biométrique, les pistes d'audit automatiques, les contrôles d'accès pour les utilisateurs simultanés, le stockage des enregistrements infalsifiable, ainsi que les procédures automatisées de sauvegarde et d'archivage.
La transition vers les cahiers de bord électroniques répond à de nombreuses observations FDA 483 courantes liées à l'intégrité des données — notamment l'antidatage des entrées, les modifications non autorisées et les enregistrements incomplets. Les organisations qui mettent en œuvre des cahiers de bord électroniques rapportent une meilleure préparation aux inspections et une réduction des constatations relatives à l'intégrité des données.