GAMP 解决方案
企业级 AI 驱动的 适用于每个制药工作流程的解决方案
为制药、生物技术和生命科学组织提供全面的经验证软件解决方案套件。
解决方案集成
面向生命科学的低代码 aPaaS — 统一集成架构
AmpleLogic 的各模块并非孤立运行。每个解决方案相互连接——共享数据、触发工作流程,并在质量、生产和 QC 实验室职能之间维护单一数据源。
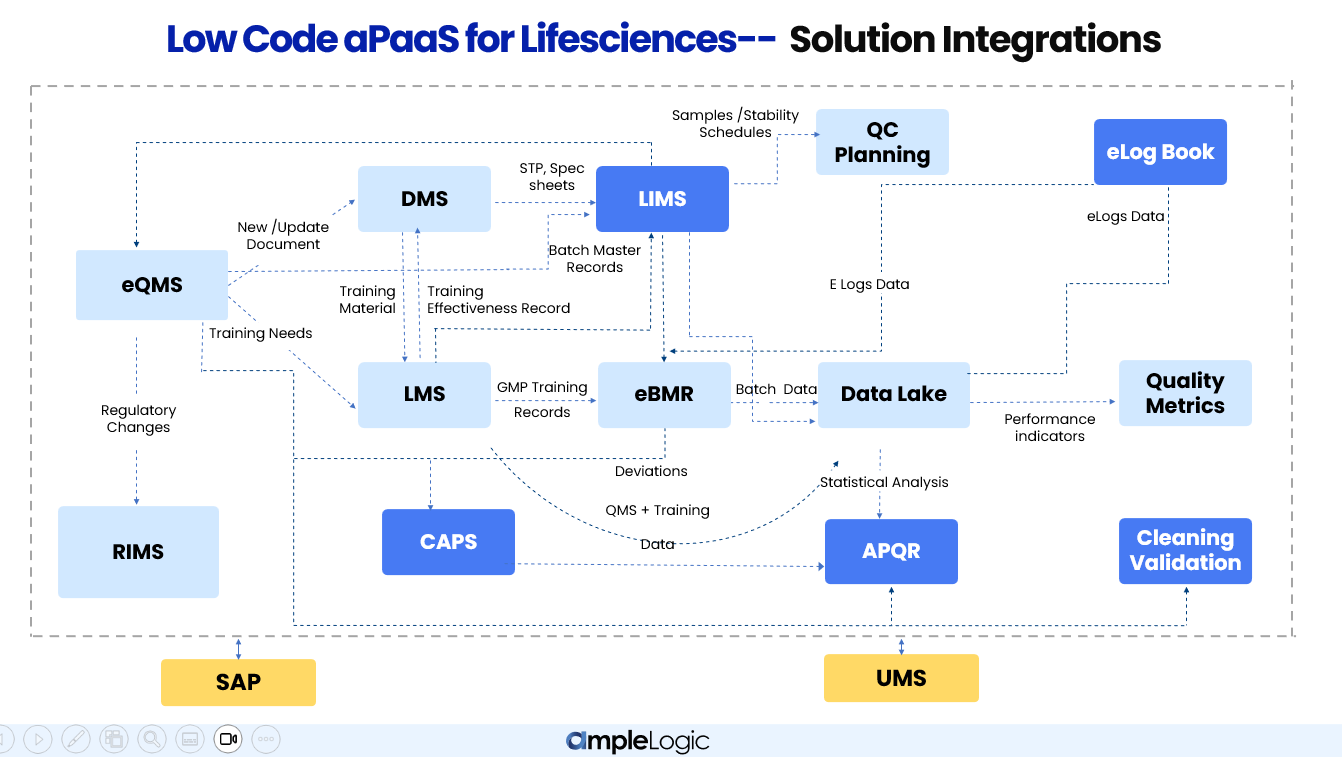
AmpleLogic 模块如何在制药公司的质量、生产和 QC 实验室职能之间集成
统一数据湖
所有模块将数据汇入集中式数据湖,无需手动整合数据,即可实现实时性能指标、质量指标及跨职能分析。
自动化工作流级联
单一事件(例如生产中的偏差)可自动在 eQMS 中触发 CAPA、在 DMS 中触发文件修订、在 LMS 中触发再培训,以及在 APQR 中触发影响评估。
双向数据流
数据在各模块之间双向流动。例如,LMS 将培训有效性记录回传至 eQMS,而 LIMS 将分析结果返回至 eBMR 用于批次放行。
集成如何跨职能运作
质量管理
eQMSDMSLMSAPQRUMS
质量管理生态系统确保每一项偏差、CAPA、变更控制和审计发现均得到端到端追踪。eQMS 处于核心位置——在 DMS 中触发文件工作流、在 LMS 中触发培训分配,并将统计数据输送至 APQR 用于年度产品质量回顾。
eQMSDMS
新建/更新文件
当 eQMS 中发起偏差或变更控制时,DMS 自动启动 SOP 修订工作流,确保文件随每一质量事件保持更新。
eQMSLMS
培训需求
新建或修订的 SOP 会在 LMS 中自动触发培训分配。培训有效性记录回流至 eQMS,以闭合质量管理环路。
Data LakeAPQR
统计分析
批次数据、偏差、CAPA 记录和工艺参数在数据湖中汇总,并输送至 APQR 以进行全面的年度产品质量回顾。
CAPSAPQR
QMS 与培训数据
来自 CAPS 的校准偏差和预防性维护记录流入 APQR,提供设备和仪器对产品质量影响的完整视图。
引领生命科学前沿
获取最新产品更新、合规动态及行业洞察,直接发送至您的邮箱。