エンタープライズAI搭載 あらゆる製薬ワークフローに対応するソリューション
製薬、バイオテク、ライフサイエンス企業向けの包括的な検証済みソフトウェアソリューション群。
ライフサイエンス向けローコードaPaaS — 統合アーキテクチャ
AmpleLogicのモジュールはサイロで動作しません。すべてのソリューションが相互接続されており、データを共有し、ワークフローをトリガーし、品質・製造・QCラボ機能全体で唯一の情報源を維持します。
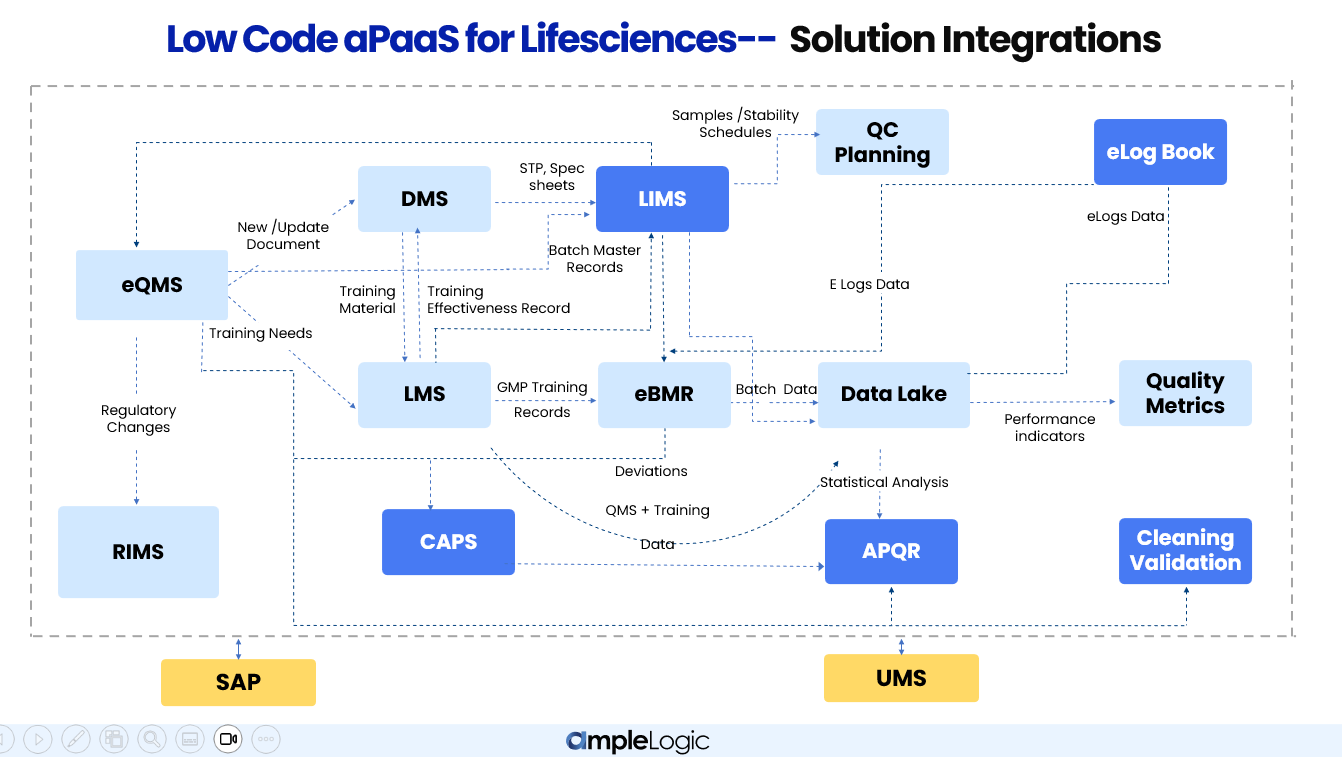
AmpleLogicモジュールが製薬企業の品質・製造・QCラボ機能全体で統合される仕組み
統合データレイク
すべてのモジュールが集中型データレイクに情報を供給し、手動のデータ統合なしにリアルタイムのパフォーマンス指標、品質メトリクス、クロスファンクショナル分析を実現します。
自動化ワークフローカスケード
製造における逸脱などの単一イベントが、eQMSのCAPA、DMSのドキュメント改訂、LMSの再トレーニング、APQRの影響評価を自動的にトリガーします。
双方向データフロー
モジュール間でデータが双方向に流れます。例えば、LMSはトレーニング有効性記録をeQMSに送り返し、LIMSはバッチリリースのために分析結果をeBMRに返します。
機能横断的な統合の仕組み
品質管理
品質管理エコシステムは、すべての逸脱、CAPA、変更管理、監査所見のエンドツーエンドの追跡を確保します。eQMSが中心となり、DMSのドキュメントワークフロー、LMSのトレーニング割り当てをトリガーし、年次製品品質レビューのために統計データをAPQRに供給します。
ドキュメントの新規作成・更新
eQMSで逸脱または変更管理が提起されると、DMSが自動的にSOP改訂ワークフローを開始し、すべての品質イベントに応じてドキュメントが最新状態に保たれます。
トレーニングニーズ
新規または改訂されたSOPは、LMSのトレーニング割り当てを自動的にトリガーします。トレーニング有効性記録はeQMSに送り返され、品質ループを完結させます。
統計分析
バッチデータ、逸脱、CAPA記録、プロセスパラメータがデータレイクに集約され、包括的な年次製品品質レビューのためにAPQRに供給されます。
QMS・トレーニングデータ
CAPSからの校正逸脱および予防保全記録がAPQRに流れ込み、製品品質への設備・機器の影響を包括的に把握できます。
ライフサイエンスの最前線へ
最新の製品アップデート、コンプライアンスニュース、業界インサイトをお届けします。