紙のバッチ記録があなたのビジネスを阻む理由
手動の eBMR/MES システムは、コンプライアンスリスクから生産遅延まで、製造オペレーション全体に構造的なリスクをもたらします。
ヒューマンエラーと改ざんリスク
手書きの紙記録は転記ミス、記入漏れ、データ改ざんが起こりやすく、ファーマ MES ソフトウェアと電子バッチ製造によりバッチ製造自動化を通じてこれらのリスクを排除します。
エラーが生じやすいバッチデータ
紙に記録された製品・バッチデータはリアルタイムの生産監視ができないため、仕様外の不合格や手直しが発生しますが、医薬品製造ソフトウェアがこれを防ぎます。
リアルタイム可視性の欠如
紙ベースのシステムはライブの生産状況を提供できませんが、リアルタイム生産監視と設備効率モニタリングを備えたデジタル製造プラットフォームが遅延レポートや現場巡回に取って代わります。
困難な監査・査察対応
FDA/MHRA 査察時に紙記録を取得・集約・検証するには膨大な時間がかかりますが、GxP 準拠の MES と GMP 製造ソフトウェアが即座の監査準備を可能にします。
コンプライアンスとセキュリティのギャップ
紙には 21 CFR Part 11 が要求する強固なアクセス制御、改ざん防止監査証跡、電子署名が欠如していますが、このライフサイエンス MES プラットフォームがすべてのコンプライアンスギャップを解消します。
限られた連携と遅延
部門間の紙の引き継ぎはバッチ実行を遅らせますが、自動化されたファーマ規制ワークフローと製造現場実行システムの機能がボトルネックを排除します。
信頼性の低い原材料トレーサビリティ
手動の原材料ログは不整合につながりますが、バーコード照合による計量スケール連携が正確な分注記録と収率調整を保証します。
標準維持の難しさ
紙の SOP とマスター記録を最新の状態に保つことは運用コストが高くなりますが、ローコード製造アプリケーションによるレシピ管理が製品・拠点をまたいだ更新を簡素化します。
完全な製造実行 — 単一プラットフォーム
マスターレシピの作成からバッチ実行、品質チェック、リリースまで、すべてのモジュールが単一のデータレイヤー上で連携します。
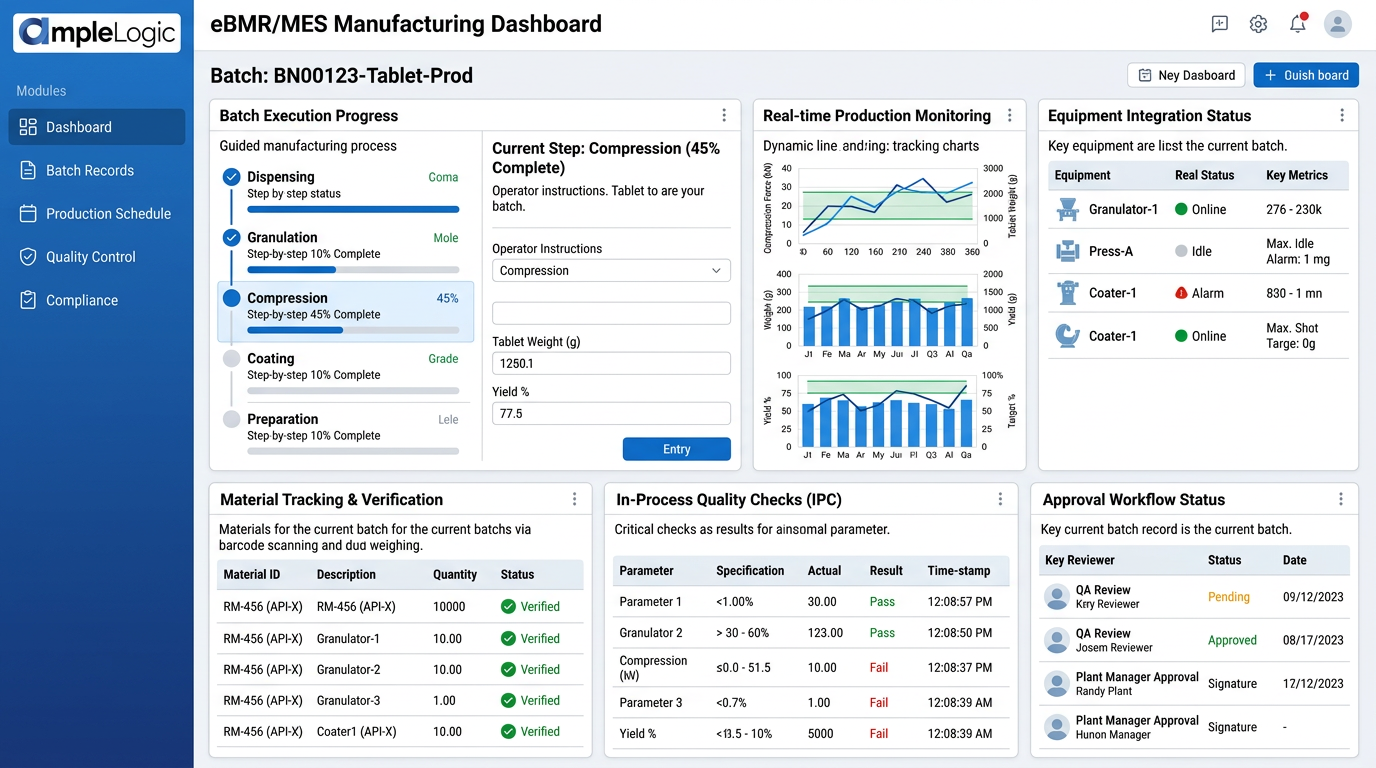
実行とリアルタイム生産監視
リアルタイム生産監視、ステップバイステップのガイドプロセス、ライブ生産ダッシュボード、設備効率モニタリング、および設備からの自動データ収集を備えた製造現場実行システム(ファーマ MES ソフトウェア)。
エンタープライズグレードの製造機能
準拠した、効率的で、ペーパーレスな製造フロアを運営するために必要なすべての機能。
リアルタイムデータ収集と生産監視
設備、PLC、計器からの自動データ収集を備えたファーマ MES ソフトウェア — このデジタル製造プラットフォームでリアルタイム生産監視と設備効率モニタリングにより手動転記を排除します。
設備連携(PLC/HMI/SCADA)
このスマートファクトリープラットフォームで、OPC、Historian データベース、標準 PLC プロトコルを介したリアルタイムプロセスデータの直接連携を備えた製造現場実行システム。
電子署名と監査証跡
この GMP 製造ソフトウェアで、21 CFR Part 11 準拠の電子署名と、すべてのアクション、変更、承認に対する改ざん防止タイムスタンプ付き監査証跡を備えた GxP 準拠 MES。
自動化されたワークフロー管理
この医薬品製造ソフトウェアで、設定可能な多段階承認ワークフロー、自動ルーティング、エスカレーション、並列・逐次処理を備えたバッチ製造自動化。
例外レビュー
このライフサイエンス MES プラットフォームで、QA レビューのために例外と逸脱のみをハイライトする AI 駆動の製造インサイトにより、バッチリリースを大幅に加速します。
リマインダーとエスカレーションアラート
保留中のタスク、バッチ承認ステージ、期限超過のアクティビティ、および管理者へのエスカレーションに対する自動メールアラートを備えたクラウド MES プラットフォーム。
製品ラベル管理
すべての製品ラベルの一貫性、バージョン管理、および規制準拠を確保する一元化されたラベル管理を備えたデジタル製造プラットフォーム。
包装部品管理
設定可能な部品表、部品トレーサビリティ、および調整を含む、製品ごとの多様な包装要件に対応する医薬品製造ソフトウェア。
ローコード製造アプリケーション
カスタムコーディング不要でファーマ製造デジタル化を実現する、プロセスのカスタマイズのための直感的なドラッグ&ドロップインターフェースを備えたローコード製造アプリケーション。
高度な生産スケジューリング
リソース配分を最適化し、切り替え時間を最小化し、スループットを最大化する Industry 4.0 製造スケジューリングアルゴリズムを備えたスマートファクトリープラットフォーム。
スケーラブルなクラウド MES プラットフォーム
100%カスタマイズ可能なクラウド MES プラットフォーム — バイオファーマ製造プラットフォームのニーズに合わせて、単一ラインから企業全体のマルチサイト展開まで拡張可能。
完全な生産ライフサイクルの可視性
計画からバッチリリース、保管に至る生産ライフサイクル全体にわたるエンドツーエンドの可視性と制御によるデジタル製造変革。
マスター設定からバッチリリースまで
レシピ作成から最終バッチ承認まで、製造プロセスを導く構造化されたエンドツーエンドのフロー。
マスター設定
- マスターの作成(製品、原材料、設備、部屋)
- 製品・ステージマッピング
- 原材料と製品のマッピング
- 部屋・設備マッピング
- 逐次・並列プロセスの定義
レシピとスケジューリング
- マスターレシピの作成(ドラッグ&ドロップ)
- 生産スケジューリングとリソース配分
- バッチ計画と発行
バッチ実行
- バーコード照合による原材料の分注
- ステップバイステップのガイド付きバッチ実行
- 設備連携と自動データ収集
- 工程内品質チェックと試験結果
- 部屋・設備ログエントリー
レビューとリリース
- 例外処理と逸脱管理
- 電子署名と多段階承認
- より迅速なバッチリリースのための例外レビュー
- 完全な監査証跡とバッチ系譜
段階的な移行:紙から完全 eBMR へ
BIMS(バッチ記録発行管理)
- マスターコピーのバージョン管理と文書発行
- 手動ミスを排除する自動印刷
- 母バッチ、共同包装、二層錠ロジック
- 数量管理(借方・貸方)
- 手動記録ミス、追加ページ要求、訂正に対する管理
電子バッチ記録
- 発行プロセスをオンラインワークフローに変換
- バッチ情報をオンラインで記録(ハードコピーから移行)
- 設備でのみ記録が行われることを確認する措置
- eQMS システムとの連携
完全 eBMR
- 手動記録から設備による自動データ入力への移行
- PLC、HMI、SCADA とのリアルタイムデータ連携
- 完全なペーパーレス製造フロア
- 21 CFR Part 11 / EU Annex 11 への完全準拠
製造現場の実行を簡素化
製造フロアのオペレーターのために設計 — 直感的で、ガイド付きで、エラーのない操作を実現。
ガイド付きプロセス
製造ステップを実行するためのユーザーフレンドリーなステップバイステップの指示を備えた製造現場実行システム — オペレーターはこのファーマ MES ソフトウェアで直感的なプロンプトに従い一貫性を確保します。
リアルタイム生産監視
このデジタル製造プラットフォームで設備効率モニタリングを備え、オペレーターが現在のアクティビティ状況を一目で把握できるアニメーションビジュアルキューとステータスアイコンによるリアルタイム生産監視。
自動バリデーション
誤入力、仕様外の値、および欠落ステップに対するシステム警告で、電子バッチ製造記録に到達する前にエラーを防ぐバッチ製造自動化。
オンスクリーン SOP
実行中の即時参照のために、使用時点で SOP を画面上に直接表示する GMP 製造ソフトウェア。
アクティビティガイダンスと次のステップ
このライフサイエンス MES プラットフォームで、オペレーターが常にプロセスの次のステップを把握できるよう、各タスクの次のステップに対する明確な指示を提供するスマートファクトリープラットフォーム。
バーコードとQRスキャン
Industry 4.0 製造現場で、原材料の照合、設備の識別、およびエラーのないデータ入力のための計量スケール連携と統合されたバーコード/QRスキャン。
オペレーション全体とシームレスに連携
品質、ラボ、トレーニング、設備、エンタープライズシステム全体でネイティブ連携 — すべて一つのプラットフォームで。
品質システム
- eQMS(CAPA、逸脱、変更管理)
- OOS/OOT 管理
- 監査管理
- 苦情処理
ラボラトリー
- LIMS(工程内試験、CoA)
- 安定性試験
- 環境モニタリング(EMS)
文書・トレーニング
- DMS(SOP、マスター記録)
- LMS(オペレータートレーニング、能力評価)
- 電子ログブック(eLogs)
設備・自動化
- PLC / HMI / SCADA 連携
- OPC サーバー接続
- Historian データベース
- 計量・分注システム
エンタープライズシステム
- SAP / Oracle ERP
- 倉庫管理(WMS)
- サプライチェーン管理
- 財務システム
校正・保守
- CAPS(校正スケジューリング)
- 予防保全
- 設備適格性評価
- 資産ライフサイクル管理
AmpleLogic MES の比較
AmpleLogic が従来型、エンタープライズ型、自動化中心の MES ソリューションとどのように異なるかをご覧ください。
| 機能 | AmpleLogic | クラウド MES | エンタープライズ MES | オートメーション MES |
|---|---|---|---|---|
| 導入スピード | 数週間(ローコード aPaaS) | 数ヶ月(クラウド SaaS) | 6〜18ヶ月(オンプレ/クラウド) | 6〜12ヶ月(オンプレ/クラウド) |
| カスタマイズ性 | 100% ドラッグ&ドロップ、コーディング不要 | テンプレートベースの設定 | プロフェッショナルサービスが必要 | システムインテグレーターが必要 |
| レシピ管理 | ビジュアルドラッグ&ドロップビルダー | テンプレート駆動の EBR | レシピ駆動の ISA-88 エンジン | レシピ管理モジュール |
| 設備連携 | OPC 経由の PLC/HMI/SCADA | 限定的(QMS 中心) | 深い ISA-95 / OPC-UA | ベンダー固有の PLC エコシステム |
| 品質システム連携 | ネイティブ(同一プラットフォーム) | ネイティブ QMS + EBR | サードパーティ連携 | サードパーティ連携 |
| 統合プラットフォーム | 単一 aPaaS 上に14以上のアプリ | QMS + 製造のみ | MES のみ(クローズドエコシステム) | MES のみ(ベンダーエコシステム) |
| インフラコスト | 最大70%低減(オープンソース) | クラウドサブスクリプションモデル | 高(エンタープライズライセンス) | 高(プラットフォーム+インテグレーター) |
| 継続的な製品アップグレード | 含まれる、定期リリース | クラウド自動更新 | バージョンアップグレード(プロジェクトベース) | メジャーバージョンリリース |
ローコードによる100%カスタマイズ
このファーマ MES ソフトウェアで、カスタムコーディング不要であなたの製造要件に完全に合わせた、すべてのワークフロー、フォーム、プロセスを設定可能なローコード製造アプリケーション。
ドラッグ&ドロップのレシピビルダー
このデジタル製造プラットフォームで、プロセスエンジニアが IT 部門の関与なしにマスターレシピを構築・修正できるビジュアルレシピ作成ツールによるレシピ管理。
継続的アップグレードを備えたクラウド MES プラットフォーム
定期的な製品リリース、新機能、規制アップデート、パフォーマンス改善を備えたクラウド MES プラットフォーム — サブスクリプションに含まれるデジタル製造変革を実現。
Industry 4.0 への迅速な導入
従来の MES 実装で一般的な6〜18ヶ月ではなく、数週間での導入を可能にするスマートファクトリープラットフォームとライフサイエンス MES プラットフォームにより、ファーマ製造デジタル化を加速します。
ペーパーレス製造のビジネスケース
AmpleLogic eBMR/MES を導入した医薬品メーカーが達成した定量的な成果。
バッチリリースの高速化
例外レビューと自動化されたワークフローにより、紙ベースのプロセスと比較してバッチリリース時間を半減。
紙コストの削減
製造オペレーション全体で、紙のバッチ記録、印刷、保管、取得にかかるコストを排除。
データ入力エラーの削減
自動バリデーション、設備連携、ガイド付きプロセスにより、手動転記エラーを事実上排除。
インフラコストの低減
オープンソースのインフラスタック(Linux、PostgreSQL)により IT インフラ費用を大幅に削減。
投資対効果
顧客は通常、運用効率化を通じて導入後18ヶ月以内に3〜5倍の ROI を達成。
監査準備の高速化
完全な監査証跡を備えた改ざん防止電子記録への即時アクセスにより、査察準備を加速。
16以上のグローバル規制機関に準拠
初日からの規制準拠を前提に設計 — FDA 21 CFR Part 11、EU Annex 11、GAMP 5 など。
コンプライアンス基準
規制機関
USFDA
アメリカ
MHRA
イギリス
TGA
オーストラリア
CDSCO
インド
Health Canada
カナダ
MCC
南アフリカ
ANVISA
ブラジル
EMEA
欧州連合
SFDA
中国
MPA
スウェーデン
Swissmedic
スイス
MCAZ
ジンバブエ
MEDSAFE
ニュージーランド
MHLW
日本
NAFDAC
ナイジェリア
KFDA
韓国
規制対象製造向けに特化
医薬品製造
- 固形製剤(経口)
- 液剤・半固形製剤
- 無菌注射剤
- API 製造
- ファーマ製造デジタル化
バイオファーマ製造プラットフォーム
- 生物製剤製造
- 細胞培養
- 精製
- 充填・仕上げ
- バイオテク製造実行
医療機器
- 機器組立
- 包装・ラベリング
- 滅菌記録
- DHR 管理
CDMO / CMO
- 複数クライアントのバッチ記録
- キャンペーン製造
- 技術移転
- 迅速なサイトオンボーディング
- デジタル製造変革
ライフサイエンスの最前線へ
最新の製品アップデート、コンプライアンスニュース、業界インサイトをお届けします。