40%
試験セットアップの迅速化
100%
ICH コンプライアンス
30%
サンプルプル見落としの削減
60%
手動追跡の削減
50%
コスト削減
3–6
ヶ月での導入完了
安定性スケジュール管理とは?
安定性スケジュール管理とは、医薬品安定性試験の体系的な計画、実施、および追跡です。安定性試験プロトコルに定義されたとおり、すべての製品バッチが適切な保存条件、サンプリング時点、および分析試験を確実に受けられるようにし、ICH Q1A、FDA 21 CFR Part 211.166、およびGMP要件に準拠した正確な有効期間の決定と規制コンプライアンスを実現します。
安定性試験プロトコル
安定性試験プロトコルは、保存条件、時点、試験パラメータ、合格基準、および包装構成など、試験設計を定義します。AmpleLogicは、ICH Q1A準拠のテンプレートを用いてプロトコル作成を自動化します。
安定性スケジュールカレンダー
安定性スケジュールカレンダーは、すべてのアクティブな試験を横断したプル日程、チャンバー割り当て、および担当分析者の視覚的なタイムラインです。AmpleLogicはこのカレンダーをリアルタイムで自動生成・維持します。
安定性スケジュール管理
安定性スケジュール管理は、プロトコル承認からサンプルプル、試験実施、トレンド分析、有効期間の決定まで、ライフサイクル全体を単一のバリデーション済みプラットフォームで統合的に管理します。
自動化なしの安定性スケジュール管理における課題
安定性試験プロトコル管理および安定性スケジュールカレンダーの追跡に手動プロセスを利用している組織は、重大なリスクに直面しています。
手動による安定性スケジュール管理
チームはスプレッドシートと紙の記録に依存して安定性スケジュールを計画しており、サンプルプルの見落とし、スケジュールの競合、および試験タイムラインのリアルタイム可視性の欠如につながります。
一貫性のない安定性試験プロトコル
標準化されたシステムがない場合、安定性試験プロトコルの作成がチームやサイト間で異なり、規制上のギャップ、監査指摘事項、および不統一な試験設計を引き起こします。
一元化された安定性スケジュールカレンダーの欠如
統一された安定性スケジュールカレンダーがないと、分析者は今後のプル、チャンバー割り当て、または重複する試験を一か所で確認することができません。
環境データの分断
チャンバーの温度および湿度データが安定性試験とは別に追跡されており、トレーサビリティのギャップとエクスカーション対応の遅延を生じさせます。
トレンド分析および報告の遅延
安定性トレンド分析のための手動データ集計により、有効期間の決定、規制当局への申請、および製品上市のタイムラインが遅延します。
断片化したシステムによるコンプライアンスリスク
安定性プログラム管理に複数の分断されたツールを使用することで、データインテグリティリスクが高まり、ICH Q1AおよびFDA監査対応が困難になります。
安定性試験プロトコルおよびスケジュール自動化に対するAmpleLogicのアプローチ
手動の安定性スケジュール管理を完全に自動化されたICH準拠ワークフローへと変革する6つの統合ステップ。
安定性試験プロトコルの定義
設定可能な試験設計、保存条件、合格基準、および自動サンプリングスケジュールを含むICH Q1A準拠の安定性試験プロトコルを、単一のバリデーション済みシステムで作成します。
安定性スケジュールカレンダーの構築
時点プル日程、チャンバー割り当て、分析者配置、および自動リマインダーを含む視覚的な安定性スケジュールカレンダーを自動生成し、手動計画を完全に排除します。
チャンバー条件のモニタリング
自動エクスカーションアラート、センサー統合、および安定性試験記録に直接リンクされた環境データを含む、リアルタイムの温度・湿度モニタリング。
試験実施と結果の記録
直接機器接続、インライン計算、およびサンプルから結果までの完全なトレーサビリティを備えた統合LIMSワークフロー内で分析試験を実施します。
トレンド分析と有効期間の決定
劣化モデリング、統計的有効期間予測、有効期限の決定、および信頼区間レポートを含むAI搭載の安定性トレンド分析。
規制報告書の作成
安定性データから、ICH準拠の安定性報告書、FDA申請パッケージ、およびGMP安定性プログラム文書を自動生成します。
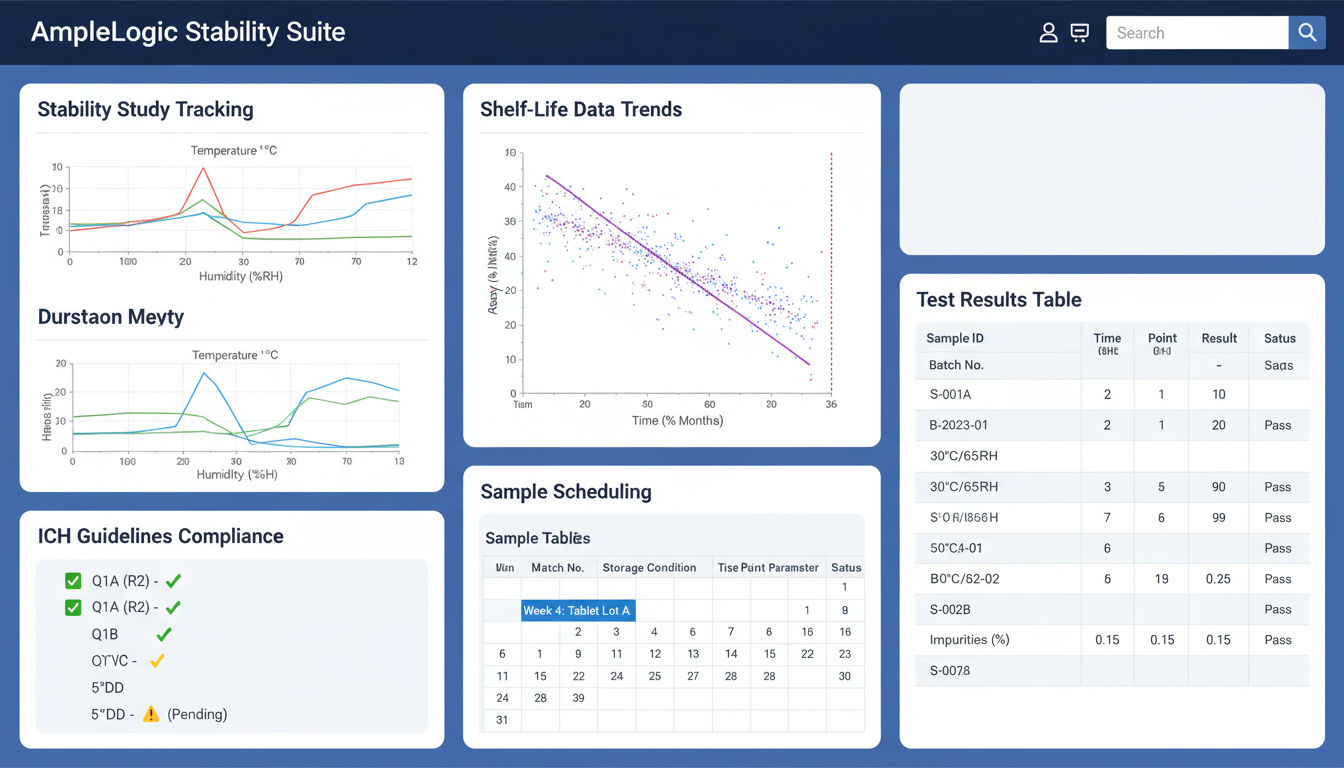
AmpleLogic 安定性スケジュールカレンダーおよびデータハブ
安定性試験プロトコル管理、安定性スケジュールカレンダー、トレンド分析、およびコンプライアンス文書を一か所に統合する一元化されたプラットフォーム。
統合試験ダッシュボード
すべての製品と条件を横断した、リアルタイムステータス、今後のプル日程、および期限超過アラートを含む、すべてのアクティブ・完了・計画中の安定性試験の単一ビュー。
安定性スケジュール管理エンジン
自動プルスケジューリング、動的スケジュール変更、優先度ベースのキュー管理、および各試験のカレンダービューを備えた一元化された安定性スケジュール管理。
インタラクティブなトレンド分析
マルチバッチオーバーレイチャート、劣化曲線フィッティング、OOT/OOS検出、および予測的有効期間予測 — すべて単一の分析コンソールからアクセス可能。
完全な監査証跡
安定性試験プロトコルの作成から結果入力および報告書作成まで、すべての操作がタイムスタンプ付き、ユーザー識別済み、ALCOA+準拠の監査記録として記録されます。
スマート通知センター
今後のプル、期限超過試験、OOT結果、チャンバーエクスカーション、およびプロトコル逸脱に対する設定可能なアラートと、マルチレベルエスカレーションワークフロー。
クロスシステム統合
組織全体のすべての安定性データの単一の信頼できる情報源を構築するための、LIMS、ERP、QMS、および機器システムとの双方向統合。
手動 vs. 自動化された安定性スケジュール管理
AmpleLogicが安定性試験プロトコル管理および安定性スケジュールカレンダー運用のあらゆる側面をどのように変革するかをご覧ください。
| 領域 | 導入前(手動) | 導入後(AmpleLogic) |
|---|---|---|
| 試験スケジューリング | 手動スプレッドシートによる追跡、スケジュールの競合 | リマインダー付き自動安定性スケジュールカレンダー |
| プロトコル作成 | Wordドキュメント、サイト間でフォーマットが不統一 | 標準化された安定性試験プロトコルテンプレート(ICH Q1A) |
| プル管理 | プルの見落とし、リアルタイム可視性なし | 自動スケジューリングとアラートにより見落としゼロ |
| チャンバーモニタリング | 分断されたセンサー、エクスカーション対応の遅延 | 即時アラート付きリアルタイムモニタリング |
| トレンド分析 | 手動Excelチャート作成、集計に数週間を要する | AI搭載分析、即時有効期間予測 |
| 報告書作成 | 手動集計、エラーが発生しやすい | ワンクリックでICH/FDA規制対応報告書を生成 |
| 監査対応 | 証拠収集に追われる | 完全ALCOA+証跡により常に監査対応可能 |
ライフサイエンス分野全体で信頼される
安定性試験プロトコルおよびスケジュール管理のための規制コンプライアンス
ライフサイエンスの最前線へ
最新の製品アップデート、コンプライアンスニュース、業界インサイトをお届けします。