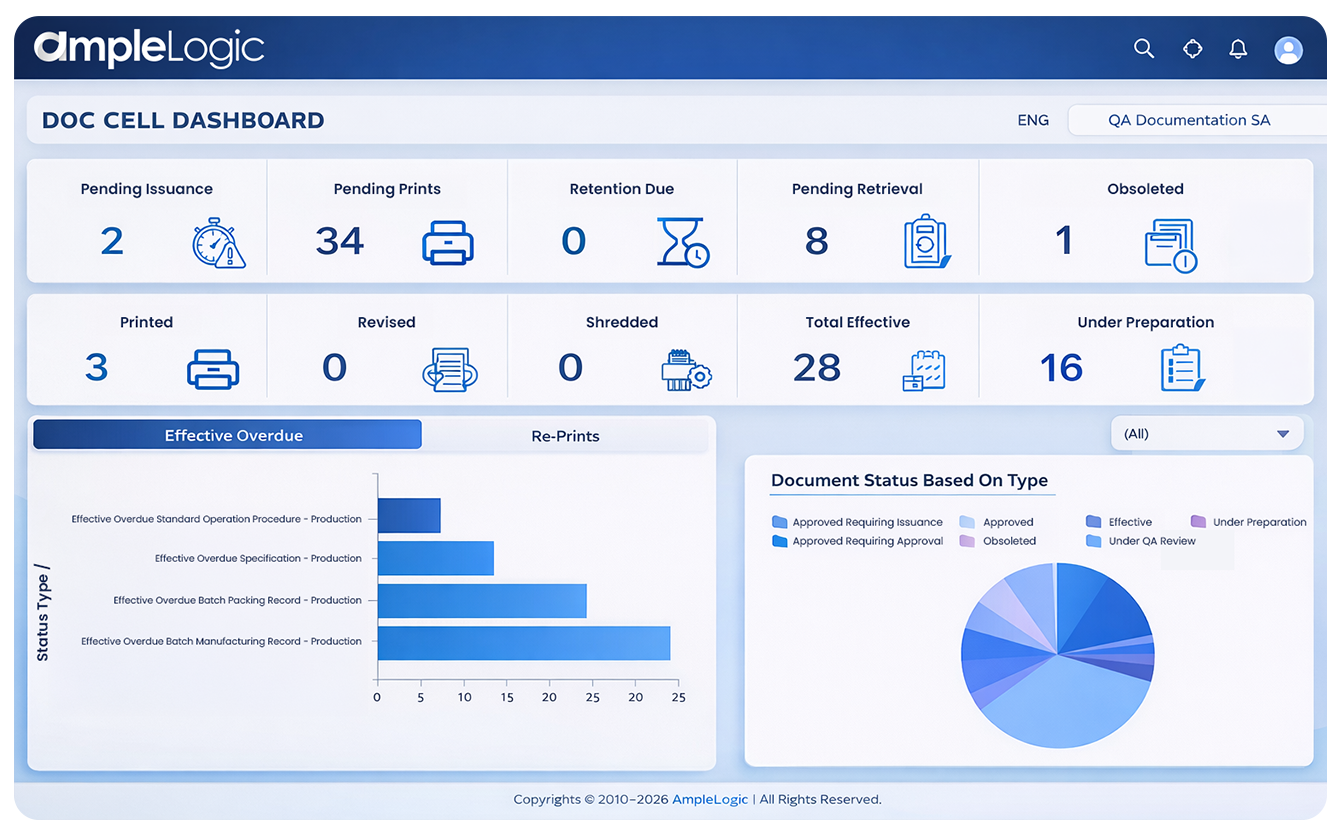
文書管理ソフトウェアなしの主な課題
医薬品文書管理におけるコンプライアンス、効率、トレーサビリティに影響を与える重大な問題点
紙または部分的にデジタル化された文書システムが継続
コンプライアンス文書管理システムがない場合、手動の文書追跡に週15〜20時間を費やし、エラーと検索時間が増加します。
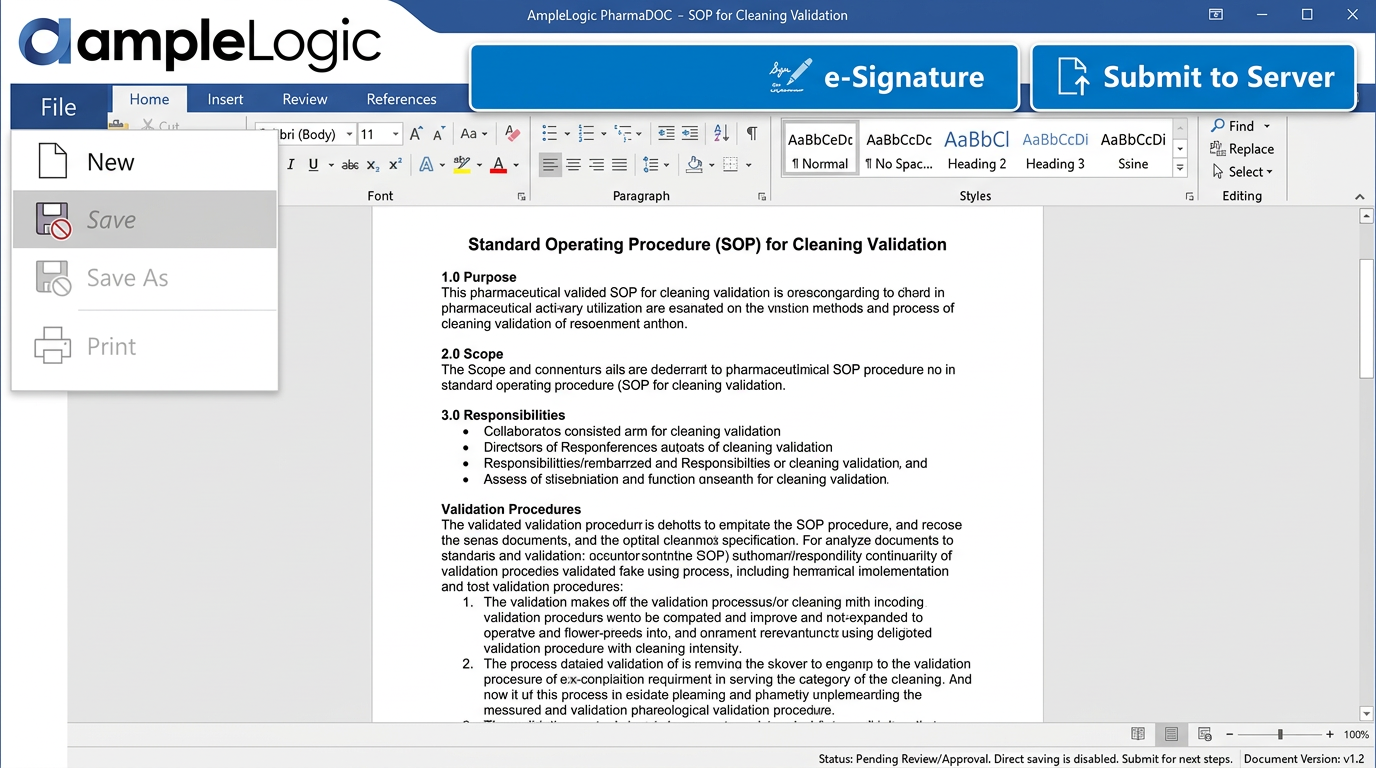
EDMS 機能の不足:バージョン管理の脆弱性と印刷管理の限界
文書バージョン管理ソフトウェアの欠如により、オペレーターが古いSOP を使用し、監査指摘事項やコンプライアンス違反につながります。
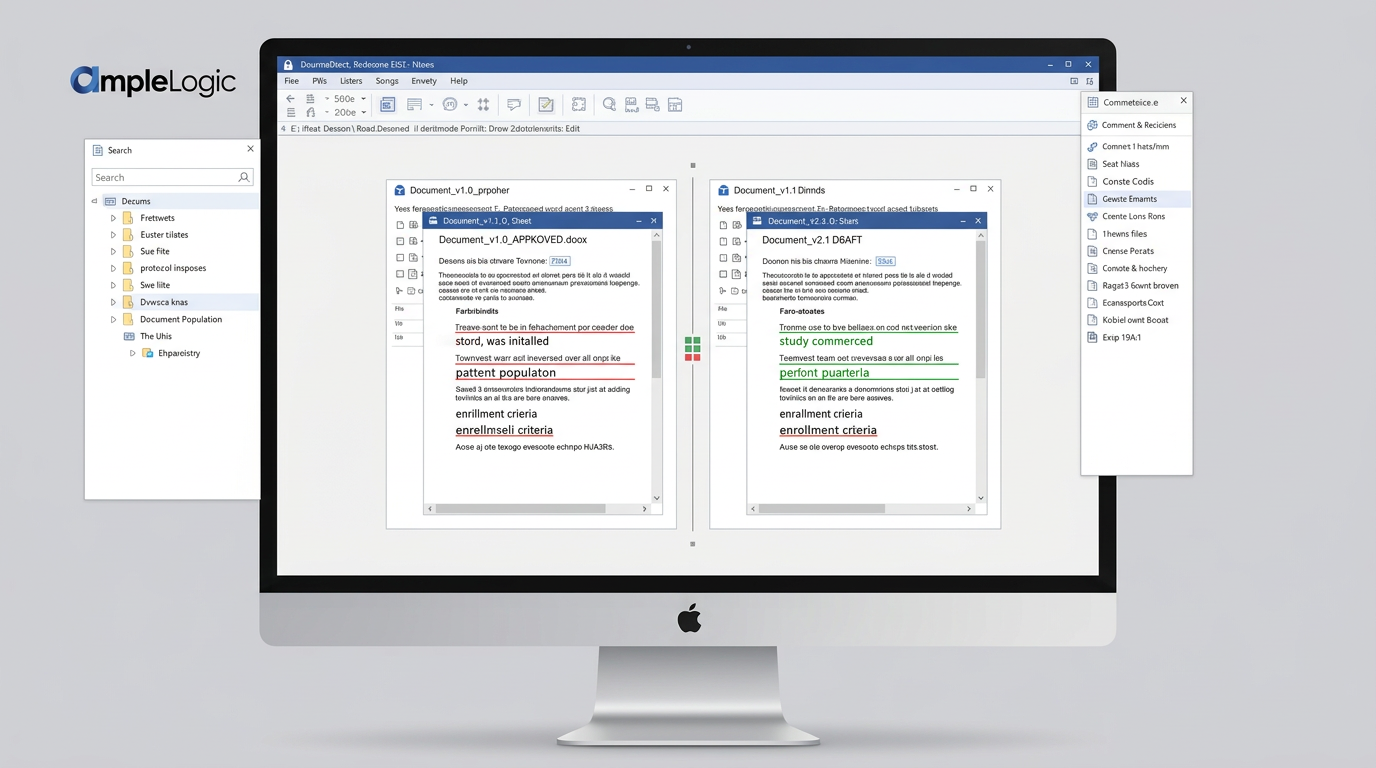
バーコード追跡なし、廃止文書管理の不備
廃止文書が管理コピー追跡や自動廃止の仕組みなしに流通し続けます。
LMS、eQMS、LIMS、MES との統合困難
切り離されたシステムはトレーサビリティを損ない、監査準備の工数と対応時間を増加させます。
製薬グレードの電子文書管理システムが提供すべきもの
文書ライフサイクル管理、規制コンプライアンス、管理されたSOP管理、および検証済み自動化
文書ライフサイクル管理
作成から審査、承認、リリース、アーカイブまで、管理された更新と廃止を含む完全な文書ライフサイクル管理ソフトウェア。
バリデーションとコントロール
規制要件にマッピングされたコントロールとデジタル文書管理システム機能を備えた検証済み文書承認ワークフローソフトウェア。
統合と自動化
シームレスなシステム統合、高度な検索、および手動調整を削減するAI 駆動の自動化。
規制コンプライアンス
FDA、EU Annex 11、および GxP 文書管理システム要件を満たし、コントロールがマッピングされた21 CFR Part 11 準拠の文書管理システム。
トレーサビリティとセキュリティ
堅牢な文書バージョン管理ソフトウェア、監査証跡、電子署名、および管理コピーの印刷・検索追跡。
医薬品文書管理ソフトウェアで管理されるコア文書タイプ
GMP 対応のための監査証跡とメタデータを備えた文書ライフサイクル管理ソフトウェア
品質文書
- バージョン管理付き標準作業手順書 (SOP)
- 承認ワークフロー付き変更管理記録
- コンプライアンストレーサビリティのためのリンクされたトレーニング記録
- 廃止コピー管理と更新管理
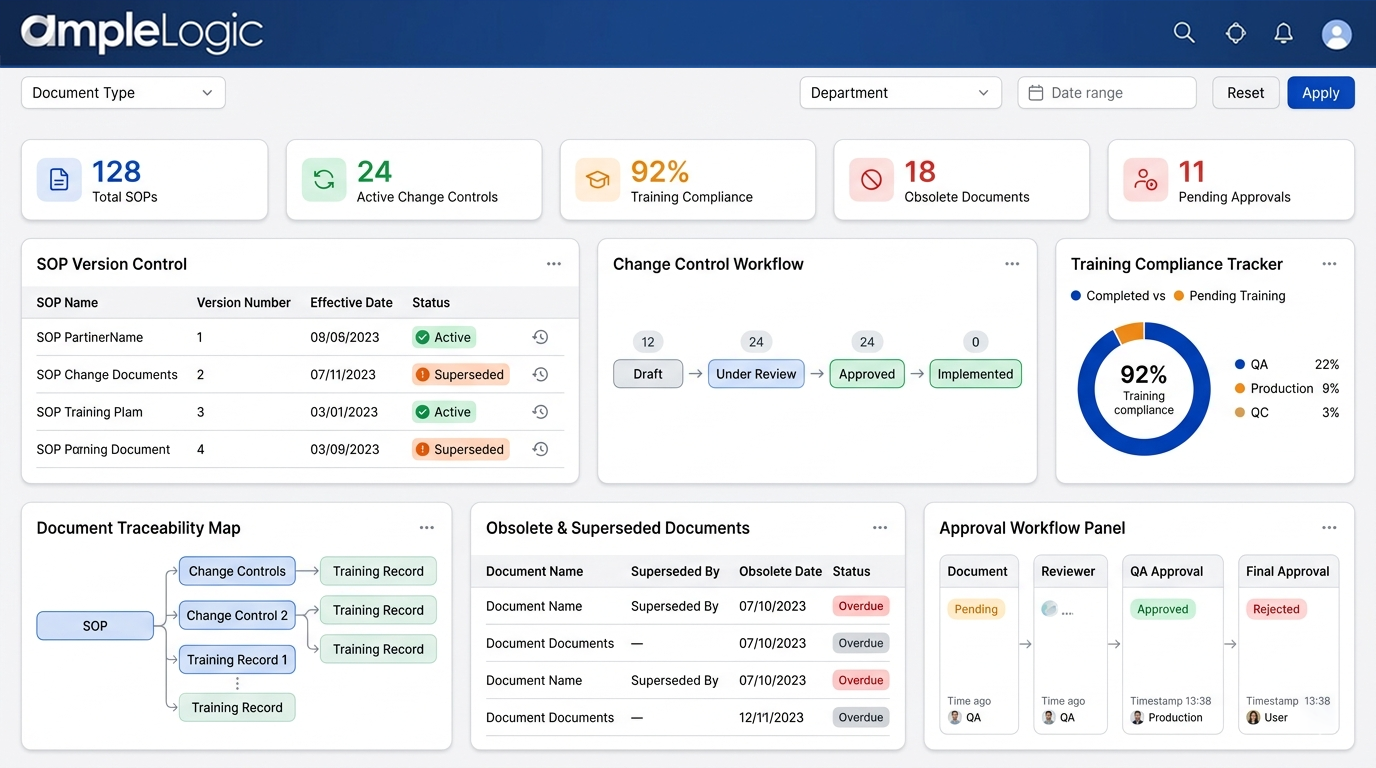
文書バージョン管理ソフトウェア:更新管理と廃止コピー管理
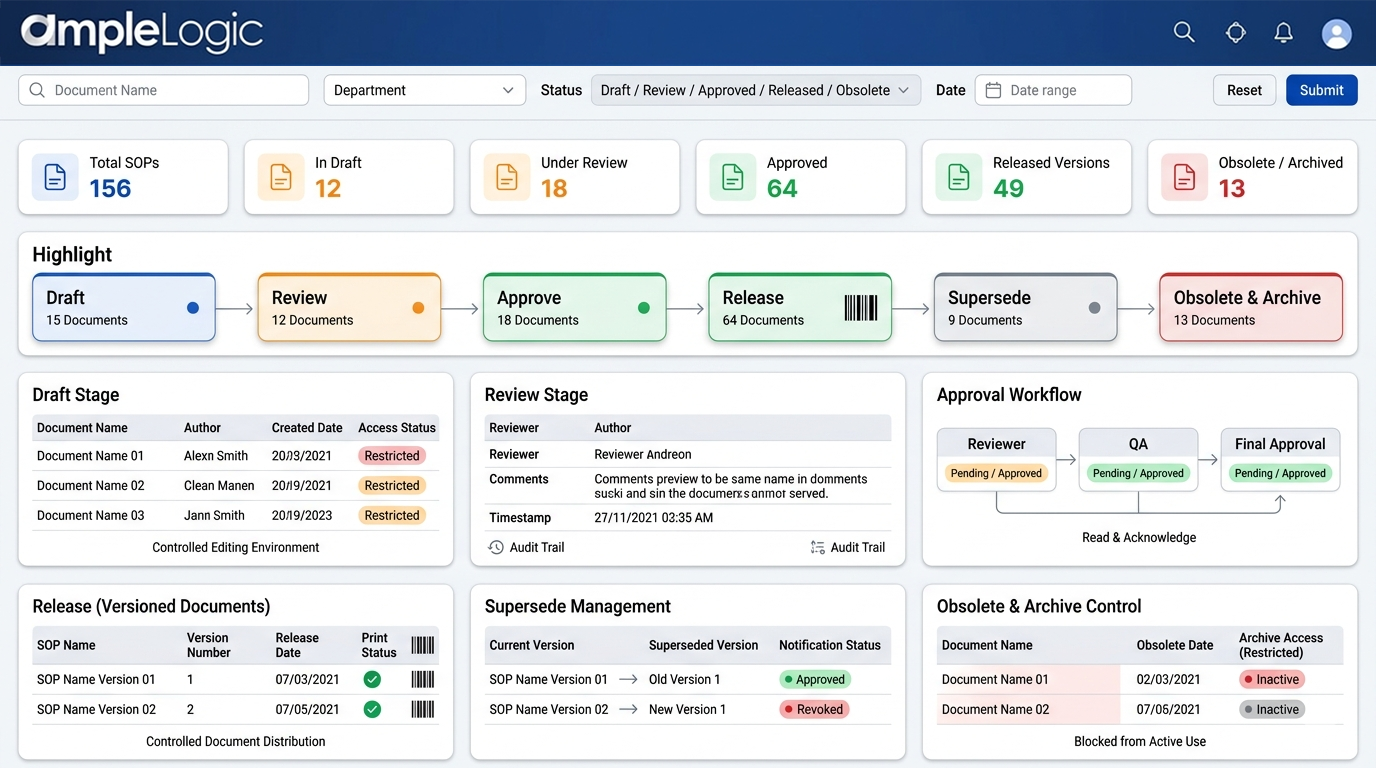
デジタル文書管理による現行文書のみでの規制プロセスの確保
下書き
明確な下書きステータスと制限されたアクセスによる管理された文書編集。
審査
日時スタンプ付きの審査者コメントの完全な監査証跡を伴う、クロスファンクショナルチームによる並行審査。
承認
読取りおよび確認ステップを強制した正式な承認ワークフロー。
リリース(バージョン管理)
バージョン番号付け、印刷管理、および印刷物へのバーコード割り当て。
更新(Supersede)
古いバージョンの自動更新とユーザーへの通知。
廃止とアーカイブ
廃止文書の明示的な無効化、管理されたアーカイブアクセス、およびアクティブプロセスでの使用ブロック。
下書き
明確な下書きステータスと制限されたアクセスによる管理された文書編集。
審査
日時スタンプ付きの審査者コメントの完全な監査証跡を伴う、クロスファンクショナルチームによる並行審査。
承認
読取りおよび確認ステップを強制した正式な承認ワークフロー。
リリース(バージョン管理)
バージョン番号付け、印刷管理、および印刷物へのバーコード割り当て。
更新(Supersede)
古いバージョンの自動更新とユーザーへの通知。
廃止とアーカイブ
廃止文書の明示的な無効化、管理されたアーカイブアクセス、およびアクティブプロセスでの使用ブロック。
印刷発行、管理コピーの印刷と回収
管理されていないコピー、トレーニングコピー、下書きコピーを含め、現行の承認済み文書のみが製造現場に届くことを確保
承認
文書承認ワークフローソフトウェアを通じてバージョンと承認メタデータを持つ文書を最終確定。
バージョンのロック
デジタル文書管理システムのセーフガードを使用して承認バージョンを凍結し、編集を防止して更新済みステータスをマーク。
印刷発行
役割/サイトによる印刷権限の付与、管理コピー・非管理コピー・トレーニングコピー・下書きコピーなどのウォーターマーク生成。サイト全体での管理コピーの印刷と回収を可能にします。
配布
バーコードラベルと引渡し時の確認署名を伴う、管理されたサイトおよび役割ベースのリストへの公開。
調整と監査証跡
完全な医薬品文書管理システムトレーサビリティのため、印刷詳細を追跡し監査で発行済み紙コピーを調整。
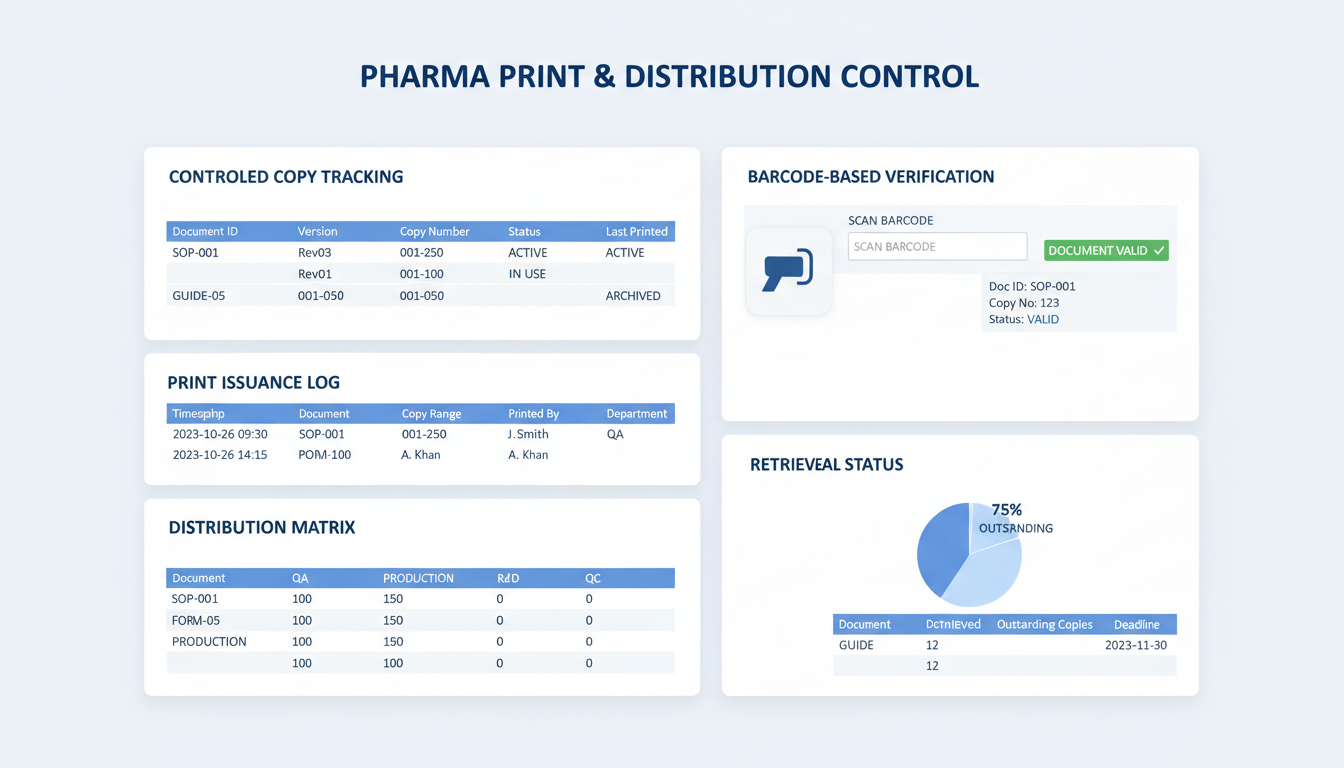
印刷管理と検証
バーコードベースの追跡によるデジタルシステムと物理的なフロアコピーのギャップを埋める
動的バーコード生成
印刷されたすべての物理的コピーに対する自動ウォーターマークと固有バーコードの生成。
使用時点での検証
製造フロアでの文書承認ステータスとバージョンを確認するリアルタイムバーコードスキャン。
包括的な印刷監査
ユーザーごとの印刷ログと場所データを含む配布済み物理コピーの完全な追跡。
コンプライアンス文書管理システムのためのインテリジェントOCR と検索
規制文書をデジタル文書管理システム全体で検索可能・審査可能・アクセス可能にする
AI 搭載OCR
スキャンや画像を検索可能な編集可能テキストに変換。
手動転記を削減し、より速い文書探索を実現します。
インテリジェント検索
文脈的な関連性を持つ規制コンテンツを表示。
文書ストア全体の検索精度を向上させます。
音声アクティベーション検索
ハンズフリーの検索とレビューを加速。
監査やチームワークフロー中のより速いアクセスを実現します。
電子開示と監査サポート
より速い文書レビュー、証拠検索、および監査対応を可能にします。
コンプライアンス、トレーサビリティ、規制監査を支援します。
チーム全体のアクセシビリティ
部門横断的に管理文書への一貫したアクセスを提供。
規制環境でのトレーサビリティとコラボレーションを実現します。
DMS ソリューションの統合
エンドツーエンドの文書トレーサビリティのためのエンタープライズGxP 文書管理システムエコシステムとシームレスに接続
LMS
新しいSOP 導入やバージョン変更からのトレーニングニーズ。トレーニング完了確認。
eQMS
変更管理、監査指摘事項、CAPAからのバージョン変更。
RIMS
規制上の指摘事項からのバージョン変更。
LIMS
試験方法とSTPの実験室結果と記録。
eLog Book
ログブックテンプレートの参照。
クリーニングバリデーション
洗浄手順のSOP へのアクセス。
eBMR/MES
BMR/BPR 文書管理とアクセス。
CAPS
校正手順のための機器マニュアル/SOP。
SAP
エンタープライズリソースプランニング統合。
UMS
ユーザー管理システム統合。
AmpleLogicプラットフォームの強みとAI 対応の価値
ライフサイエンス向けのローコード柔軟性、コンプライアンス対応、管理された自動化
LCNC ドラッグアンドドロップデザイナー
ビジュアルビルダーがカスタムコードを削減し、高速なアプリ構築のための開発を加速。
製薬向けクラウド文書管理
加速したタイムラインと迅速なビジネス効果をもたらす製薬向けクラウド文書管理ソフトウェア — 最短3ヶ月でROI を実現。
規制業界の文書管理
文書管理と監査のために設計された規制業界向け文書管理ソフトウェア。USFDA、MHRA、ISO 対応。
18以上の COTS アプリケーション
一般的なライフサイエンスワークフロー向けのプレビルドアプリ — 即時デプロイ可能。
100社以上のライフサイエンス顧客
顧客ベースは強力な業界牽引力と検証済みプラットフォーム採用を示しています。
AI 対応自動化
AI が自動化、抽出、アプリアセンブリを支援し、構築と処理を加速。
ビジネス効果、ROI と次のステップ
コンプライアンス、スピード、精度、スケーラブルなデジタル品質
25%
監査指摘事項削減
デプロイ後の指摘事項削減目標パーセント。
30%
リリースまでの時間改善
文書リリースまでの時間の予測削減率。
50%
手動作業の削減
手動処理時間の推定削減率。
ライフサイエンスの最前線へ
最新の製品アップデート、コンプライアンスニュース、業界インサイトをお届けします。