Elektronisches Qualitätsmanagementsystem (eQMS) für Life Sciences
AmpleLogic bietet eine cloudbasierte, KI-gestützte pharmazeutische QMS-Softwareplattform für unternehmensweite Compliance. Unsere digitale QMS-Plattform vereint CAPA-Management, Abweichungsmanagement, Änderungskontrolle, Audits und Lieferantenqualität in einer einzigen GxP-konformen Qualitätsereignis-Managementsoftware — vertraut von Pharma-, Biotech- und Medizinproduktunternehmen weltweit.
11+
Integrierte QMS-Module
100%
21 CFR Part 11 konform
50%
Schnellere CAPA-Abschlüsse
300+
Weltweite Implementierungen
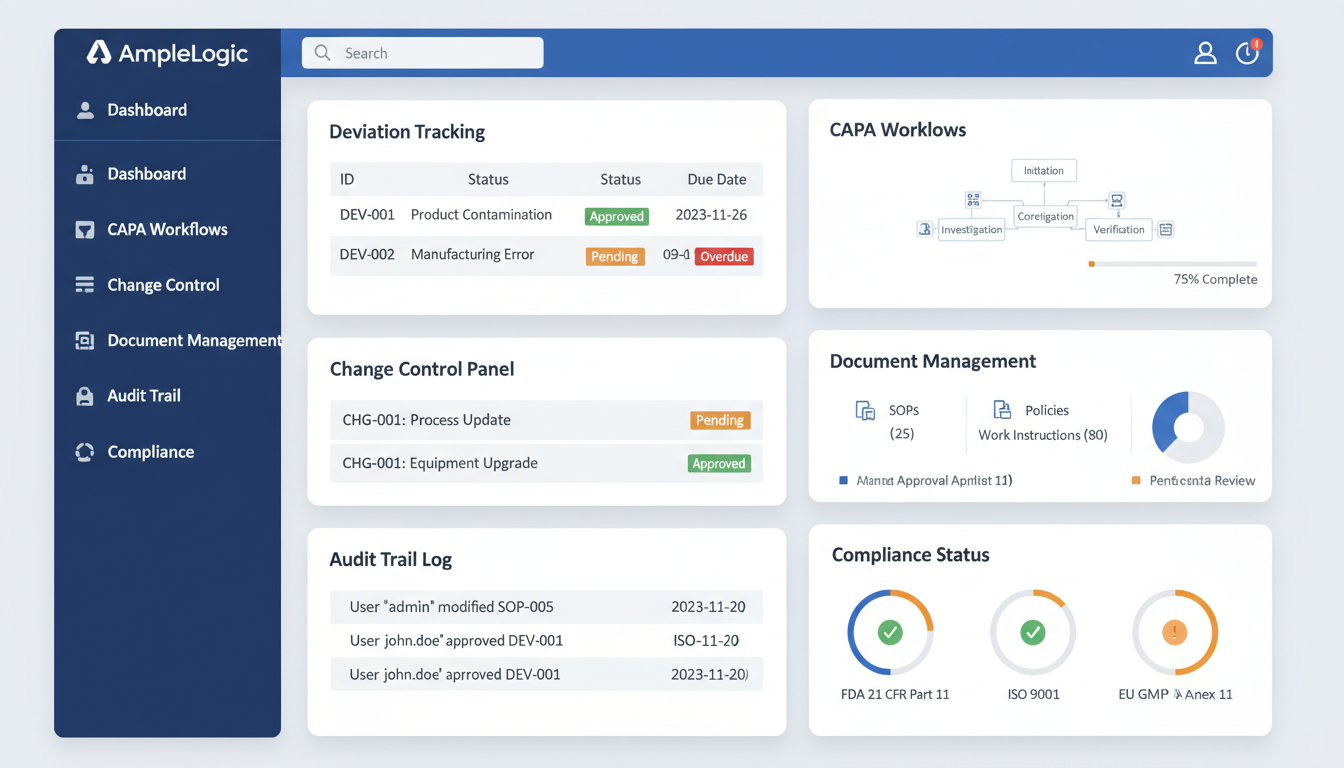
Warum veraltete Qualitätsmanagementsystem-Software unzureichend ist
Wie fragmentierte manuelle Prozesse in pharmazeutischer Compliance-Managementsoftware und veralteten GMP-Qualitätsmanagementsystemen zu Verzögerungen bei Qualitätsereignissen, Lücken im Nichtkonformitätsmanagement und höheren Qualitätskosten führen
Regulatorische Nichtkonformität
Hohes Risiko von Sanktionen durch manuelle Dokumentationsfehler, fehlende Audit-Trails und eingeschränkte Rückverfolgbarkeit — Probleme, die eine GxP-konforme Qualitätsmanagementsystemsoftware beseitigt
Isolierte Qualitätssysteme
Eigenständige QMS-Module mit schwachen Integrationen führen zu verzögerten Untersuchungen, doppelter Dateneingabe und verlängerten CAPA-Abschlüssen im unternehmensweiten Qualitätsmanagementsystem
Keine Echtzeit-Analytik
Fehlende Dashboards für Abweichungsmanagement, CAPA, Änderungskontrolle und OOS schränken proaktive Entscheidungsfindung und Risikotransparenz ohne eine digitale Qualitätsmanagementplattform ein
Langsame Untersuchungszyklen
Papierbasierte oder e-Mail-gesteuerte Untersuchungen dauern 2–4 Mal länger als digitale Workflows in moderner pharmazeutischer Qualitätsmanagementsoftware, was die Chargenfreigabe verzögert
Eingeschränkte externe Zusammenarbeit
Kein Echtzeit-Partnerzugang für Lieferantenqualitätsmanagement, CDMO-Untersuchungen oder Koordination von Vertragslaboren — eine Lücke, die cloudbasierte QMS-Software schließt
Globale Abstimmungslücken
Multisite-Betrieb kämpft mit inkonsistenten Prozessen, fragmentierten Daten und der Unfähigkeit, Qualitätskennzahlen ohne ein unternehmensweites Qualitätsmanagementsystem zu konsolidieren

Die Kosten manueller Prozesse
Unternehmensweites Qualitätsmanagementsystem — Vorteile
Cloudbasierte SaaS-QMS-Plattform mit Lebenszyklusmanagemement, regulatorischer Compliance, Qualitäts-Workflow-Automatisierung und validierter Unternehmensqualitätsplattform für Pharma und Biotech
Geschlossener Kreislauf-Wirksamkeitsnachweis
Integrierte Verifizierung für CAPA-Management, Änderungskontrolle, Abweichungen und Auditmanagement-Software-Workflows
Echte durchgängige Rückverfolgbarkeit
Ein-Klick-Verknüpfung über Abweichungsmanagement, CAPA, Änderungen, Beschwerden, OOS/OOT und Auditdatensätze in einem einheitlichen QMS
Jederzeit auditbereit
Automatisierte Beweissammlung, unveränderliche Audit-Trails und Inspektionsdashboards für FDA-21-CFR-Part-11-konformen QMS-Betrieb
Risikobasierte Entscheidungsunterstützung
Priorisierung von Maßnahmen mittels Risikobewertung und historischen Qualitätsdaten innerhalb des unternehmensweiten Qualitätsmanagementsystems
KI-gestützte Qualitätsintelligenz
Schnellere Ursachenanalyse, Anomalieerkennung und Wirksamkeitsverifizierung mit KI-gestützten Qualitätsmanagementsystem-Fähigkeiten
Automatisierte Eskalation & Erinnerungen
Risiko- und zeitplangesteuerte Erinnerungen mit automatischer Eskalation in der pharmazeutischen Compliance-Managementsoftware
Warum AmpleLogic — Cloud-QMS-Software für Life Sciences
Branchenführende pharmazeutische Qualitätsmanagementsoftware mit nachgewiesenem ROI und regulatorischer Verteidigungsfähigkeit
Die Kosten manueller Qualität
Manuelle Qualitätsprozesse erhöhen Fehler, Verzögerungen und Betriebskosten — Cloud-QMS-Software beseitigt diese Ineffizienzen
Intelligente Empfehlungsmaschine
Intelligente, datengestützte Empfehlungen zur Beschleunigung der Problemlösung auf Ihrer digitalen Qualitätsmanagementplattform
Cloud-basierter aPaaS-Vorteil
Low-Code-cloudbasierte QMS-Software beschleunigt Deployment, Anpassung und Multisite-Rollout für das pharmazeutische Qualitätsmanagement
GxP-Compliance und Validierung
GxP-konformes Qualitätsmanagementsystem mit integrierten FDA-21-CFR-Part-11-Kontrollen stellt sicher, dass Prozesse regulatorische Standards erfüllen und Audits bestehen
Quantifizierbare ROI-Kennzahlen
Misst Effizienzgewinne und Kosteneinsparungen durch den Einsatz unternehmensweiter Qualitätsmanagementsystemsoftware im Betrieb
Nahtlose Integrationen
Verbindet sich mühelos mit LIMS, eBMR, DMS, ERP und vorhandener Qualitätsmanagementsystemsoftware in Ihrem Technologie-Stack
CAPA-, Abweichungs-, Audit- und Lieferantenqualitätsmanagement
Erkunden Sie jedes Modul unserer Qualitätsmanagementsystemsoftware — CAPA-Managementsoftware, Abweichungsmanagementsoftware, Änderungskontroll-Managementsoftware, Auditmanagement-Software, Beschwerdemanagementsoftware, Qualitätsrisikomanagementsoftware, Lieferantenqualität und Nichtkonformitätsmanagement
Abweichungsmanagement
Pharmazeutisches Qualitätsereignis-Managementsystem
Umfassende Abweichungsmanagementsoftware für pharmazeutische Unternehmen, die ein durchgängiges Abweichungslebenszyklus-Management pharmazeutischer Produktionsabweichungen und Nichtkonformitäten liefert — von der Erkennung bis zum Abschluss. Dieses cloudbasierte Abweichungsmanagementsystem bietet ein Abweichungsverfolgungssystem für die Pharmaproduktion mit vollständiger Rückverfolgbarkeit, risikobasierter Abweichungsklassifizierung und GMP-Abweichungsmanagement-Verteidigungsfähigkeit.
CAPA-Management
Pharmazeutische CAPA-Managementsoftware
Unternehmensweite Korrektur- und Vorbeugungsmaßnahmen-Software speziell für Pharma und Life Sciences. Dieses elektronische CAPA-Managementsystem liefert eine geschlossene CAPA-Lebenszyklus-Automatisierung — von der Einleitung über die Ursachenuntersuchung, CAPA-Workflow-Automatisierung und Wirksamkeitsverfolgung — und stellt sicher, dass jedes Qualitätsereignis gelöst, dokumentiert und auditbereit gemäß FDA-, GxP- und 21-CFR-Part-11-Anforderungen ist.
Änderungskontrolle
Planen, Bewerten, Umsetzen, Verifizieren
Verwalten Sie geplante und ungeplante Änderungen an Prozessen, Ausrüstung, Materialien und Systemen mit strukturierter Auswirkungsanalyse, Genehmigung durch mehrere Stakeholder und Überprüfung nach der Implementierung.
Auditmanagement
Auditmanagement-Software für pharmazeutische Qualitätssysteme
Umfassende Auditmanagement-Software für pharmazeutische Unternehmen, die internes und externes Auditmanagement, Lieferanten- und Anbieter-Auditmanagement sowie regulatorische Inspektionsbereitschaft abdeckt. Dieses GMP-konforme Auditmanagementsystem verfügt über automatisierte Auditplanung und -terminierung, Jahresauditplaner und Jahresauditkalender, Auditbefund- und CAPA-Integration, Drittparteien-Auditmanagement sowie Audit-Analytik und -Berichterstattung — alles innerhalb einer Cloud-Auditmanagement-Software für Pharma.
Beschwerdemanagement
KI-gestütztes Beschwerdemanagement für pharmazeutische Qualitätssysteme
Speziell entwickelte Beschwerdemanagementsoftware für pharmazeutische Unternehmen — ein GMP-konformes Beschwerdemanagementsystem, das den gesamten Beschwerdeuntersuchungsworkflow von der Multikanal-Eingabe über die Ursachenanalyse, regulatorische Berichterstattung und Beschwerde-Lösungsverfolgung mit vollständiger Rückverfolgbarkeit zu verwandten Qualitätsereignissen automatisiert.
OOS-Management
OOS-Managementsoftware für Außerhalb-der-Spezifikation-Untersuchungen
Speziell entwickelte OOS-Managementsoftware mit strukturierten Phase-I- und Phase-II-Außerhalb-der-Spezifikation-Untersuchungsworkflows, abgestimmt auf die FDA-Leitlinien — eine GMP-OOS-Untersuchungssoftware, die sicherstellt, dass Laborergebnisse mit wissenschaftlicher Strenge als regulatorisch konformes OOS-System mit vollständiger Verteidigungsfähigkeit untersucht werden.
OOT-Management
Außerhalb-des-Trends-Analyse
Statistische Trendüberwachung und alarmgesteuerte Untersuchungsworkflows zur Erkennung allmählicher Qualitätsschwankungen, bevor sie zu OOS-Ereignissen werden, und Ermöglichung eines proaktiven Qualitätsmanagements.
Laborzwischenfallmanagement
Laborzwischenfallmanagement-Software für pharmazeutische QC-Labore
Speziell entwickelte Laborzwischenfallmanagement-Software und Laborvorfallsmanagementsystem für pharmazeutisches Laborzwischenfallmanagement — verfolgen und untersuchen Sie Gerätestörungen, Probenkontaminationen, Umgebungsabweichungen und Analytikerfehlern mit dieser QC-Laborzwischenfallmanagement-Software mit strukturierten Korrekturmaßnahmen-Workflows und GxP-konformen Laborzwischenfallberichtssystem-Fähigkeiten.
Qualitätsrisikomanagement
Pharmazeutische Risikomanagementsoftware — KI-gesteuertes Qualitätsrisikomanagementsystem
Speziell entwickelte QRM-Software für Pharmazeutika und unternehmensweite Risikomanagementsoftware, die ein integriertes Qualitätsrisikomanagementsystem für Pharma liefert — eine pharmazeutische Risikomanagementsoftware und Qualitätsrisikobewertungssoftware-Plattform mit KI-gesteuerter Risikomanagementsoftware-Fähigkeiten, Risikobewertung und -priorisierung für Arzneimittelprodukte, FMEA-Risikoanalysesoftware, Fischgräten-Diagramm-Analysesoftware, Ursachenanalyse-Tools und cloudbasierter Risikomanagementsoftware für Pharma, abgestimmt auf ICH Q9.
Lieferanten-/Anbieterqualifikation
Lieferantenqualitätsmanagement & Anbieterqualifikationssoftware
Speziell entwickelte Anbieterqualifikationssoftware und Lieferantenqualifikations-Managementsystem für durchgängiges Anbieterlebenszyklus-Management — eine Lieferantenqualitätsmanagement-Software und Anbieterqualifikationssystem für Pharmazeutika, das Lieferantenrisikobewertungssystem-Fähigkeiten von der Erstqualifikation über die Lieferantenqualitätsüberwachungssoftware, das Lieferantenleistungsmanagement bis zur periodischen Neuqualifikation liefert.
Produktrückrufmanagement
Einleiten, Durchführen, Berichten, Abschließen
Schnelle Rückrufeinleitung und -durchführung mit chargengenauer Rückverfolgbarkeit, Management regulatorischer Benachrichtigungen, Kundenkommunikationsverfolgung und Wirksamkeitsbewertung nach dem Rückruf.
CAPA-Lebenszyklus: Wirksamkeitsprüfungen
Lebenszyklusmanagement, Beweiserfassung und Automatisierung für regulatorische Verteidigungsfähigkeit
Erkennung
Probleme aus Abweichungen, Beschwerden, Audits, OOS/OOT identifizieren. Automatische Ereignisklassifizierung und Verknüpfung von Quelldatensätzen.
Untersuchung
Ursachenanalyse mit Zeitplänen, Datennachverfolgung und Risikobewertung. Historische Muster leiten Untersuchungen.
Maßnahmenplan
System empfiehlt relevante Maßnahmen, Risikopriorität und bewährte Best Practices.
Implementierung
Maßnahmen ausführen, Beweise anhängen, verknüpfte Abweichungen, Änderungen und Beschwerdeunterlagen aktualisieren.
KI-Wirksamkeitsintelligenz
KI vergleicht jede neue CAPA mit offenen Wirksamkeitsprüfungs-CAPAs ähnlicher Art — kennzeichnet Überschneidungen, empfiehlt Konsolidierung und verhindert redundante Untersuchungen.
Abschluss
Beweise bestätigen, Verknüpfungen zu Audit-/Beschwerdeunterlagen finalisieren und für regulatorische Überprüfung archivieren.
Erkennung
Probleme aus Abweichungen, Beschwerden, Audits, OOS/OOT identifizieren. Automatische Ereignisklassifizierung und Verknüpfung von Quelldatensätzen.
Untersuchung
Ursachenanalyse mit Zeitplänen, Datennachverfolgung und Risikobewertung. Historische Muster leiten Untersuchungen.
Maßnahmenplan
System empfiehlt relevante Maßnahmen, Risikopriorität und bewährte Best Practices.
Implementierung
Maßnahmen ausführen, Beweise anhängen, verknüpfte Abweichungen, Änderungen und Beschwerdeunterlagen aktualisieren.
KI-Wirksamkeitsintelligenz
KI vergleicht jede neue CAPA mit offenen Wirksamkeitsprüfungs-CAPAs ähnlicher Art — kennzeichnet Überschneidungen, empfiehlt Konsolidierung und verhindert redundante Untersuchungen.
Abschluss
Beweise bestätigen, Verknüpfungen zu Audit-/Beschwerdeunterlagen finalisieren und für regulatorische Überprüfung archivieren.
Manuelle vs. digitale Qualitätsmanagementsystem-Software
Quantifizierter ROI durch den Einsatz cloudbasierter pharmazeutischer Qualitätsmanagementsoftware von AmpleLogic über den gesamten Qualitätslebenszyklus
Abweichungsuntersuchungszyklus
35–50 % schneller45–90 Tage durchschnittliche Zykluszeit mit papierbasierter Untersuchung, e-Mail-gesteuerter Koordination und manueller Beweissammlung abteilungsübergreifend
Automatisierte Workflows mit KI-gestützter Ursachenanalyse, automatisch verknüpften Qualitätsdatensätzen und konfigurierbarer SLA-Verfolgung reduzieren die Zykluszeit auf 15–30 Tage
CAPA-Abschluss & Wirksamkeitsverifizierung
40–60 % schneller60–120 Tage CAPA-Zyklen mit manueller Verfolgung, verpassten Wirksamkeitsprüfungen, isolierten Maßnahmenplänen und ohne systematische Beweissammlung
Geschlossener Lebenszyklus mit automatisierten Wirksamkeitsprüfungen, Meilenstreinverfolgung, Nachweisanforderungen und KI-empfohlenen Korrekturmaßnahmen
Auditvorbereitung & Inspektionsbereitschaft
80 % Aufwandseinsparung2–4 Wochen manuelle Beweissammlung, systemübergreifende Querverweise und kurzfristige Dokumentenzusammenstellung vor jedem Audit
Auf Anfrage generierte inspektionsbereite Beweispakete — Ein-Klick-Audit-Trail-Zusammenstellung, Echtzeit-Compliance-Dashboards und Lückenanalyse
Änderungskontrolllebenszyklus
60 % ZyklusreduktionMehrwöchige abteilungsübergreifende Auswirkungsbewertungen mit manueller Genehmigungsweiterleitung, getrennter Implementierungsverfolgung und verzögerten SOP-Updates
KI-gestützte Änderungsauswirkungsvorhersage, automatisierte Multi-Stakeholder-Weiterleitung, meilensteinbasierte Implementierungsverfolgung und automatisch ausgelöste SOP-/Schulungsupdates
KI-gestütztes Qualitätsmanagementsystem
Nutzung von KI-Agenten und maschinellem Lernen zur Automatisierung von Untersuchungen, Risikovorhersage und Beschleunigung von Qualitätsentscheidungen auf Ihrer digitalen Qualitätsmanagementplattform
CAPA-Wirksamkeitsintelligenz
KI überwacht kontinuierlich offene Wirksamkeitsprüfungs-CAPAs und vergleicht automatisch jede neue CAPA ähnlicher Art — kennzeichnet potenzielle Duplikate, empfiehlt Konsolidierung oder Querverweise und macht bestehende Korrekturmaßnahmen sichtbar, um redundante Untersuchungen zu verhindern
Qualitätsereignis-Zusammenfassungsagenten
Aggregieren automatisch Daten über Untersuchungen, Abweichungen und CAPA-Pläne hinweg, um narrative Zusammenfassungen zu erstellen — Reduzierung der Dokumentationszeit um 60 %
KI-gestützte Ursachenanalyse
Mustererkennung anhand historischer CAPA- und Abweichungsdaten zur Vorhersage wahrscheinlicher Ursachen, Empfehlung bewährter Vorbeugungsmaßnahmen und Erklärung wesentlicher Treiber
Prädiktive Qualitätsanalytik
Modelle des maschinellen Lernens erkennen aufkommende Qualitätssignale, prognostizieren Abweichungstrends und priorisieren Hochrisikobereiche, bevor sie zu Compliance-Problemen werden
Intelligente Änderungsauswirkungsvorhersage
Analyse historischer Änderungsdaten und Abweichungsmuster zur Vorhersage von Änderungsauswirkungen auf Produkte, Prozesse und regulatorische Einreichungen vor der Implementierung
Automatisierte Workflow-Optimierung
KI lernt kontinuierlich aus Prozessausführungsdaten, um Workflow-Verbesserungen vorzuschlagen, Engpässe zu identifizieren und SLA-optimierte Weiterleitungspfade zu empfehlen
eQMS-Plattformfunktionen
Unternehmensweite Qualitätsmanagementsystemsoftware-Fähigkeiten — CAPA-Management, Abweichungsmanagement, Auditmanagement, Nichtkonformitätsmanagementsoftware und Lieferantenqualität mit integrierter Qualitäts-Workflow-Automatisierung für Life-Sciences-Compliance
Geschlossene Wirksamkeitsverifizierung
Integrierte Verifizierungsworkflows für CAPA, Änderungskontrolle, Abweichungen und Audits — mit vordefinierten Erfolgskriterien, Nachtestprotokollen und automatisierter Beweissammlung für regulatorische Verteidigungsfähigkeit.
Risikobasierte Entscheidungsunterstützung
Multisite-Qualitätsharmonisierung
Echtzeit-Qualitätsdashboards
Elektronische Unterschrift & Audit-Trail
Konfigurierbarer Low-Code-Workflow-Engine
KI-gestützte Untersuchungsunterstützung
Jährliche Produktqualitätsüberprüfung (APQR)
Mobile Qualitätsdurchführung
Automatisierter Eskalationsmodul
Externe Echtzeitzusammenarbeit
Interne Teams, CDMOs, Lieferanten und Partner in ein einziges Qualitätsökosystem für schnellere Lösung und globale Abstimmung einbinden
Lieferanten- & CDMO-Zugang
Kontrollierten Zugang für externe Partner für Echtzeitzusammenarbeit bei Untersuchungen, Auditbefunden und Lieferanten-Korrekturmaßnahmen gewähren
Vertragslaborkoordination
OOS/OOT-Daten teilen, Untersuchungen koordinieren und Methodentransfers mit Vertragstestlaboren in einem einheitlichen System verwalten
Bereitschaft für regulatorische Behörden
Inspektionsbereite Beweispakete mit einem Klick generieren — vollständige Audit-Trails, verknüpfte Qualitätsdatensätze und Compliance-Dashboards
Multisite-Qualitätsausrichtung
Qualitätsprozesse über globale Produktionsstandorte mit zentralisierter Konfiguration, lokalisierten Workflows und konsolidierter Berichterstattung standardisieren
Einheitlicher eQMS-Integrations-Hub
Cloudbasierte QMS-Software nahtlos mit Ihrem gesamten Unternehmensökosystem verbunden für durchgängige Qualitätsrückverfolgbarkeit
Dokumentenmanagement (DMS)
SOP-Revisionen, kontrollierte Kopienverteilung, Versionsverwaltung
Lernmanagementsystem (LMS)
Automatisch ausgelöste Schulungen bei Änderungskontrollgenehmigungen und SOP-Updates
LIMS
Laborvorfälle, Abweichungen, OOS/OOT-Autoeinleitung und Datenabruf
eBMR / MES
Chargenhalte-Auslöser, Produktionsabweichungserfassung, Echtzeit-Prozessdaten
Regulatorisch (RIMS)
Änderungskontrollkoordination, Auswirkung auf Produktregistrierung, regulatorische Einreichungen
Reinigungsvalidierung
Abweichungen, OOS/OOT aus Reinigungsprozessüberwachung und Grenzwerttestung
eLogbook
Abweichungserfassung aus Logbuchereignissen, Umgebungsabweichungen
Sicherheit / Pharmakovigilanz
Beschwerde-zu-Sicherheitsfall-Verknüpfung, Korrelation unerwünschter Ereignisse
ERP / Lieferkette
Lieferantendatensynchronisation, Chargenabstammung, Materialrückverfolgbarkeit, Haltemanagement

AmpleLogic eQMS Hub
Vernetztes Unternehmensökosystem
GxP-konformes Qualitätsmanagementsystem
FDA-21-CFR-Part-11-konformes QMS, ISO-13485-Qualitätsmanagementsystem und GMP-Qualitätsmanagementsoftware mit integrierter Auditbereitschaftssoftware, Inspektionsbereitschaftsplattform und pharmazeutischem Compliance-Management für regulierte Branche Qualitätsmanagement
21 CFR Part 11
Elektronische Aufzeichnungen und Unterschriften
EU Annex 11
Validierung computergestützter Systeme
ICH Q9
Qualitätsrisikomanagement
ICH Q10
Pharmazeutisches Qualitätssystem
GAMP 5 / ISPE
Risikobasierte Validierung
ISO 9001 / 13485
Qualitäts- und Medizinprodukte-Standards
EU MDR / IVDR
Medizinprodukteverordnung
ALCOA+-Grundsätze
Datenintegritätsrahmen
Qualitätsmanagementsoftware für jeden Life-Sciences-Sektor
Branchenspezifische eQMS-Lösungen — pharmazeutisches Qualitätsmanagementsystem, Biotech-QMS-Software und Medizinprodukte-QMS-Software für jeden regulierten Hersteller
Pharmazeutika
Durchgängige GMP-Qualitätsmanagementsoftware für Arzneimittelherstellung, API-Produktion und Formulierungsanlagen — speziell entwickelte Qualitätsmanagementsoftware für Pharma.
Biotechnologie
Spezialisierte Qualitätsmanagementsoftware für Biotech — unterstützt Biologic-, Biosimilar- und Therapiepräparat-Entwicklung und -Herstellung.
Medizinprodukte
Medizinprodukte-Qualitätsmanagementsoftware — ISO-13485-, EU-MDR/IVDR-konform für Produktdesign, -herstellung und Post-Market-Surveillance.
Gen- & Zelltherapie
Life-Sciences-Qualitätsmanagementsystem für ATMP- und Zell-/Gentherapie-Herstellung mit spezialisierter regulatorischer Ausrichtung.
CDMO / CMO
Unternehmensweites Qualitätsmanagementsystem für Lohnhersteller mit Mehrkundenqualitätsmanagement und Auditbereitschaft.
Nahrungsergänzungsmittel
Pharmazeutische Qualitätsmanagementsoftware für die Herstellung von Nahrungsergänzungsmitteln und Nutraceuticals mit GMP-Compliance.
AmpleLogic eQMS — Pharmazeutische Qualitätsmanagementsoftware
Pharmazeutisches Compliance-Management, Untersuchungen, Verifizierung und Auditbereitschaft über den gesamten Qualitätslebenszyklus mit unternehmensweiten QMS-Lösungen und Life-Sciences-Compliance-Software beschleunigen
GxP-konformes Qualitätsmanagementsystem mit FDA-, ICH-Q10-, ISO-, EU-MDR/IVDR- und WHO-GMP-Abdeckung
40–50 % schnellere Untersuchungen und CAPA-Abschlüsse mit KI-gestützten Qualitätsmanagementsystem-Fähigkeiten
Nachweisbare geschlossene Kreislauf-Wirksamkeitsverifizierung in jeder Phase des QMS-Lebenszyklus
Auditbereite Beweissammlung innerhalb von Sekunden — nicht Tagen — für pharmazeutisches Compliance-Management
Pilot-First-Rollout mit risikobasierter Validierung (GAMP-5-ausgerichtet) auf cloudbasierter QMS-Software
Externe Echtzeitzusammenarbeit mit CDMOs, Lieferanten und Partnern durch Lieferantenqualitätsmanagement-Software
Multisite-, mehrsprachige globale Qualitätsausrichtung vom ersten Tag an mit unternehmensweitem Qualitätsmanagementsystem
Einheitliche Qualitätsdaten für Jährliche Produktqualitätsüberprüfungen (APQR) in einer einzigen digitalen Qualitätsmanagementplattform
eQMS-Software-Anerkennung & Kundenzufriedenheitsauszeichnungen
Vertraut von führenden Life-Sciences-Organisationen weltweit
Nr. 1 Einfachste Bedienung
Medizinisches QMS
Höchste Kundenzufriedenheit
Branchenführender CSAT
Plattformstärken
Drag-and-Drop-Anpassung
89 G2-Auszeichnungen
Multi-Kategorie-Leader
"Das Amplelogic-QMS-System verfügt über alle erforderlichen qualitätsbezogenen Module, und alle Abweichungen, Änderungskontrollen und CAPAs werden effektiv gepflegt und verfolgt. Alle Module sind äußerst einfach zu bedienen."
Kandikattu K.
Qualitätsfachmann
"Die Integration mit unseren anderen Tools funktioniert reibungslos. Die meisten unserer individuellen Anpassungswünsche wurden berücksichtigt, was die Nutzung für uns sehr benutzerfreundlich macht."
Quality Assurance Manager
Mittelständische Pharmaindustrie
"Das System entspricht den Anforderungen von 21 CFR Part 11 und EU Annex 11. Die Unterstützung des Teams während der anfänglichen Einrichtung war sehr hilfreich und ermöglichte einen reibungslosen Übergang."
Krishna C.
Compliance-Leiter
Bereit, Ihr Qualitätsmanagementsystem zu transformieren?
Schließen Sie sich führenden Pharma-, Biotech- und Medizinprodukte-Unternehmen an, die Compliance mit dem besten elektronischen Qualitätsmanagementsystem (eQMS) beschleunigen — einer cloudbasierten digitalen QMS-Plattform und SaaS-QMS-Plattform für das moderne Unternehmen.
In der Life Sciences vorne bleiben
Erhalten Sie die neuesten Produktupdates, Compliance-Nachrichten und Brancheneinblicke direkt in Ihr Postfach.