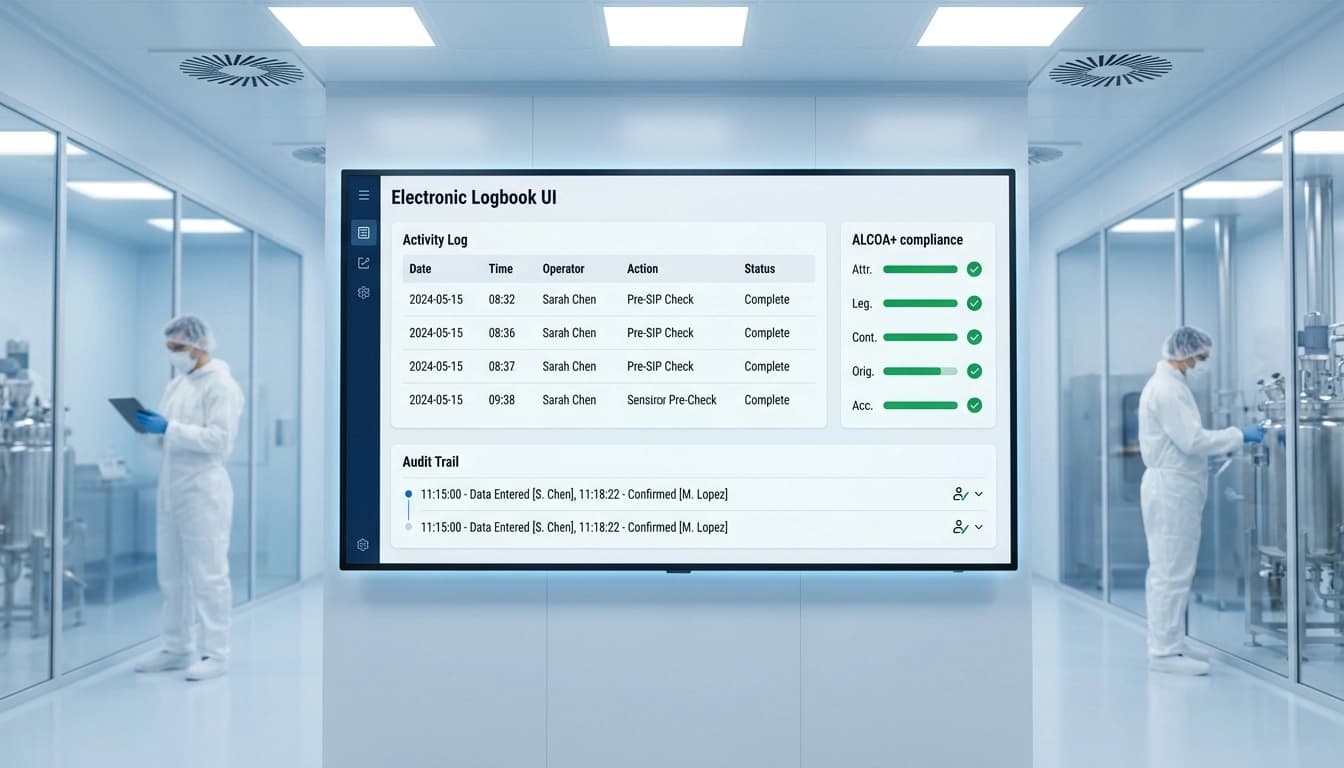
En la industria farmacéutica, mantener la integridad de los datos es crucial para garantizar la calidad del producto, la seguridad del paciente y el cumplimiento normativo. La integridad de los datos se refiere a la precisión y coherencia de los datos a lo largo de su ciclo de vida. Los libros de registro electrónicos se han convertido en herramientas esenciales para mantener el cumplimiento de ALCOA+.
Los libros de registro electrónicos reemplazan los libros de registro en papel utilizados en todas las operaciones farmacéuticas, desde registros de uso de equipos y registros de limpieza hasta monitoreo ambiental y registros de acceso al área. El formato digital garantiza que las entradas tengan automáticamente una marca de tiempo, se atribuyan a usuarios específicos y se protejan contra modificaciones no autorizadas.
Las características clave de integridad de datos incluyen firmas electrónicas con verificación biométrica, pistas de auditoría automáticas, controles de acceso de usuarios simultáneos, almacenamiento de registros a prueba de manipulaciones y procedimientos automatizados de copia de seguridad y archivo.
La transición a los libros de registro electrónicos aborda muchas observaciones comunes de la FDA 483 relacionadas con la integridad de los datos, incluidas las entradas retroactivas, las modificaciones no autorizadas y los registros incompletos. Las organizaciones que implementan libros de registro electrónicos informan que mejoraron la preparación para las inspecciones y redujeron los hallazgos sobre la integridad de los datos.