Ejecute laboratorios de control de calidad más inteligentes con LIMS impulsado por IA
Plataforma LIMS empresarial y sistema de gestión de información de laboratorio basado en la nube para productos farmacéuticos, biotecnológicos y ciencias biológicas reguladas, que ofrece automatización del flujo de trabajo de laboratorio, integración de instrumentos y cumplimiento normativo con IA integrada, ISO 17025, implementación de código bajo/sin código y el único ecosistema GxP digital integrado de la industria.
20%
Entrega más rápida
25%
Más muestras/cambio
100%
Integridad de datos
Fast
Implementación de 3 a 6 meses
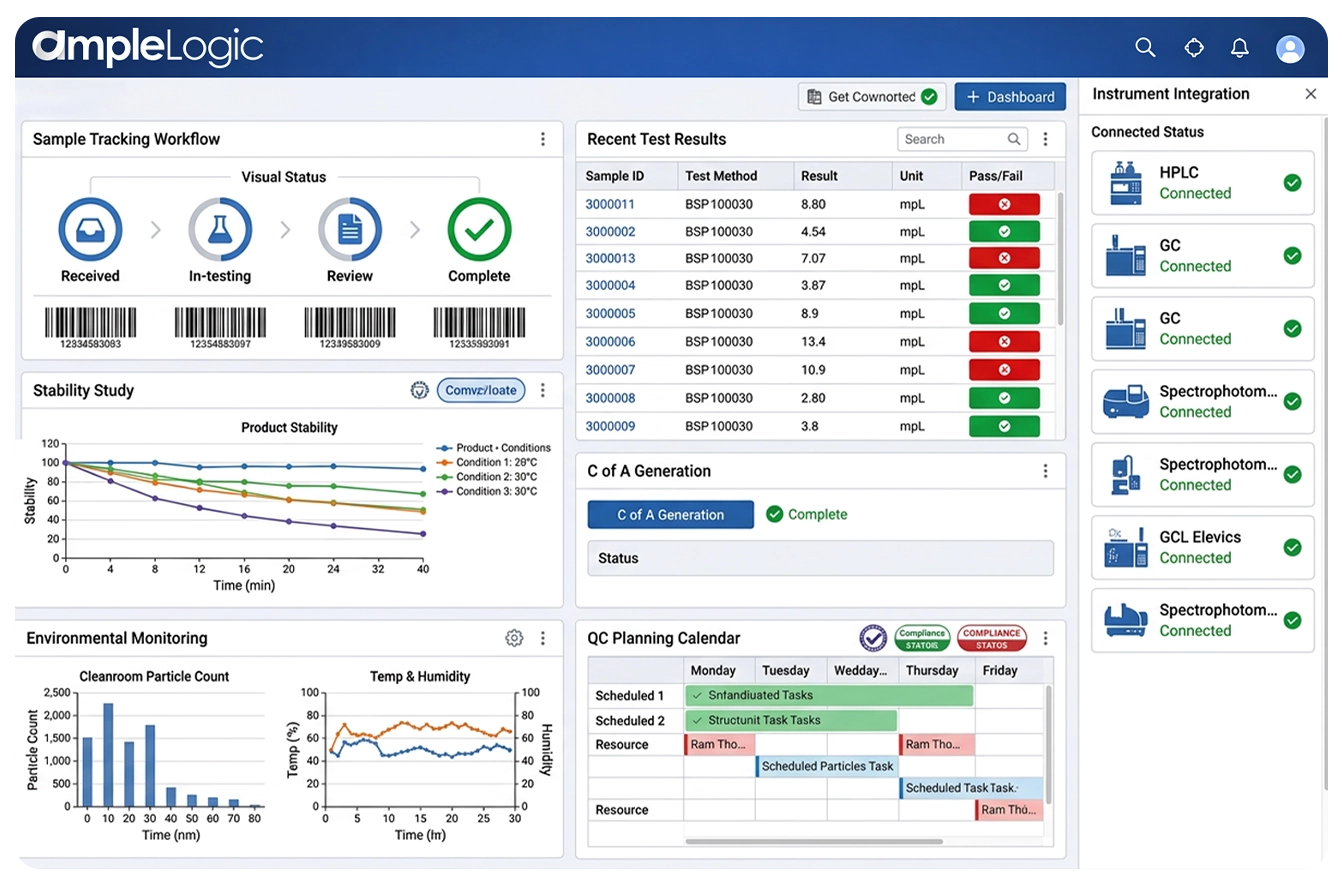
Ecosistema de laboratorio conectado: plataforma digital LIMS unificada
AmpleLogic LIMS crea una única fuente de verdad para las operaciones de laboratorio: elimina los silos de datos, reduce los errores de transcripción y permite la visibilidad en tiempo real en toda la empresa como un LIMS unificado en la nube y una plataforma de gestión de datos científicos.
Instrumentos analíticos
Analizadores de HPLC, GC, LC-MS, ICP-OES, UV-Vis, disolución y partículas conectados a través de interfaces bidireccionales validadas
Sistemas ERP
Integración perfecta con SAP, Oracle y NetSuite para liberación de lotes, inventario y gestión de materiales.
Ejecución de fabricación
Intercambio de datos en tiempo real con MES y eBMR para pruebas en proceso, registros de lotes y programación de producción.
Gestión de Calidad
Integración bidireccional con eQMS para activación de desviaciones, gestión CAPA e investigaciones OOS
Sistemas de datos de cromatografía
Conectores prediseñados para Empower, Chromeleon, OpenLab y MassLynx con importación automática de resultados
Gestión de documentos
PNT, métodos analíticos y especificaciones sincronizados con DMS para operaciones de laboratorio de control de calidad controladas por versiones
LIMS diseñado específicamente para laboratorios regulados por GxP
Registro de muestra
Inicio de sesión de muestra automatizado con escaneo de códigos de barras/RFID, registro a nivel de lote desde ERP/MES y planes de muestra configurables con asignaciones de prueba predefinidas
Seguimiento de muestras
Cadena de custodia en tiempo real con seguimiento de ubicación, gestión de almacenamiento, estado de retención/liberación y alertas automatizadas para acercarse a los plazos del SLA
Ejecución de prueba
Ejecución de métodos analíticos basados en plantillas con captura de datos de instrumentos, verificación de idoneidad del sistema y cálculos en línea con reglas de redondeo configurables.
Validación de resultados
Detección automatizada de OOS/OOT, evaluación de aprobación/rechazo basada en reglas, revisión multinivel y flujos de trabajo de aprobación con firmas electrónicas
Certificado de Análisis
COA/ROA generado automáticamente con plantillas configurables, agregación a nivel de lotes, formatos específicos del cliente y distribución digital
Informes regulatorios
Exportaciones de datos listos para inspección, informes de tendencias de estabilidad, paquetes de análisis estadístico y resultados formateados para presentaciones regulatorias para presentaciones ante FDA/EMA.
Registro de muestra
Inicio de sesión de muestra automatizado con escaneo de códigos de barras/RFID, registro a nivel de lote desde ERP/MES y planes de muestra configurables con asignaciones de prueba predefinidas
Seguimiento de muestras
Cadena de custodia en tiempo real con seguimiento de ubicación, gestión de almacenamiento, estado de retención/liberación y alertas automatizadas para acercarse a los plazos del SLA
Ejecución de prueba
Ejecución de métodos analíticos basados en plantillas con captura de datos de instrumentos, verificación de idoneidad del sistema y cálculos en línea con reglas de redondeo configurables.
Validación de resultados
Detección automatizada de OOS/OOT, evaluación de aprobación/rechazo basada en reglas, revisión multinivel y flujos de trabajo de aprobación con firmas electrónicas
Certificado de Análisis
COA/ROA generado automáticamente con plantillas configurables, agregación a nivel de lotes, formatos específicos del cliente y distribución digital
Informes regulatorios
Exportaciones de datos listos para inspección, informes de tendencias de estabilidad, paquetes de análisis estadístico y resultados formateados para presentaciones regulatorias para presentaciones ante FDA/EMA.
Panorama actual del software LIMS
Comprender el estado actual del software informático de laboratorio y las plataformas LIMS en el sector farmacéutico
La mayoría de los laboratorios ya cuentan con un LIMS
Presencia generalizada del sistema de referencia
Los LIMS existentes están muy personalizados y son difíciles de actualizar.
Las integraciones personalizadas crean fricciones en las actualizaciones
Alto coste de mantenimiento y validación.
Gasto continuo para mantenimiento y revalidación regulatoria.
Coexisten múltiples soluciones puntuales
El conjunto de herramientas fragmentado aumenta la carga de integración
Prioridades del director del laboratorio de control de calidad: validación y costo total de propiedad
Reducir la carga de validación de LIMS + Consolidar soluciones puntuales para reducir el costo total de propiedad (TCO) a largo plazo
Desafíos clave con el software LIMS existente
Flujos de trabajo fragmentados, procesos manuales y riesgos de cumplimiento
Centrado principalmente en el seguimiento de muestras
Limita la visibilidad más allá de la entrada y salida de la muestra.
- Limita la visibilidad de un extremo a otro
- Aumenta las transferencias manuales
- Aumenta el riesgo de cumplimiento
- Conduce a lanzamientos de productos más lentos
Estabilidad y EMS manejados fuera de LIMS
Las operaciones fragmentadas aumentan la complejidad y el riesgo
- Crea control operativo fragmentado
- Límites Alcance Cobertura
- Complica la validación
- Las unidades necesitan evaluar reemplazos
Dependencia de la hoja de cálculo
Los procesos manuales socavan el cumplimiento y la eficiencia
- Causas Actualizaciones de estado manuales
- Debilita las tendencias y las pistas de auditoría
- Aumenta las tasas de error
- Hace que los líderes dependan de los informes informales
Mala experiencia de usuario
Los sistemas heredados ralentizan la adopción y los flujos de trabajo
- Reduce la adopción
- Ralentiza los flujos de trabajo diarios
- Impulsa los desafíos de personalización
- Destaca la necesidad de mejoras en la integración
Desafíos de integración de instrumentos
Silos de instrumentos
HPLC, GC, LC-MS y microsistemas funcionan desconectados
Transferencia manual de datos desde CDS
Los sistemas de datos de cromatografía requieren pasos de entrada manual
Riesgos de integridad de los datos
Lagunas en el seguimiento de auditoría y posibles violaciones de cumplimiento
Carga de validación compleja
Cada conexión requiere pruebas exhaustivas de idoneidad del sistema.
Priorizar conectores validados
Las integraciones de instrumentos calificados y prediseñados reducen el riesgo
Priorizar el soporte de seguimiento de auditoría
Trazabilidad completa desde el instrumento hasta el informe
Priorizar y minimizar las transferencias manuales
Automatice la captura de datos para reducir errores y tiempo de ciclo
Capacidades principales del software LIMS
Funciones del software LIMS farmacéutico especialmente diseñadas para la gestión de operaciones de laboratorio modernas
Ejemplo de gestión del ciclo de vida
Software de seguimiento de muestras empresarial que proporciona gestión integral del ciclo de vida de las muestras, desde el registro hasta el análisis, la generación de informes y la disposición.
Ejecución de pruebas y métodos
Definir y ejecutar procedimientos analíticos con total trazabilidad.
Conectividad del instrumento
Software de integración de instrumentos para una conectividad perfecta con instrumentos de laboratorio de control de calidad, sistemas de datos de cromatografía e integración LIMS ELN
Manejo de códigos de barras y RFID
Identificación automatizada de muestras y seguimiento de gestión de inventario de laboratorio de control de calidad
Flujos de trabajo de control de calidad
Verificaciones de control de calidad, aprobaciones y verificación de cumplimiento integradas en toda la plataforma de laboratorio digital
Firmas electrónicas y pistas de auditoría
Software de laboratorio compatible con la FDA con requisitos completos de 21 CFR Parte 11, LIMS compatible con GxP y LIMS compatible con ISO 17025
Informes personalizables
Plataforma de análisis de laboratorio con COA, ROA, análisis de rendimiento de laboratorio flexibles y generación de informes preparados para la normativa
Paneles intuitivos
Paneles de gestión de operaciones de laboratorio en tiempo real con KPI, análisis de datos científicos y análisis del rendimiento del laboratorio.
Módulos LIMS avanzados para laboratorios farmacéuticos
Soluciones LIMS diseñadas específicamente para operaciones de laboratorio especializadas
Gestión avanzada de estabilidad
Software de gestión de estudios de estabilidad compatible con ICH para productos farmacéuticos y biotecnológicos
AmpleLogic Advanced Stability Management es un sistema de gestión de pruebas de estabilidad diseñado específicamente para gestionar el ciclo de vida completo del estudio de estabilidad, desde la creación del protocolo de estabilidad y la programación de extracción de muestras hasta la gestión del almacenamiento en cámara, la ejecución de pruebas, el análisis de tendencias de estabilidad y la generación de informes preparados para la normativa.
Características clave
Creación de protocolo de estabilidad
Defina protocolos de estabilidad que cumplan con ICH Q1A con diseños de estudio configurables, condiciones de almacenamiento, criterios de aceptación y programas de muestreo automatizados.
Programación de muestras de estabilidad
Programación automatizada de extracción de muestras con recordatorios basados en calendario, reprogramación dinámica y seguimientos de auditoría completos
Cámara y Monitoreo Ambiental
Supervise las condiciones de almacenamiento de estabilidad, como la temperatura y la humedad, en cámaras de estabilidad y almacenes.
Ejecución de pruebas y captura de datos
Ejecute pruebas analíticas dentro del mismo flujo de trabajo LIMS con integración directa de instrumentos y trazabilidad completa.
Análisis e informes de tendencias de estabilidad
Análisis de tendencias estadístico automatizado con ajuste de curvas de degradación, gráficos de control e informes de estabilidad listos para la regulación.
Determinación de la vida útil basada en IA
Proyección de vida útil basada en aprendizaje automático con intervalos de confianza, alertas de riesgo de vencimiento temprano y predicción de estabilidad acelerada
Determinación de vencimiento y gestión de fecha de nueva prueba
Determinación sistemática de la caducidad basada en datos de tendencias de estabilidad, cálculo de la fecha de nueva prueba y soporte automatizado de reclamo de etiquetas
Cumplimiento normativo ICH Q1A
Alineación incorporada con las pautas de estabilidad ICH Q1A-Q1F para programas de estabilidad farmacéutica y biotecnológica
Cumplimiento de los requisitos de estabilidad de la FDA
Flujos de trabajo preconfigurados que cumplen con los requisitos de estabilidad de la FDA, incluido 21 CFR Parte 211.166
Gestión del programa de estabilidad GMP
Programas integrales de estabilidad GMP con compromisos de estabilidad continuos y monitoreo posterior a la aprobación.
Análisis de tendencias de estabilidad y predicción de vida útil
La IA analiza los resultados de las pruebas de estabilidad para identificar tendencias de degradación del producto y estimar la vida útil del producto.
Beneficios clave
Acelere la ejecución de estudios de estabilidad con programación y gestión de protocolos automatizadas
Reduzca el tiempo de determinación de la vida útil en un 40 % con análisis de tendencias impulsado por IA
Garantice el cumplimiento normativo total con flujos de trabajo alineados con ICH Q1A, FDA y GMP
Elimine las extracciones de muestras perdidas con la programación automatizada de extracción de muestras
Centralice la gestión del almacenamiento en cámara con monitoreo ambiental en tiempo real
11 características de IA que transforman las operaciones LIMS farmacéuticas
Desde la verificación de estándares de referencia impulsada por IA y asistentes virtuales de laboratorio de control de calidad hasta el mantenimiento predictivo y el procesamiento de documentos OCR: AmpleLogic LIMS incorpora la automatización inteligente en cada flujo de trabajo del laboratorio.
Verificación del catálogo de estándares de referencia de IA para laboratorios farmacéuticos
La IA verifica automáticamente el catálogo de estándares de referencia y lo compara con los estándares utilizados actualmente en el laboratorio, identificando estándares actualizados, vencidos, con cambios de versión y recientemente disponibles para garantizar el cumplimiento normativo.
- Garantiza el uso correcto del estándar de referencia.
- Evita el uso estándar obsoleto
- Actualizaciones automatizadas del catálogo y seguimiento de versiones.
Asistente de laboratorio de IA (LIMS-MAN): Entrenador virtual de LIMS
Asistente virtual inteligente integrado en la plataforma LIMS. Los usuarios interactúan con consultas en lenguaje natural como "¿Cuál es el estado del lote B12345?" o 'Mostrar resultados de ensayo para el Producto X': recuperar datos de laboratorio al instante y actuar como entrenador virtual para nuevos usuarios.
- Acceso más rápido a la información del laboratorio
- Reducción del tiempo de formación para nuevos usuarios.
- Navegación LIMS y toma de decisiones simplificadas
Preparación automatizada de hojas de trabajo impulsadas por IA para laboratorios de control de calidad
La IA analiza datos STP (procedimiento de prueba estándar), incluidos parámetros de prueba, fórmulas de cálculo, reactivos necesarios, detalles del instrumento y criterios de aceptación, para generar dinámicamente hojas de trabajo digitales listas para usar para los analistas.
- Generación automática de hojas de trabajo de prueba a partir de datos STP
- Población inteligente de campos de cálculo
- Eliminación de errores de transcripción.
Motor de optimización de recursos de IA para operaciones de laboratorio
El optimizador de recursos impulsado por IA analiza datos de pruebas históricos y predice los requisitos futuros del laboratorio, estimando los reactivos necesarios, los estándares de referencia, los consumibles y el tiempo de utilización de los instrumentos para los próximos lotes.
- Planificación de adquisiciones y gestión de inventario precisas
- Reducción de la escasez y el desperdicio de reactivos
- Utilización optimizada de los instrumentos y reducción de costes.
Revisión automatizada de resultados y análisis de tendencias de IA (revisor virtual)
El revisor virtual impulsado por IA analiza continuamente datos analíticos: detecta errores durante el análisis, revisa pistas de auditoría automáticamente, identifica tendencias anormales, problemas de integridad de datos, resultados OOT y marca desviaciones del método de análisis.
- Revisión de resultados más rápida con información basada en IA
- Detección temprana de problemas de calidad y tendencias OOT
- Carga de trabajo de revisión manual reducida
Evaluación de cromatogramas basada en IA para HPLC, GC y UPLC
La IA evalúa cromatogramas de instrumentos HPLC, GC y UPLC, evaluando automáticamente las áreas de los picos, los tiempos de retención, la simetría de los picos, la resolución y las desviaciones estándar. Alerta a los analistas inmediatamente cuando se detectan desviaciones de los patrones estándar.
- Revisión automatizada de datos cromatográficos.
- Detección de picos anormales y problemas de integración.
- Automatización de revisión en proceso para conjuntos de muestras
Predicción de estabilidad y vida útil impulsadas por IA
Los algoritmos de aprendizaje automático analizan datos históricos de estudios de estabilidad para predecir el comportamiento futuro del producto, estimando la vida útil, las tendencias de degradación, las probabilidades de variación de la estabilidad y el riesgo de fallas en las especificaciones.
- Identificación temprana de posibles problemas de estabilidad
- Predicciones de vida útil basadas en datos con intervalos de confianza
- Documentación regulatoria mejorada para programas de estabilidad.
Predicción de fallas de instrumentos de IA y mantenimiento predictivo
La IA monitorea continuamente los datos de rendimiento de los instrumentos (registros de calibración, horas de uso, registros de errores, historial de mantenimiento y tendencias de rendimiento) utilizando análisis predictivos para estimar los niveles de riesgo de fallas y generar puntuaciones de riesgo de los instrumentos.
- Alertas de mantenimiento predictivo ante fallos
- Reducción del tiempo de inactividad y retrasos del instrumento.
- Programación de mantenimiento optimizada
Estimación del tiempo de muestreo impulsada por IA para control de calidad farmacéutico
El motor de IA analiza datos de muestreo históricos según el tipo de producto, la categoría de material, la cantidad de contenedores, el tamaño del lote y la complejidad del procedimiento de muestreo para estimar el tiempo de muestreo esperado para cada lote.
- Mejora de la programación del laboratorio y la planificación de la fuerza laboral
- Reducción de los retrasos en el muestreo
- Mayor eficiencia operativa
Procesamiento de documentos habilitado por OCR para datos de laboratorio
El reconocimiento óptico de caracteres (OCR) extrae automáticamente información de los documentos cargados, incluidos archivos PDF, imágenes, informes escaneados, certificados y registros escritos a mano, convirtiéndolos en registros digitales estructurados integrados en la base de datos LIMS.
- Extracción automatizada de datos de documentos escaneados
- Eliminación de la entrada de datos manual
- Procesamiento de documentos más rápido y accesibilidad mejorada
Predicción TAT de pruebas de muestras de IA para la eficiencia del laboratorio
La IA analiza las duraciones históricas de las pruebas y predice el tiempo de finalización esperado para cada muestra, considerando la complejidad del método de prueba, la disponibilidad de los instrumentos, la carga de trabajo de los analistas y las duraciones históricas de las pruebas para un pronóstico TAT preciso.
- Previsión precisa del tiempo de respuesta
- Programación y priorización de muestras mejoradas
- Mayor productividad del laboratorio
Arquitectura de flujo de trabajo LIMS
Automatización integral del flujo de trabajo del laboratorio, desde la ingesta de muestras hasta los informes regulatorios.
Datos maestros
Productos, Métodos, Instrumentos, Usuarios, Estándares
Estabilidad
Estudios y vida útil
Calificación
Validación de CI/OQ/PQ
COA/ROA
Reguladora
Datos maestros
- •Productos
- •Métodos
- •Instrumentos
- •Usuarias
- •Estándares de calidad
Gestión Auxiliar
- •Gestión de activos
- •Seguimiento de químicos y reactivos
- •Gestión de columnas
- •Estándares de referencia
- •Preparación de la solución
- •Gestión de medios
- •Gestión Cultural
Ciclo de vida de muestra
- •Registro de muestra
- •Recogida y recepción
- •Iniciar sesión en el sistema
- •Asignación a pruebas
- •Ejecución del análisis
- •Revisión y aprobación de resultados
- •Certificado de Análisis (COA)
Salida regulatoria
- •Certificado de Análisis (COA)
- •Informe de Análisis (ROA)
- •Presentaciones regulatorias
Integridad de datos LIMS y cumplimiento normativo
Integridad de datos ALCOA+, 21 CFR Parte 11, Anexo 11 de la UE, ISO 17025 y cumplimiento de GxP: integrado en la plataforma LIMS empresarial AmpleLogic
Marco de integridad de datos ALCOA+
Cada punto de datos es atribuible, legible, contemporáneo, original y preciso, con extensiones completas, consistentes, duraderas y disponibles integradas en la plataforma.
- Pistas de auditoría inmutables para cada cambio de datos
- Firmas electrónicas con intención y significado.
- Copia de seguridad automatizada con validación de recuperación de datos
- Arquitectura de almacenamiento de datos a prueba de manipulaciones
Cumplimiento de FDA 21 CFR Parte 11
Firmas y registros electrónicos prevalidados con controles de sistema cerrado, comprobaciones de autoridad y verificación de dispositivos para laboratorios regulados por la FDA.
- Flujos de trabajo de firma electrónica configurables
- Comprobaciones de autoridad y control de acceso basado en roles
- Registros de auditoría atribuibles y con sello de tiempo
- Arquitectura de seguridad de sistema cerrado
Cumplimiento del Anexo 11 de la UE
Controles de sistemas computarizados para la fabricación farmacéutica europea, incluidos requisitos de validación, almacenamiento de datos, impresiones y continuidad del negocio.
- Soporte de validación del sistema computarizado (IQ/OQ/PQ)
- Controles de migración y archivo de datos
- Continuidad del negocio y recuperación ante desastres
- Documentación de calificación del proveedor
Cumplimiento normativo GxP
Cumplimiento integral de buenas prácticas en entornos GLP, GMP y GCP con controles integrados para ICH, OMS, PIC/S y más de 16 autoridades sanitarias globales.
- Plantillas de flujo de trabajo GLP, GMP, GCP
- Alineación de las pautas ICH Q2, Q7, Q10
- Paquetes de informes listos para la inspección
- Control de cambios y soporte de revalidación
Ecosistema GxP digital integrado para laboratorios farmacéuticos y biotecnológicos
El LIMS farmacéutico de AmpleLogic se integra de forma nativa con 13 soluciones GAMP, una ventaja competitiva que ningún otro proveedor puede igualar.
OOS produce desviaciones de activación automática; Los resultados de CAPA actualizan los métodos de prueba; controles de cambios gestionar actualizaciones de procedimientos analíticos
Bidireccional: OOS → Desviaciones, CAPA → Actualizaciones de métodos
Los datos de estabilidad y los COA se incorporan directamente a las presentaciones regulatorias; actualizaciones del estado del registro requisitos de prueba de muestra
LIMS → Datos de estabilidad → Envíos de RIMS
Muestras en proceso creadas automáticamente a partir de registros de lotes; Los resultados del control de calidad desencadenan decisiones de liberación de lotes; datos medioambientales vinculados a lotes
Bidireccional: muestras por lotes ↔ resultados de control de calidad
Los datos de tendencias de control de calidad, los resultados de estabilidad y las estadísticas OOS completan automáticamente los informes anuales de revisión de productos sin necesidad de compilación manual.
LIMS → Tendencias de control de calidad + Estadísticas OOS → Informes APQR
SOP, métodos analíticos y especificaciones controlados por versiones en DMS; documentos efectivos vinculados automáticamente en la ejecución de pruebas LIMS
DMS → Documentos controlados → Ejecución del método LIMS
Cualificaciones de los analistas verificadas antes de la ejecución de la prueba; La finalización de la formación activa automáticamente el acceso al método analítico.
LMS → Estado de capacitación → Calificación de analista de LIMS
Los datos de las pruebas de lanzamiento y durante el proceso alimentan los modelos estadísticos CPV para el monitoreo continuo de la capacidad del proceso.
LIMS → Datos de proceso → Análisis estadístico CPV
Datos de seguimiento de salas blancas vinculados a lotes de producción; las excursiones activan flujos de trabajo automatizados de retención/liberación en LIMS
EMS → Datos medioambientales → Retención/liberación de lotes LIMS
A diferencia de los proveedores de LIMS de análisis modulares, centrados en I+D o empresariales heredados, AmpleLogic es el único proveedor que ofrece un ecosistema GxP completo e integrado de forma nativa donde los datos LIMS fluyen sin problemas a través de sistemas de calidad, regulatorios, de fabricación y de cumplimiento sin middleware.
Integración LIMS empresarial: ERP, ELN y conectividad de instrumentos
Conecte su plataforma LIMS empresarial a todo su ecosistema operativo
Instrumentos de laboratorio
Conectividad perfecta con equipos analíticos
- Espectrometría de masas (MS)
- HPLC
- GC
- ICP-OES
- UV-Vis
Sistemas empresariales
Integración con sistemas empresariales y de fabricación.
- SAVIA
- Oráculo
- NetSuite
- MES (Sistema de ejecución de fabricación)
- SGC (Sistema de Gestión de Calidad)
- DMS (Sistema de Gestión de Documentos)
- ELN (Cuaderno de Laboratorio Electrónico)
Datos y análisis
Conéctese a almacenes de datos e inteligencia empresarial
- Almacenes de datos
- Plataformas BI (Inteligencia Empresarial)
- Motores de IA/ML
- Análisis de la nube
Opciones de conectividad
Múltiples protocolos para una integración flexible
- Más de 100 conectores prediseñados
- API REST
- SFTP
- Conexiones directas de bases de datos
- HL7 (Protocolos sanitarios)
Arquitectura API-First
Plataforma moderna y extensible para necesidades de integración personalizadas
- API RESTful
- Soporte de webhook
- Conectores personalizados
- Marcos de integración de terceros
Cumplimiento automatizado de LIMS: elimine las comprobaciones manuales repetitivas
La plataforma que prioriza la automatización reduce los gastos generales de verificación manual
Verificaciones automatizadas basadas en reglas
Elimine las comprobaciones manuales de control de calidad con lógica empresarial configurable y reglas de cumplimiento
Ejecución de métodos basados en plantillas
Las plantillas preconfiguradas garantizan una ejecución consistente y reducen la configuración manual
Estado de calificación del instrumento en tiempo real
Seguimiento automático de la idoneidad del sistema y los programas de mantenimiento.
Armonización de datos maestros
Fuente única de verdad para estándares, métodos y procedimientos en todo el laboratorio de control de calidad
Revisiones basadas en excepciones
Centrar la atención de los analistas en las desviaciones y los resultados fuera de especificaciones.
Flujo de proceso de un extremo a otro
Enrutamiento automatizado de muestras y resultados a través de un flujo de trabajo de laboratorio completo
ROI del software LIMS: impacto empresarial medible para los laboratorios de calidad
Resultados reales de la transformación LIMS
+25%
Impacto en el tiempo del ciclo
-20%
Pérdida de rendimiento
+30%
Carga de trabajo de cumplimiento
20%
Reducción de TAT
Tiempo de respuesta un 20% más rápido para resultados analíticos
25%
Aumento de la productividad
25 % más de muestras procesadas por turno de analista
90%
Preparación para la auditoría
Reducción del 90 % en el tiempo para cerrar las observaciones.
El costo oculto de los LIMS heredados
Tiempo de inactividad del equipo
Los instrumentos permanecen sin uso entre cambios manuales
10-30% de pérdida de capacidad
Cuello de botella de la analista
Las verificaciones y aprobaciones manuales ralentizan la entrega de resultados
Retrasos en la entrega de muestras
Silos de datos en todos los sistemas
ELN, MES y CDS funcionan de forma independiente
Consolidación manual y riesgo de error
Comprobaciones manuales repetitivas
Verificaciones idénticas realizadas en cada paso.
+25 % de inflación del tiempo de ciclo
Gastos generales de validación y control de cambios
Se requieren pruebas exhaustivas para cualquier modificación del sistema.
+30% de carga de trabajo de cumplimiento
Cómo LIMS inteligente de código bajo supera a las plataformas tradicionales
Comparación lado a lado de los enfoques de implementación
| Dimensión | Monolítico heredado | Modulares Tradicionales | Código bajo inteligente |
|---|---|---|---|
| Cronograma de implementación | 18-24 meses | 12-18 meses | 3-6 meses |
| Costo total de propiedad (TCO) | 2,5-3,5 millones de dólares | 1,8-2,5 millones de dólares | 1,0-1,5 millones de dólares |
| IA y análisis | Legado, limitado a informes | Capacidades adicionales, costo adicional | IA integrada, análisis predictivo nativo |
| Personalización y flexibilidad | Alta carga de control de cambios codificada de forma rígida | Modular pero requiere desarrolladores | Código bajo/sin código, los usuarios empresariales pueden configurar |
Cronograma de implementación
Legado: 18-24 meses
Tradicional: 12-18 meses
Inteligente: 3-6 meses
Costo total de propiedad (TCO)
Legado: 2,5-3,5 millones de dólares
Tradicional: 1,8-2,5 millones de dólares
Inteligente: 1,0-1,5 millones de dólares
IA y análisis
Legado: Legado, limitado a informes
Tradicional: Capacidades adicionales, costo adicional
Inteligente: IA integrada, análisis predictivo nativo
Personalización y flexibilidad
Legado: Alta carga de control de cambios codificada de forma rígida
Tradicional: Modular pero requiere desarrolladores
Inteligente: Código bajo/sin código, los usuarios empresariales pueden configurar
AmpleLogic LIMS: posicionamiento en el mercado y ventaja competitiva
Cómo se compara AmpleLogic con los proveedores de LIMS establecidos
| Categoría | Vendedoras | Posicionamiento | Limitación |
|---|---|---|---|
| LIMS empresarial heredado | Vendedores Tradicionales | Base de clientes farmacéutica establecida y altamente configurable, amplio soporte de instrumentos | Implementaciones de 18 a 24 meses, se requiere mucha personalización, alto costo total de propiedad, sin ecosistema GxP integrado |
| Plataformas de I+D empresarial | Proveedores centrados en I+D | Modelado molecular + informática de laboratorio, plataformas en la nube, asistentes AI/GenAI | I+D centrado, no en control de calidad, costoso, dependencia del proveedor en ecosistemas cerrados, integración de fabricación limitada |
| Plataformas de laboratorio digitales modernas | Startups nativas de la nube | UX moderno, nativo de la nube, API primero, implementación rápida para I+D | Capacidades limitadas de control de calidad farmacéutico, cumplimiento normativo débil, no validado por GMP para la fabricación |
| LIMS de análisis modular | Proveedores de análisis primero | Análisis/ML integrados, HTML5 nativo de la nube, pila LIMS+ELN+LES+SDMS integrada | Implementación compleja, ecosistema GxP limitado, las funciones de IA requieren una sobrecarga de validación |
| Plataforma GxP integrada | AmpleLogic | Informática de laboratorio impulsada por IA + ecosistema GxP digital completo (13 soluciones GAMP), Low-Code/No-Code, implementación de 3 a 6 meses | Los participantes más nuevos construyen una base de referencia empresarial |
LIMS empresarial heredado
Vendedores TradicionalesPosicionamiento: Base de clientes farmacéutica establecida y altamente configurable, amplio soporte de instrumentos
Limitación: Implementaciones de 18 a 24 meses, se requiere mucha personalización, alto costo total de propiedad, sin ecosistema GxP integrado
Plataformas de I+D empresarial
Proveedores centrados en I+DPosicionamiento: Modelado molecular + informática de laboratorio, plataformas en la nube, asistentes AI/GenAI
Limitación: I+D centrado, no en control de calidad, costoso, dependencia del proveedor en ecosistemas cerrados, integración de fabricación limitada
Plataformas de laboratorio digitales modernas
Startups nativas de la nubePosicionamiento: UX moderno, nativo de la nube, API primero, implementación rápida para I+D
Limitación: Capacidades limitadas de control de calidad farmacéutico, cumplimiento normativo débil, no validado por GMP para la fabricación
LIMS de análisis modular
Proveedores de análisis primeroPosicionamiento: Análisis/ML integrados, HTML5 nativo de la nube, pila LIMS+ELN+LES+SDMS integrada
Limitación: Implementación compleja, ecosistema GxP limitado, las funciones de IA requieren una sobrecarga de validación
Plataforma GxP integrada
AmpleLogicPosicionamiento: Informática de laboratorio impulsada por IA + ecosistema GxP digital completo (13 soluciones GAMP), Low-Code/No-Code, implementación de 3 a 6 meses
Limitación: Los participantes más nuevos construyen una base de referencia empresarial
Reconocimiento de analistas de software LIMS y premios de la industria
Con la confianza de organizaciones líderes y el reconocimiento de analistas
Radar de escarcha: cuadrante líder
Escarcha y Sullivan
Reconocido como líder en espacio LIMS de código bajo con una implementación 10 veces más rápida
Más de 120 implementaciones globales
AmpleLogic
Historial comprobado con clientes empresariales y compañías Fortune 500
Evaluación de Gartner 2024-2025
Gartner
Incluido en el Cuadrante Mágico de Gartner para la evaluación LIMS con credibilidad de terceros
2024-2025
"Interfaz fácil de usar y fácil de usar para la gestión del laboratorio. Redujo el trabajo manual y nos ayudó a avanzar hacia flujos de trabajo de laboratorio completamente sin papel."
Gerente de laboratorio
Control de calidad farmacéutico
"Buen soporte del proveedor y capacidad de respuesta durante la implementación. Las capacidades de integración de instrumentos simplificaron significativamente nuestros flujos de trabajo de pruebas de control de calidad."
Analista de control de calidad
Ciencias de la vida
"Los módulos de gestión de estabilidad y programación de muestras son excepcionales. La visibilidad de datos en tiempo real en todas las operaciones del laboratorio ha sido transformadora para nuestro equipo."
Usuario verificada de G2
Director de laboratorio
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.