Gestione cada evento de calidad en un eQMS integrado
AmpleLogic ofrece una plataforma de software QMS farmacéutico basada en la nube y basada en IA diseñada para el cumplimiento a nivel empresarial. Nuestra plataforma QMS digital unifica la gestión CAPA, la gestión de desviaciones, el control de cambios, las auditorías y la calidad de los proveedores en una solución de software de gestión de eventos de calidad compatible con GxP, en la que confían empresas farmacéuticas, biotecnológicas y de dispositivos médicos de todo el mundo.
11+
Módulos QMS integrados
100%
Cumple con 21 CFR Parte 11
50%
Cierre CAPA más rápido
300+
Implementaciones globales
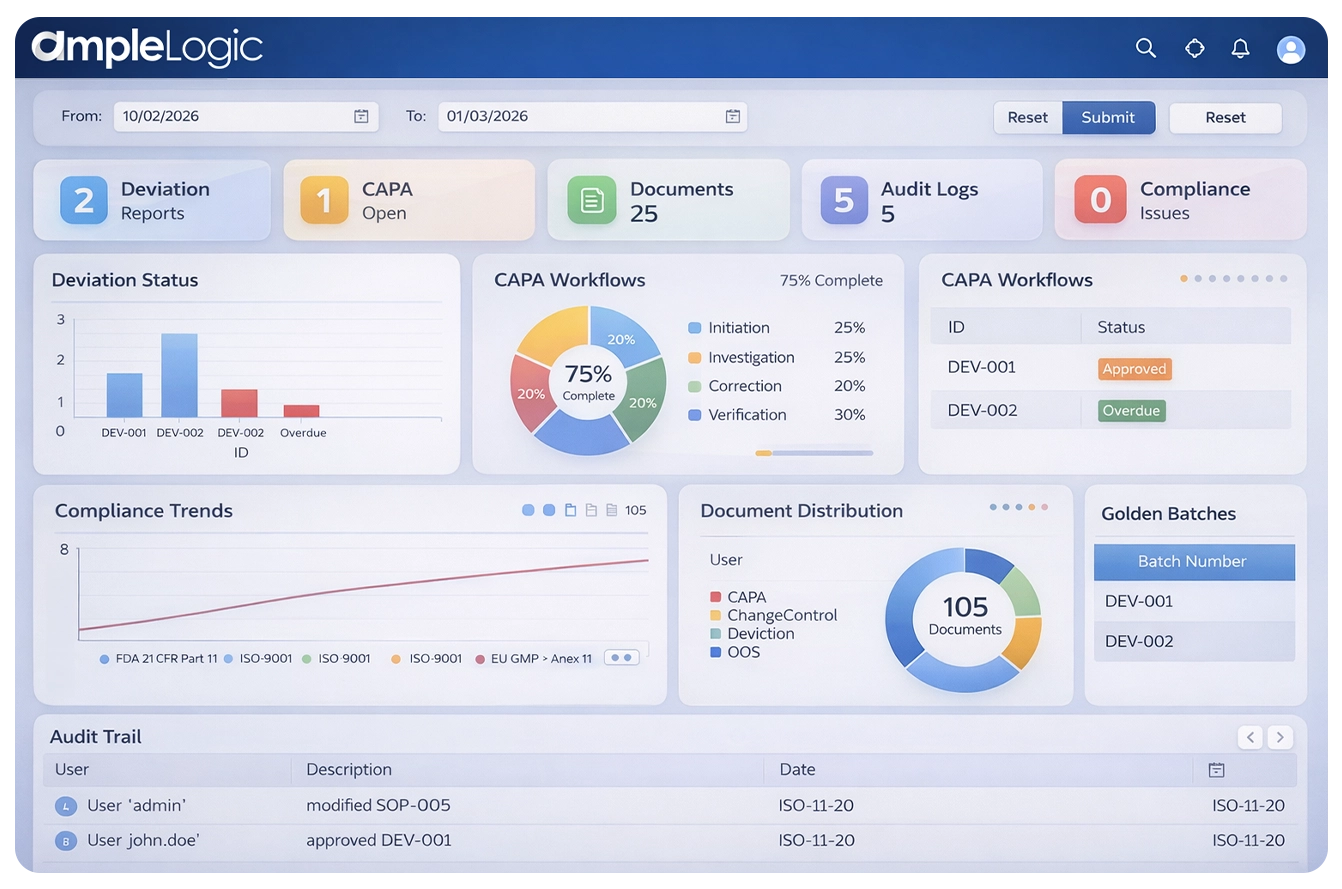
Por qué el software heredado del sistema de gestión de calidad se queda corto
Cómo los procesos manuales fragmentados en el software de gestión de cumplimiento farmacéutico y los sistemas de gestión de calidad GMP heredados generan retrasos en los eventos de calidad, brechas en el software de gestión de no conformidades y mayores costos de calidad
Incumplimiento regulatorio
Alto riesgo de sanciones debido a errores de documentación manual, falta de pistas de auditoría y trazabilidad limitada: problemas que el software de sistema de gestión de calidad compatible con GxP elimina
Sistemas de calidad aislados
Los módulos QMS independientes con integraciones débiles dan como resultado investigaciones retrasadas, entrada de datos duplicada y cierres prolongados de CAPA en todo el sistema de gestión de calidad empresarial.
Sin análisis en tiempo real
La falta de paneles de control en gestión de desviaciones, CAPA, control de cambios y OOS limita la toma de decisiones proactiva y la visibilidad de riesgos sin una plataforma de gestión de calidad digital.
Ciclos de investigación lentos
Las investigaciones en papel o por correo electrónico tardan entre 2 y 4 veces más que los flujos de trabajo digitales en el software moderno de gestión de calidad farmacéutica, lo que retrasa la liberación de lotes.
Colaboración externa limitada
No hay acceso de socios en tiempo real para la gestión de calidad de proveedores, investigaciones de CDMO o coordinación de laboratorios contratados: una brecha que resuelve el software QMS basado en la nube
Brechas de alineación global
Las operaciones en múltiples sitios luchan con procesos inconsistentes, datos fragmentados e incapacidad para consolidar métricas de calidad sin un sistema de gestión de calidad empresarial.

Manual del costo de quedarse
Sistema de gestión de calidad empresarial: ventajas
Plataforma SaaS QMS basada en la nube con control del ciclo de vida, cumplimiento normativo, automatización del flujo de trabajo de calidad y plataforma de calidad empresarial validada para productos farmacéuticos y biotecnológicos.
Eficacia de circuito cerrado
Verificación integrada para flujos de trabajo de software de gestión de auditoría, control de cambios, desviaciones y gestión de CAPA
Verdadera trazabilidad de extremo a extremo
Enlace con un solo clic entre gestión de desviaciones, CAPA, cambios, quejas, OOS/OOT y registros de auditoría en un sistema de gestión de la calidad unificado
Listo para auditoría en todo momento
Ensamblaje de evidencia automatizado, pistas de auditoría inmutables y paneles de inspección para operaciones de SGC que cumplen con FDA 21 CFR Parte 11
Soporte de decisiones basado en riesgos
Priorizar acciones utilizando puntuación de riesgo y datos históricos de calidad dentro del sistema de gestión de calidad empresarial.
Inteligencia de calidad asistida por IA
RCA, detección de anomalías y verificación de eficacia más rápidas con capacidades del sistema de gestión de calidad impulsado por IA
Escalamiento automatizado y recordatorios
Recordatorios basados en riesgos y cronogramas con escalamiento automático en todo el software de gestión de cumplimiento farmacéutico
Por qué AmpleLogic: software QMS en la nube creado para las ciencias biológicas
Software de gestión de calidad farmacéutica líder en la industria con retorno de la inversión comprobado y defensa regulatoria
El costo de la calidad manual
Los procesos de calidad manuales aumentan los errores, las demoras y los costos operativos: el software QMS en la nube elimina estas ineficiencias
Motor de recomendación inteligente
Recomendaciones inteligentes basadas en datos para acelerar la resolución de problemas en su plataforma de gestión de calidad digital
Ventaja de aPaaS basada en la nube
El software QMS de código bajo y basado en la nube acelera la implementación, la personalización y la implementación en múltiples sitios para la gestión de la calidad farmacéutica.
Cumplimiento y validación de GxP
El sistema de gestión de calidad que cumple con GxP con controles integrados FDA 21 CFR Parte 11 garantiza que los procesos cumplan con los estándares regulatorios y pasen las auditorías.
Métricas de ROI cuantificables
Mide las ganancias de eficiencia y los ahorros de costos al implementar software de sistema de gestión de calidad empresarial en todas las operaciones.
Integraciones perfectas
Se conecta sin esfuerzo con LIMS, eBMR, DMS, ERP y el software de sistema de gestión de calidad existente en su pila de tecnología.
CAPA, Desviaciones, Auditoría y Gestión de Calidad de Proveedores
Explore cada módulo de nuestro software de sistema de gestión de calidad: software de gestión CAPA, software de gestión de desviaciones, software de gestión de control de cambios, software de gestión de auditorías, software de gestión de quejas, software de gestión de riesgos de calidad, calidad de proveedores y gestión de no conformidades.
Gestión de desviaciones
Sistema de gestión de eventos de calidad farmacéutica
Gestión integral del ciclo de vida de las desviaciones para la fabricación farmacéutica: desde la detección hasta el cierre con trazabilidad completa, clasificación basada en riesgos y defensa de GMP.
Gestión CAPA
Software de gestión CAPA farmacéutica
Ciclo de vida de las acciones correctivas y preventivas de circuito cerrado: desde el inicio hasta la investigación de la causa raíz, la automatización del flujo de trabajo y el seguimiento de la eficacia con el cumplimiento de la FDA y las GxP.
Control de cambios
Planificar, evaluar, implementar, verificar
Gestione los cambios planificados y no planificados en procesos, equipos, materiales y sistemas con análisis de impacto estructurado, aprobación de múltiples partes interesadas y revisión posterior a la implementación.
Gestión de Auditoría
Software de gestión de auditorías para sistemas de calidad farmacéutica
Gestión de auditorías internas, externas y de proveedores con planificación automatizada, programación, integración de hallazgos a CAPA y paneles de preparación para inspecciones regulatorias.
Gestión de quejas
Gestión de quejas impulsada por IA para sistemas de calidad farmacéutica
Ciclo de vida de quejas de principio a fin, desde la recepción multicanal hasta la investigación, los informes regulatorios y el seguimiento de la resolución con trazabilidad completa hasta los eventos de calidad relacionados.
Gestión de OOS
Software de gestión OOS para investigaciones fuera de especificación
Flujos de trabajo estructurados de investigación fuera de especificación de Fase I y Fase II alineados con la guía de la FDA con rigor científico y completa defensa regulatoria.
Gestión OOT
Análisis fuera de tendencia
Monitoreo estadístico de tendencias y flujos de trabajo de investigación basados en alertas para detectar cambios graduales en la calidad antes de que se conviertan en eventos OOS, lo que permite una gestión de calidad proactiva.
Gestión de incidentes de laboratorio
Software de gestión de incidentes de laboratorio para laboratorios de control de calidad farmacéuticos
Realice un seguimiento e investigue el mal funcionamiento de los instrumentos, la contaminación de las muestras, las desviaciones ambientales y los errores de los analistas con flujos de trabajo estructurados de acciones correctivas y cumplimiento de GxP.
Gestión de riesgos de calidad
Sistema de gestión de riesgos de calidad impulsado por IA
Gestión de riesgos alineada con ICH Q9 con FMEA, análisis de espina de pescado, puntuación de riesgos, identificación de riesgos basada en IA y paneles de control de riesgos empresariales para decisiones de calidad proactivas.
Calificación del vendedor/proveedor
Software de gestión de calidad y calificación de proveedores
Gestión integral del ciclo de vida de los proveedores: desde la calificación inicial hasta el monitoreo continuo del desempeño, la programación de auditorías basada en riesgos y la recalificación periódica.
Gestión de retirada de productos
Iniciar, ejecutar, informar, cerrar
Inicio y ejecución rápidos de retiros con trazabilidad a nivel de lotes, gestión de notificaciones regulatorias, seguimiento de comunicaciones con el cliente y evaluación de efectividad posterior al retiro.
Ciclo de vida de CAPA: comprobaciones de eficacia
Control del ciclo de vida, captura de evidencia y automatización para la defensa regulatoria
Detección
Identificar problemas de desviaciones, quejas, auditorías, OOS/OOT. Clasifica automáticamente eventos y vincula registros de origen.
Investigación
Análisis de causa raíz con cronogramas, seguimiento de datos y evaluación de riesgos. Los patrones históricos guían las investigaciones.
Plan de acción
El sistema recomienda acciones relevantes, prioridad de riesgo y mejores prácticas comprobadas.
Implementación
Ejecutar acciones, adjuntar pruebas, actualizar desvíos vinculados, cambios y registros de quejas.
Inteligencia de eficacia de la IA
AI compara cada CAPA nuevo con CAPA abiertos de verificación de efectividad de naturaleza similar: señala superposiciones, recomienda consolidación y evita investigaciones redundantes.
Cierre
Confirme la evidencia, finalice los enlaces a los registros de auditoría/quejas y archívelos para su revisión regulatoria.
Detección
Identificar problemas de desviaciones, quejas, auditorías, OOS/OOT. Clasifica automáticamente eventos y vincula registros de origen.
Investigación
Análisis de causa raíz con cronogramas, seguimiento de datos y evaluación de riesgos. Los patrones históricos guían las investigaciones.
Plan de acción
El sistema recomienda acciones relevantes, prioridad de riesgo y mejores prácticas comprobadas.
Implementación
Ejecutar acciones, adjuntar pruebas, actualizar desvíos vinculados, cambios y registros de quejas.
Inteligencia de eficacia de la IA
AI compara cada CAPA nuevo con CAPA abiertos de verificación de efectividad de naturaleza similar: señala superposiciones, recomienda consolidación y evita investigaciones redundantes.
Cierre
Confirme la evidencia, finalice los enlaces a los registros de auditoría/quejas y archívelos para su revisión regulatoria.
Software de sistema de gestión de calidad manual versus digital
Retorno de la inversión cuantificado al implementar el software de gestión de calidad farmacéutica basado en la nube AmpleLogic durante todo el ciclo de vida de la calidad
Ciclo de investigación de desviaciones
35-50% más rápidoTiempo de ciclo promedio de 45 a 90 días con investigación en papel, coordinación basada en correo electrónico y recopilación manual de evidencia en todos los departamentos.
Los flujos de trabajo automatizados con RCA asistido por IA, registros de calidad vinculados automáticamente y seguimiento de SLA configurable reducen el tiempo del ciclo a 15-30 días.
Cierre de CAPA y verificación de efectividad
40-60% más rápidoCiclos CAPA de 60 a 120 días con seguimiento manual, controles de eficacia omitidos, planes de acción aislados y sin recopilación sistemática de evidencia
Ciclo de vida de circuito cerrado con comprobaciones de eficacia automatizadas, seguimiento de hitos, requisitos de evidencia y acciones correctivas recomendadas por IA.
Preparación para auditorías y preparación para inspecciones
80% de esfuerzo ahorradoDe 2 a 4 semanas de recopilación manual de evidencia, referencias cruzadas entre sistemas y recopilación de documentación de último momento antes de cada auditoría.
Paquetes de evidencia listos para inspección generados bajo demanda: ensamblaje de pistas de auditoría con un solo clic, paneles de control de cumplimiento en tiempo real y análisis de brechas.
Ciclo de vida del control de cambios
Reducción del ciclo del 60%Evaluaciones de impacto de varias semanas en todos los departamentos con enrutamiento de aprobación manual, seguimiento de implementación desconectado y actualizaciones retrasadas de SOP
Predicción del impacto del cambio impulsada por IA, enrutamiento automatizado de múltiples partes interesadas, seguimiento de implementación basado en hitos y actualizaciones de SOP/capacitación activadas automáticamente
Sistema de gestión de calidad impulsado por IA
Aprovechar los agentes de IA y el aprendizaje automático para automatizar investigaciones, predecir riesgos y acelerar la toma de decisiones de calidad en su plataforma de gestión de calidad digital.
Inteligencia de eficacia CAPA
La IA monitorea continuamente los CAPA abiertos para verificar su efectividad y compara automáticamente cada CAPA nuevo de naturaleza similar, señalando posibles duplicados, recomendando consolidación o referencias cruzadas y sacando a la luz acciones correctivas existentes para evitar investigaciones redundantes.
Agentes de resumen de eventos de calidad
Agregue automáticamente datos de investigaciones, desviaciones y planes CAPA para generar resúmenes narrativos, lo que reduce el tiempo de documentación en un 60 %.
Análisis de causa raíz impulsado por IA
Compare patrones con datos históricos de CAPA y desviaciones para predecir causas fundamentales probables, recomendar acciones preventivas comprobadas y explicar los factores clave
Análisis predictivo de calidad
Los modelos de aprendizaje automático detectan señales de calidad emergentes, pronostican tendencias de desviación y priorizan áreas de alto riesgo antes de que se conviertan en problemas de cumplimiento.
Predicción inteligente del impacto del cambio
Analice datos de cambios históricos y patrones de desviación para predecir el impacto de los cambios en productos, procesos y presentaciones regulatorias antes de la implementación.
Optimización automatizada del flujo de trabajo
La IA aprende continuamente de los datos de ejecución de procesos para sugerir mejoras en el flujo de trabajo, identificar cuellos de botella y recomendar rutas de enrutamiento optimizadas para SLA.
Características de la plataforma eQMS
Capacidades de software del sistema de gestión de calidad de nivel empresarial: gestión CAPA, gestión de desviaciones, gestión de auditorías, software de gestión de no conformidades y calidad de proveedores con automatización del flujo de trabajo de calidad incorporada para el cumplimiento de las ciencias biológicas.
Verificación de eficacia en circuito cerrado
Flujos de trabajo de verificación integrados para CAPA, control de cambios, desviaciones y auditorías, con criterios de éxito predefinidos, protocolos de nueva prueba y recopilación de evidencia automatizada para la defensa regulatoria.
Soporte de decisiones basado en riesgos
Armonización de calidad en múltiples sitios
Paneles de calidad en tiempo real
Firma electrónica y seguimiento de auditoría
Motor de flujo de trabajo configurable de bajo código
Asistencia de investigación impulsada por IA
Revisión anual de la calidad del producto (APQR)
Ejecución de calidad móvil
Motor de escalamiento automatizado
Colaboración externa en tiempo real
Reúna a los equipos internos, CDMO, proveedores y socios en un único ecosistema de calidad para una resolución más rápida y una alineación global.
Acceso a proveedores y CDMO
Otorgue acceso controlado a socios externos para colaboración en tiempo real en investigaciones, hallazgos de auditorías y acciones correctivas de proveedores.
Coordinación de laboratorio por contrato
Comparta datos OOS/OOT, coordine investigaciones y gestione transferencias de métodos con laboratorios de pruebas contratados en un sistema unificado.
Preparación de la autoridad reguladora
Genere paquetes de evidencia listos para los inspectores con un solo clic: complete pistas de auditoría, registros de calidad vinculados y paneles de cumplimiento
Alineación de calidad en múltiples sitios
Estandarice los procesos de calidad en todos los sitios de fabricación globales con configuración centralizada, flujos de trabajo localizados e informes consolidados.
Centro de integración unificado de eQMS
Software QMS basado en la nube conectado perfectamente a todo su ecosistema empresarial para una trazabilidad de la calidad de extremo a extremo
Gestión de documentos (DMS)
Revisiones de SOP, distribución controlada de copias, gestión de versiones.
Gestión del aprendizaje (LMS)
Capacitación activada automáticamente sobre aprobaciones de control de cambios y actualizaciones de SOP
LIMAS
Incidentes de laboratorio, desviaciones, inicio automático OOS/OOT y extracción de datos
eBMR/MES
Activadores de retención de lotes, captura de desviaciones de producción, datos de proceso en tiempo real
Regulatoria (RIMS)
Coordinación del control de cambios, impacto del registro de productos, presentaciones regulatorias.
Validación de limpieza
Desviaciones, OOS/OOT del monitoreo del proceso de limpieza y pruebas de límites
libro de registro electrónico
Captura de desviaciones de eventos del cuaderno de bitácora, excursiones ambientales.
Seguridad / Farmacovigilancia
Vinculación de quejas con casos de seguridad, correlación de eventos adversos
ERP/Cadena de Suministro
Sincronización de datos de proveedores, genealogía de lotes, trazabilidad de materiales, gestión de reservas

Centro AmpleLogic eQMS
Ecosistema empresarial conectado
Sistema de gestión de calidad compatible con GxP
Sistema de gestión de calidad QMS compatible con FDA 21 CFR Parte 11, sistema de gestión de calidad ISO 13485 y software de gestión de calidad GMP con software integrado de preparación para auditorías, plataforma de preparación para inspecciones y gestión de cumplimiento farmacéutico para la gestión de calidad de la industria regulada
21 CFR Parte 11
Registros electrónicos y firmas.
Anexo 11 de la UE
Validación de sistemas computarizados
ICH Q9
Gestión de riesgos de calidad
HC Q10
Sistema de calidad farmacéutica
GAMP 5 / ISPE
Validación basada en riesgos
Norma ISO 9001 / 13485
Estándares de calidad y dispositivos médicos
MDR/IVDR de la UE
Regulación de dispositivos médicos
Principios ALCOA+
Marco de integridad de datos
Software de gestión de calidad para cada segmento de ciencias biológicas
Soluciones eQMS específicas de la industria: sistema de gestión de calidad farmacéutica, software QMS de biotecnología y software QMS de dispositivos médicos para cada fabricante regulado.
Farmacéutica
Software de gestión de calidad GMP de extremo a extremo para instalaciones de fabricación de medicamentos, producción de API e instalaciones de formulación: software de gestión de calidad diseñado específicamente para el sector farmacéutico.
Biotecnología
Software de gestión de calidad especializado para biotecnología, que respalda el desarrollo y la fabricación de productos biológicos, biosimilares y terapias avanzadas.
Dispositivos médicos
Software de gestión de calidad de dispositivos médicos: cumple con ISO 13485, EU MDR/IVDR para el diseño, la fabricación y la vigilancia poscomercialización de dispositivos.
Terapia genética y celular
Sistema de gestión de calidad de ciencias biológicas para ATMP y fabricación de terapias celulares/génicas con alineación regulatoria especializada.
CDMO / CMO
Sistema de gestión de calidad empresarial para fabricantes contratados con gestión de calidad multicliente y preparación para auditorías.
nutracéuticos
Software de gestión de calidad farmacéutica para la fabricación de suplementos dietéticos y nutracéuticos con cumplimiento de GMP.
AmpleLogic eQMS: software de gestión de calidad farmacéutica
Acelere la gestión del cumplimiento farmacéutico, las investigaciones, la verificación y la preparación para auditorías a lo largo de todo el ciclo de vida de la calidad con soluciones de SGC empresarial y software de cumplimiento de ciencias biológicas.
Sistema de gestión de calidad compatible con GxP con cobertura FDA, ICH Q10, ISO, EU MDR/IVDR y WHO GMP
Investigaciones y cierre de CAPA entre un 40 % y un 50 % más rápidos con capacidades del sistema de gestión de calidad impulsado por IA
Verificación demostrable de la eficacia de circuito cerrado en cada etapa del ciclo de vida del SGC
Recopilación de evidencia lista para auditoría en segundos (no días) para la gestión del cumplimiento farmacéutico
Primera implementación piloto con validación basada en riesgos (alineada con GAMP 5) en software QMS basado en la nube
Colaboración externa en tiempo real con CDMO, proveedores y socios a través de software de gestión de calidad de proveedores.
Alineación de calidad global en múltiples sitios y múltiples idiomas desde el primer día con el sistema de gestión de calidad empresarial
Datos de calidad unificados para revisiones anuales de calidad de productos (APQR) en una única plataforma digital de gestión de calidad
Premios de satisfacción del cliente y reconocimiento del software eQMS
Con la confianza de las principales organizaciones de ciencias biológicas de todo el mundo
#1 más fácil de usar
Sistema de gestión de la calidad médico
Máxima satisfacción del cliente
CSAT líder en la industria
Fortalezas de la plataforma
Personalización de arrastrar y soltar
89 insignias G2
Líder multicategoría
"El sistema Amplelogic QMS tiene todos los módulos necesarios relacionados con la calidad y todas las desviaciones, controles de cambios y CAPA se mantienen y rastrean de manera efectiva. Todos los módulos son súper fáciles de usar."
Kandikattu K.
Profesional de calidad
"Se integra perfectamente con nuestras otras herramientas. Han atendido la mayoría de nuestras solicitudes de personalización únicas, lo que lo hace muy fácil de usar."
Gerente de Aseguramiento de Calidad
Farmacéutica del mercado medio
"El sistema está compilado de conformidad con 21 CFR Parte 11 y el Anexo 11 de la UE. El apoyo del equipo durante la configuración inicial fue realmente útil e hizo que la transición fuera fluida."
Krisna C.
Líder de Cumplimiento
¿Listo para transformar su sistema de gestión de calidad?
Únase a las principales empresas farmacéuticas, biotecnológicas y de dispositivos médicos que aceleran el cumplimiento del mejor sistema electrónico de gestión de calidad (eQMS): una plataforma QMS digital basada en la nube y una plataforma SaaS QMS para la empresa moderna.
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.