Empresarial con IA Soluciones para Cada Flujo de Trabajo Farmacéutico
Suite integral de soluciones de software validadas para organizaciones farmacéuticas, biotecnológicas y de ciencias de la vida.
aPaaS de Bajo Código para Ciencias de la Vida — Arquitectura de Integración Unificada
Los módulos de AmpleLogic no operan de forma aislada. Cada solución está interconectada — compartiendo datos, activando flujos de trabajo y manteniendo una única fuente de verdad en las funciones de Calidad, Fabricación y Laboratorio QC.
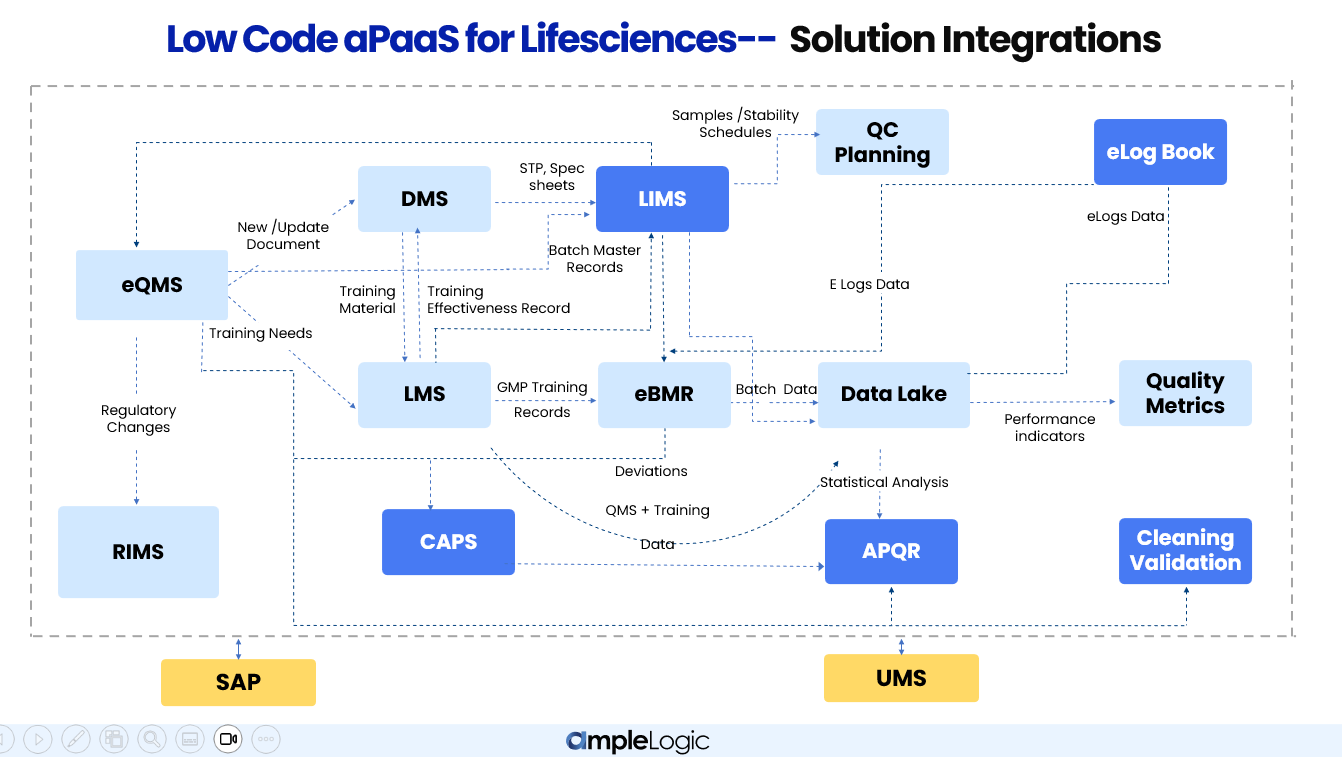
Cómo los módulos de AmpleLogic se integran entre las funciones de Calidad, Fabricación y Laboratorio QC en empresas farmacéuticas
Data Lake Unificado
Todos los módulos alimentan un Data Lake centralizado, habilitando indicadores de rendimiento en tiempo real, métricas de calidad y análisis interfuncionales sin consolidación manual de datos.
Cascadas de Flujo de Trabajo Automatizadas
Un solo evento — como una desviación en fabricación — activa automáticamente CAPA en eQMS, la revisión de documentos en DMS, el reentrenamiento en LMS y la evaluación de impacto en APQR.
Flujo de Datos Bidireccional
Los datos fluyen en ambas direcciones entre módulos. Por ejemplo, LMS envía registros de efectividad de capacitación de vuelta a eQMS, y LIMS devuelve resultados analíticos a eBMR para la liberación de lotes.
Cómo Funcionan las Integraciones entre Funciones
Gestión de Calidad
El ecosistema de Gestión de Calidad garantiza que cada desviación, CAPA, control de cambios y hallazgo de auditoría se rastree de extremo a extremo. eQMS ocupa el centro — activando flujos de trabajo de documentos en DMS, asignaciones de capacitación en LMS y alimentando datos estadísticos en APQR para las revisiones anuales de calidad del producto.
Documento Nuevo / Actualizado
Cuando se genera una desviación o control de cambios en eQMS, DMS inicia automáticamente un flujo de revisión de SOP, asegurando que los documentos estén actualizados con cada evento de calidad.
Necesidades de Capacitación
Los SOPs nuevos o revisados activan asignaciones de capacitación automáticas en LMS. Los registros de efectividad de capacitación regresan a eQMS para cerrar el ciclo de calidad.
Análisis Estadístico
Los datos de lotes, desviaciones, registros CAPA y parámetros de proceso se agregan en el Data Lake y se alimentan en APQR para las revisiones anuales de calidad del producto.
Datos de QMS + Capacitación
Las desviaciones de calibración y los registros de mantenimiento preventivo de CAPS fluyen hacia APQR, proporcionando una imagen completa del impacto de equipos e instrumentos en la calidad del producto.
Manténgase a la Vanguardia en Ciencias de la Vida
Reciba las últimas actualizaciones de productos, noticias de cumplimiento normativo e información del sector directamente en su bandeja de entrada.