Gérez chaque événement qualité dans un eQMS intégré
AmpleLogic propose une plateforme logicielle QMS pharmaceutique basée sur le cloud et propulsée par l'IA, conçue pour une conformité de niveau entreprise. Notre plateforme QMS numérique unifie la gestion des CAPA, la gestion des déviations, le contrôle des changements, les audits et la qualité fournisseurs en une seule solution logicielle de gestion des événements qualité conforme GxP — approuvée par les entreprises pharmaceutiques, biotechnologiques et de dispositifs médicaux du monde entier.
11+
Modules QMS intégrés
100%
Conforme 21 CFR Part 11
50%
Clôture CAPA plus rapide
300+
Implémentations mondiales
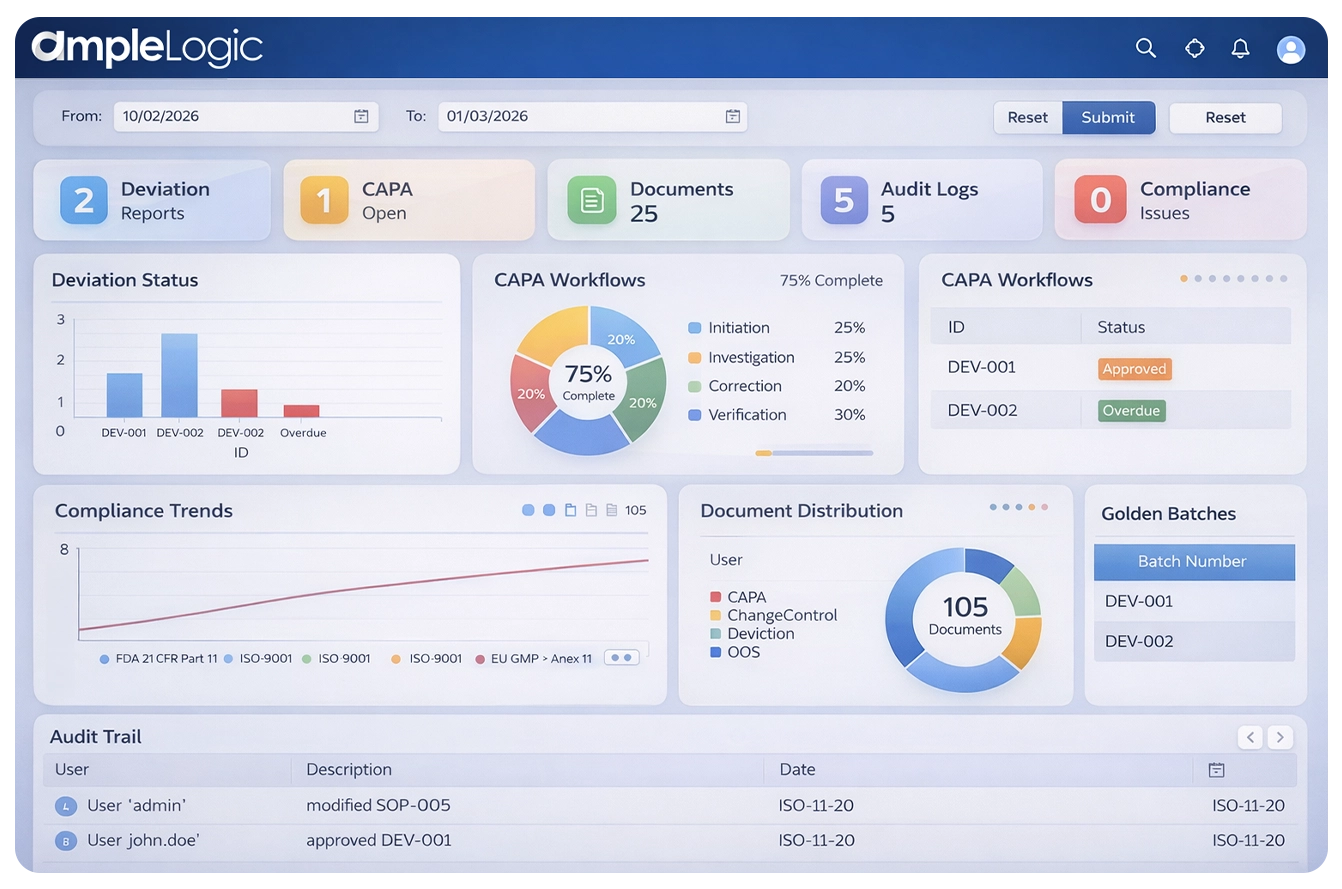
Pourquoi les logiciels de gestion de la qualité traditionnels sont insuffisants
Comment les processus manuels fragmentés dans les logiciels de gestion de la conformité pharmaceutique et les systèmes de gestion de la qualité GMP traditionnels entraînent des retards dans les événements qualité, des lacunes dans les logiciels de gestion des non-conformités et des coûts qualité plus élevés
Non-conformité réglementaire
Risque élevé de pénalités dû aux erreurs de documentation manuelle, aux pistes d'audit manquantes et à la traçabilité limitée — des problèmes qu'un logiciel de gestion de la qualité conforme GxP élimine
Systèmes qualité cloisonnés
Des modules QMS autonomes avec des intégrations faibles entraînent des investigations retardées, une saisie de données redondante et des clôtures de CAPA prolongées au sein du système de gestion de la qualité d'entreprise
Pas d'analyse en temps réel
L'absence de tableaux de bord pour la gestion des déviations, les CAPA, le contrôle des changements et les OOS limite la prise de décision proactive et la visibilité sur les risques sans plateforme de gestion de la qualité numérique
Cycles d'investigation lents
Les investigations sur papier ou par e-mail prennent 2 à 4 fois plus de temps que les workflows numériques dans les logiciels modernes de gestion de la qualité pharmaceutique, retardant la libération des lots
Collaboration externe limitée
Aucun accès partenaire en temps réel pour la gestion de la qualité fournisseurs, les investigations CDMO ou la coordination des laboratoires sous contrat — une lacune que le logiciel QMS basé sur le cloud résout
Lacunes d'alignement mondial
Les opérations multi-sites peinent avec des processus incohérents, des données fragmentées et l'impossibilité de consolider les indicateurs qualité sans système de gestion de la qualité d'entreprise

Le coût du maintien des processus manuels
Système de gestion de la qualité d'entreprise — Avantages
Plateforme QMS SaaS basée sur le cloud avec contrôle du cycle de vie, conformité réglementaire, automatisation des workflows qualité et plateforme qualité d'entreprise validée pour la pharma et la biotech
Efficacité en boucle fermée
Vérification intégrée pour les workflows de gestion des CAPA, du contrôle des changements, des déviations et des logiciels de gestion des audits
Traçabilité véritablement de bout en bout
Liaison en un clic entre la gestion des déviations, les CAPA, les changements, les réclamations, les OOS/OOT et les enregistrements d'audit dans un QMS unifié
Prêt pour l'audit à tout moment
Assemblage automatisé des preuves, pistes d'audit immuables et tableaux de bord d'inspection pour les opérations QMS conformes FDA 21 CFR Part 11
Aide à la décision basée sur les risques
Priorisez les actions grâce à la notation des risques et aux données qualité historiques au sein du système de gestion de la qualité d'entreprise
Intelligence qualité assistée par l'IA
RCA plus rapide, détection des anomalies et vérification de l'efficacité grâce aux capacités du système de gestion de la qualité propulsé par l'IA
Escalade automatisée et rappels
Rappels pilotés par les risques et les délais avec escalade automatique dans tout le logiciel de gestion de la conformité pharmaceutique
Pourquoi AmpleLogic — Logiciel QMS cloud conçu pour les sciences de la vie
Logiciel de gestion de la qualité pharmaceutique de référence avec un ROI prouvé et une défendabilité réglementaire
Le coût de la qualité manuelle
Les processus qualité manuels augmentent les erreurs, les délais et les coûts opérationnels — le logiciel QMS cloud élimine ces inefficacités
Moteur de recommandations intelligent
Recommandations intelligentes et basées sur les données pour accélérer la résolution des problèmes sur votre plateforme de gestion de la qualité numérique
Avantage aPaaS basé sur le cloud
Le logiciel QMS cloud à faible code accélère le déploiement, la personnalisation et le déploiement multi-sites pour la gestion de la qualité pharmaceutique
Conformité GxP et validation
Le système de gestion de la qualité conforme GxP avec les contrôles intégrés FDA 21 CFR Part 11 garantit que les processus respectent les normes réglementaires et passent les audits
Indicateurs ROI quantifiables
Mesure les gains d'efficacité et les économies de coûts résultant du déploiement du logiciel de système de gestion de la qualité d'entreprise dans les opérations
Intégrations transparentes
Se connecte sans effort avec LIMS, eBMR, DMS, ERP et les logiciels de système de gestion de la qualité existants dans votre stack technologique
CAPA, déviation, audit et gestion de la qualité fournisseurs
Explorez chaque module de notre logiciel de système de gestion de la qualité — logiciel de gestion des CAPA, logiciel de gestion des déviations, logiciel de gestion du contrôle des changements, logiciel de gestion des audits, logiciel de gestion des réclamations, logiciel de gestion des risques qualité, qualité fournisseurs et gestion des non-conformités
Gestion des déviations
Système de gestion des événements qualité pharmaceutique
Gestion complète du cycle de vie des déviations pour la fabrication pharmaceutique — de la détection à la clôture avec une traçabilité complète, une classification basée sur les risques et une défendabilité GMP.
Gestion des CAPA
Logiciel de gestion des CAPA pharmaceutiques
Cycle de vie des actions correctives et préventives en boucle fermée — de l'initiation à l'investigation des causes profondes, l'automatisation des workflows et le suivi de l'efficacité avec conformité FDA et GxP.
Contrôle des changements
Planifier, évaluer, mettre en œuvre, vérifier
Gérez les changements planifiés et non planifiés dans les processus, les équipements, les matériaux et les systèmes avec une analyse d'impact structurée, une approbation multi-parties prenantes et une revue post-mise en œuvre.
Gestion des audits
Logiciel de gestion des audits pour les systèmes de qualité pharmaceutique
Gestion des audits internes, externes et fournisseurs avec planification automatisée, programmation, intégration des constats vers les CAPA et tableaux de bord de préparation aux inspections réglementaires.
Gestion des réclamations
Gestion des réclamations propulsée par l'IA pour les systèmes de qualité pharmaceutique
Cycle de vie complet des réclamations depuis la réception multicanal jusqu'à l'investigation, le signalement réglementaire et le suivi de la résolution avec une traçabilité complète vers les événements qualité associés.
Gestion des OOS
Logiciel de gestion des OOS pour les investigations hors spécification
Workflows d'investigation structurés Phase I et Phase II hors spécification alignés sur les recommandations FDA avec rigueur scientifique et défendabilité réglementaire complète.
Gestion des OOT
Analyse hors tendance
Surveillance statistique des tendances et workflows d'investigation déclenchés par des alertes pour détecter les glissements qualité progressifs avant qu'ils ne deviennent des événements OOS, permettant une gestion qualité proactive.
Gestion des incidents laboratoire
Logiciel de gestion des incidents laboratoire pour les laboratoires de contrôle qualité pharmaceutique
Suivez et investiguez les dysfonctionnements d'instruments, la contamination des échantillons, les excursions environnementales et les erreurs d'analystes avec des workflows d'actions correctives structurés et la conformité GxP.
Gestion des risques qualité
Système de gestion des risques qualité piloté par l'IA
Gestion des risques alignée sur ICH Q9 avec FMEA, analyse en arête de poisson, notation des risques, identification des risques par l'IA et tableaux de bord des risques d'entreprise pour des décisions qualité proactives.
Qualification des fournisseurs
Logiciel de gestion de la qualité fournisseurs et de qualification des fournisseurs
Gestion complète du cycle de vie des fournisseurs — de la qualification initiale au suivi continu des performances, la planification d'audits basée sur les risques et la re-qualification périodique.
Gestion des rappels produits
Initier, exécuter, signaler, clôturer
Initiation et exécution rapides des rappels avec traçabilité au niveau des lots, gestion des notifications réglementaires, suivi de la communication client et évaluation de l'efficacité post-rappel.
Cycle de vie CAPA : vérifications d'efficacité
Contrôle du cycle de vie, capture des preuves et automatisation pour la défendabilité réglementaire
Détection
Identifier les problèmes à partir des déviations, des réclamations, des audits, des OOS/OOT. Classifie automatiquement les événements et lie les enregistrements sources.
Investigation
Analyse des causes profondes avec chronologies, traces de données et évaluation des risques. Les schémas historiques guident les investigations.
Plan d'action
Le système recommande les actions pertinentes, la priorité des risques et les meilleures pratiques éprouvées.
Mise en œuvre
Exécuter les actions, joindre les preuves, mettre à jour les déviations liées, les changements et les enregistrements de réclamations.
Intelligence d'efficacité par l'IA
L'IA compare chaque nouvelle CAPA avec les CAPA de vérification d'efficacité ouvertes de nature similaire — signalant les chevauchements, recommandant la consolidation et évitant les investigations redondantes.
Clôture
Confirmer les preuves, finaliser les liens vers les enregistrements d'audit et de réclamations, et archiver pour la revue réglementaire.
Détection
Identifier les problèmes à partir des déviations, des réclamations, des audits, des OOS/OOT. Classifie automatiquement les événements et lie les enregistrements sources.
Investigation
Analyse des causes profondes avec chronologies, traces de données et évaluation des risques. Les schémas historiques guident les investigations.
Plan d'action
Le système recommande les actions pertinentes, la priorité des risques et les meilleures pratiques éprouvées.
Mise en œuvre
Exécuter les actions, joindre les preuves, mettre à jour les déviations liées, les changements et les enregistrements de réclamations.
Intelligence d'efficacité par l'IA
L'IA compare chaque nouvelle CAPA avec les CAPA de vérification d'efficacité ouvertes de nature similaire — signalant les chevauchements, recommandant la consolidation et évitant les investigations redondantes.
Clôture
Confirmer les preuves, finaliser les liens vers les enregistrements d'audit et de réclamations, et archiver pour la revue réglementaire.
Logiciel de système de gestion de la qualité manuel vs. numérique
ROI quantifié du déploiement du logiciel de gestion de la qualité pharmaceutique basé sur le cloud AmpleLogic sur l'ensemble du cycle de vie qualité
Cycle d'investigation des déviations
35 à 50 % plus rapideDélai moyen de 45 à 90 jours avec des investigations sur papier, une coordination par e-mail et un assemblage manuel des preuves entre les services
Les workflows automatisés avec RCA assisté par l'IA, les enregistrements qualité liés automatiquement et le suivi SLA configurable réduisent le délai à 15-30 jours
Clôture des CAPA et vérification de l'efficacité
40 à 60 % plus rapideCycles CAPA de 60 à 120 jours avec suivi manuel, vérifications d'efficacité manquées, plans d'action cloisonnés et aucune collecte systématique de preuves
Cycle de vie en boucle fermée avec vérifications d'efficacité automatisées, suivi des jalons, exigences en matière de preuves et actions correctives recommandées par l'IA
Préparation aux audits et état de préparation aux inspections
80 % d'effort économisé2 à 4 semaines de compilation manuelle des preuves, de recoupement entre systèmes et d'assemblage de documentation de dernière minute avant chaque audit
Dossiers de preuves prêts pour l'inspection générés à la demande — assemblage de la piste d'audit en un clic, tableaux de bord de conformité en temps réel et analyse des écarts
Cycle de vie du contrôle des changements
60 % de réduction du cycleÉvaluations d'impact multi-semaines entre les services avec acheminement d'approbation manuel, suivi de mise en œuvre déconnecté et mises à jour SOP retardées
Prédiction d'impact des changements par l'IA, acheminement automatisé multi-parties prenantes, suivi de mise en œuvre basé sur des jalons et mises à jour SOP/formation déclenchées automatiquement
Système de gestion de la qualité propulsé par l'IA
Tirer parti des agents IA et du machine learning pour automatiser les investigations, prédire les risques et accélérer la prise de décision qualité sur l'ensemble de votre plateforme de gestion de la qualité numérique
Intelligence d'efficacité des CAPA
L'IA surveille en permanence les CAPA de vérification d'efficacité ouvertes et compare automatiquement chaque nouvelle CAPA de nature similaire — signalant les doublons potentiels, recommandant la consolidation ou le recoupement, et faisant remonter les actions correctives existantes pour éviter les investigations redondantes
Agents de synthèse des événements qualité
Agrégez automatiquement les données des investigations, des déviations et des plans CAPA pour générer des résumés narratifs — réduisant le temps de documentation de 60 %
Analyse des causes profondes propulsée par l'IA
Correspondance de modèles avec les données historiques CAPA et de déviations pour prédire les causes profondes probables, recommander des actions préventives éprouvées et expliquer les facteurs clés
Analyse qualité prédictive
Les modèles de machine learning détectent les signaux qualité émergents, prévoient les tendances des déviations et priorisent les zones à haut risque avant qu'elles ne deviennent des problèmes de conformité
Prédiction intelligente de l'impact des changements
Analyser les données historiques des changements et les schémas de déviations pour prédire l'impact des changements sur les produits, les processus et les dossiers réglementaires avant la mise en œuvre
Optimisation automatisée des workflows
L'IA apprend continuellement à partir des données d'exécution des processus pour suggérer des améliorations de workflow, identifier les goulots d'étranglement et recommander des chemins de routage optimisés selon les SLA
Fonctionnalités de la plateforme eQMS
Capacités logicielles de système de gestion de la qualité de niveau entreprise — gestion des CAPA, gestion des déviations, gestion des audits, logiciel de gestion des non-conformités et qualité fournisseurs avec automatisation intégrée des workflows qualité pour la conformité dans les sciences de la vie
Vérification de l'efficacité en boucle fermée
Workflows de vérification intégrés pour CAPA, contrôle des changements, déviations et audits — avec des critères de succès prédéfinis, des protocoles de re-test et un assemblage automatisé des preuves pour la défendabilité réglementaire.
Aide à la décision basée sur les risques
Harmonisation qualité multi-sites
Tableaux de bord qualité en temps réel
Signature électronique et piste d'audit
Moteur de workflow à faible code configurable
Assistance à l'investigation propulsée par l'IA
Revue annuelle de la qualité des produits (APQR)
Exécution qualité sur mobile
Moteur d'escalade automatisé
Collaboration externe en temps réel
Réunissez les équipes internes, les CDMO, les fournisseurs et les partenaires dans un seul écosystème qualité pour une résolution plus rapide et un alignement mondial
Accès fournisseurs et CDMO
Accordez un accès contrôlé aux partenaires externes pour une collaboration en temps réel sur les investigations, les constats d'audit et les actions correctives fournisseurs
Coordination des laboratoires sous contrat
Partagez les données OOS/OOT, coordonnez les investigations et gérez les transferts de méthodes avec les laboratoires de test sous contrat dans un système unifié
Préparation aux autorités réglementaires
Générez en un clic des dossiers de preuves prêts pour les inspecteurs — pistes d'audit complètes, enregistrements qualité liés et tableaux de bord de conformité
Alignement qualité multi-sites
Standardisez les processus qualité sur les sites de fabrication mondiaux avec une configuration centralisée, des workflows localisés et des rapports consolidés
Hub d'intégration eQMS unifié
Logiciel QMS basé sur le cloud connecté de manière transparente à l'ensemble de votre écosystème d'entreprise pour une traçabilité qualité de bout en bout
Gestion documentaire (DMS)
Révisions SOP, distribution des copies contrôlées, gestion des versions
Gestion de la formation (LMS)
Formation déclenchée automatiquement lors des approbations de contrôle des changements et des mises à jour SOP
LIMS
Incidents laboratoire, déviations, initiation automatique OOS/OOT et extraction de données
eBMR / MES
Déclencheurs de blocage de lots, capture des déviations de production, données de processus en temps réel
Réglementaire (RIMS)
Coordination du contrôle des changements, impact sur l'enregistrement des produits, soumissions réglementaires
Validation du nettoyage
Déviations, OOS/OOT issus de la surveillance des processus de nettoyage et des tests de limites
eLogbook
Capture des déviations issues des événements de logbook, excursions environnementales
Sécurité / Pharmacovigilance
Liaison réclamation-cas de sécurité, corrélation des événements indésirables
ERP / Chaîne d'approvisionnement
Synchronisation des données fournisseurs, généalogie des lots, traçabilité des matières, gestion des blocages

Hub AmpleLogic eQMS
Écosystème d'entreprise connecté
Système de gestion de la qualité conforme GxP
QMS conforme FDA 21 CFR Part 11, système de gestion de la qualité ISO 13485 et logiciel de gestion de la qualité GMP avec logiciel de préparation aux audits intégré, plateforme de préparation aux inspections et gestion de la conformité pharmaceutique pour la gestion de la qualité dans les industries réglementées
21 CFR Part 11
Enregistrements et signatures électroniques
EU Annex 11
Validation des systèmes informatisés
ICH Q9
Gestion des risques qualité
ICH Q10
Système de qualité pharmaceutique
GAMP 5 / ISPE
Validation basée sur les risques
ISO 9001 / 13485
Normes qualité et dispositifs médicaux
EU MDR / IVDR
Réglementation des dispositifs médicaux
ALCOA+ Principles
Cadre d'intégrité des données
Logiciel de gestion de la qualité pour chaque segment des sciences de la vie
Solutions eQMS spécifiques aux industries — système de gestion de la qualité pharmaceutique, logiciel QMS biotech et logiciel QMS dispositifs médicaux pour chaque fabricant réglementé
Pharmaceutique
Logiciel de gestion de la qualité GMP de bout en bout pour la fabrication de médicaments, la production d'API et les sites de formulation — logiciel de gestion de la qualité conçu spécifiquement pour la pharma.
Biotechnologie
Logiciel de gestion de la qualité spécialisé pour la biotech — supportant le développement et la fabrication de biologiques, de biosimilaires et de thérapies avancées.
Dispositifs médicaux
Logiciel de gestion de la qualité pour dispositifs médicaux — conforme ISO 13485, EU MDR/IVDR pour la conception, la fabrication et la surveillance post-commercialisation des dispositifs.
Thérapie génique et cellulaire
Système de gestion de la qualité pour les sciences de la vie destiné à la fabrication de produits ATMP et de thérapies cellulaires/géniques avec un alignement réglementaire spécialisé.
CDMO / CMO
Système de gestion de la qualité d'entreprise pour les fabricants sous contrat avec gestion de la qualité multi-clients et préparation aux audits.
Nutraceutiques
Logiciel de gestion de la qualité pharmaceutique pour la fabrication de compléments alimentaires et de nutraceutiques avec conformité GMP.
AmpleLogic eQMS — Logiciel de gestion de la qualité pharmaceutique
Accélérez la gestion de la conformité pharmaceutique, les investigations, la vérification et la préparation aux audits sur l'ensemble du cycle de vie qualité avec des solutions QMS d'entreprise et des logiciels de conformité pour les sciences de la vie
Système de gestion de la qualité conforme GxP avec couverture FDA, ICH Q10, ISO, EU MDR/IVDR et WHO GMP
Investigations et clôture des CAPA 40 à 50 % plus rapides grâce aux capacités du système de gestion de la qualité propulsé par l'IA
Vérification de l'efficacité en boucle fermée démontrable à chaque étape du cycle de vie QMS
Assemblage des preuves prêtes pour l'audit en quelques secondes — et non en jours — pour la gestion de la conformité pharmaceutique
Déploiement en mode pilote d'abord avec validation basée sur les risques (alignée GAMP 5) sur le logiciel QMS basé sur le cloud
Collaboration externe en temps réel avec les CDMO, les fournisseurs et les partenaires via le logiciel de gestion de la qualité fournisseurs
Alignement qualité mondial multi-sites et multilingue dès le premier jour avec le système de gestion de la qualité d'entreprise
Données qualité unifiées pour les Revues Annuelles de la Qualité des Produits (APQR) sur une seule plateforme de gestion de la qualité numérique
Récompenses de reconnaissance et de satisfaction client du logiciel eQMS
Approuvé par les principales organisations des sciences de la vie dans le monde entier
#1 Le plus facile à utiliser
QMS médical
Satisfaction client la plus élevée
CSAT leader du secteur
Points forts de la plateforme
Personnalisation par glisser-déposer
89 badges G2
Leader multi-catégories
"Le système QMS d'Amplelogic dispose de tous les modules liés à la qualité requis, et toutes les déviations, contrôles de changements et CAPA sont efficacement maintenus et suivis. Tous les modules sont très faciles à utiliser."
Kandikattu K.
Professionnel de la qualité
"Il s'intègre de manière transparente avec nos autres outils. Ils ont répondu à la plupart de nos demandes de personnalisation spécifiques, le rendant très convivial pour notre utilisation."
Responsable assurance qualité
Pharma marché intermédiaire
"Le système est conforme aux réglementations 21 CFR Part 11 et EU Annex 11. Le soutien de l'équipe lors de la configuration initiale était vraiment utile et a facilité la transition."
Krishna C.
Responsable conformité
Prêt à transformer votre système de gestion de la qualité ?
Rejoignez les principales entreprises pharmaceutiques, biotechnologiques et de dispositifs médicaux qui accélèrent leur conformité avec le meilleur système de gestion électronique de la qualité (eQMS) — une plateforme QMS numérique basée sur le cloud et une plateforme QMS SaaS pour l'entreprise moderne.
Gardez une longueur d'avance dans les sciences de la vie
Recevez les dernières mises à jour produit, actualités de conformité et analyses du secteur directement dans votre boîte mail.