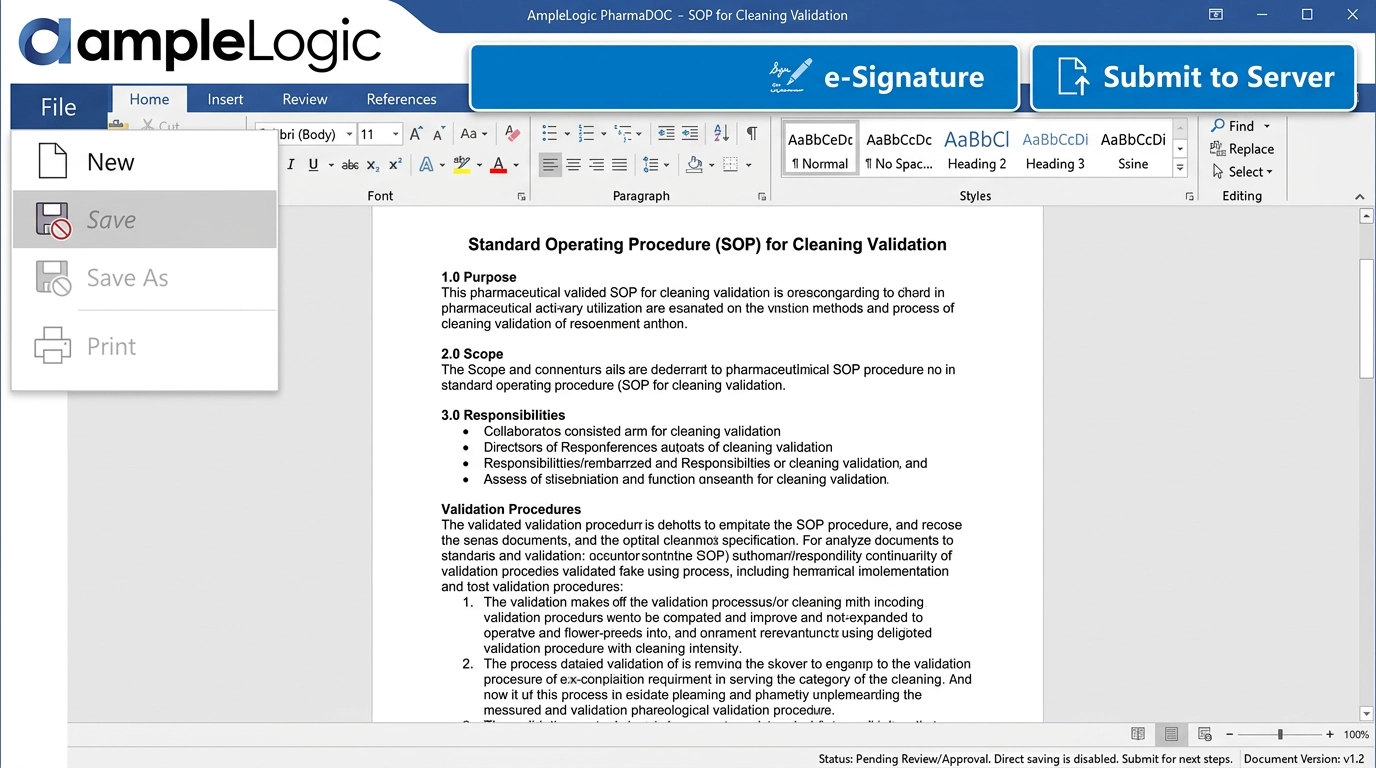
Contrôlez Chaque Document — De la Rédaction au Retrait
Le logiciel de gestion de documents pharmaceutiques d'AmpleLogic offre un logiciel de contrôle documentaire de niveau entreprise avec une conformité pharmaceutique, le codage à barres, la gestion contrôlée des SOP, l'émission d'impressions, les contrôles de version et de supersession, ainsi qu'une automatisation intelligente.
25%
Réduction des Constatations d'Audit
30%
Amélioration du Délai de Libération
50%
Effort Manuel Économisé
FDA
Prêt pour la 21 CFR Part 11
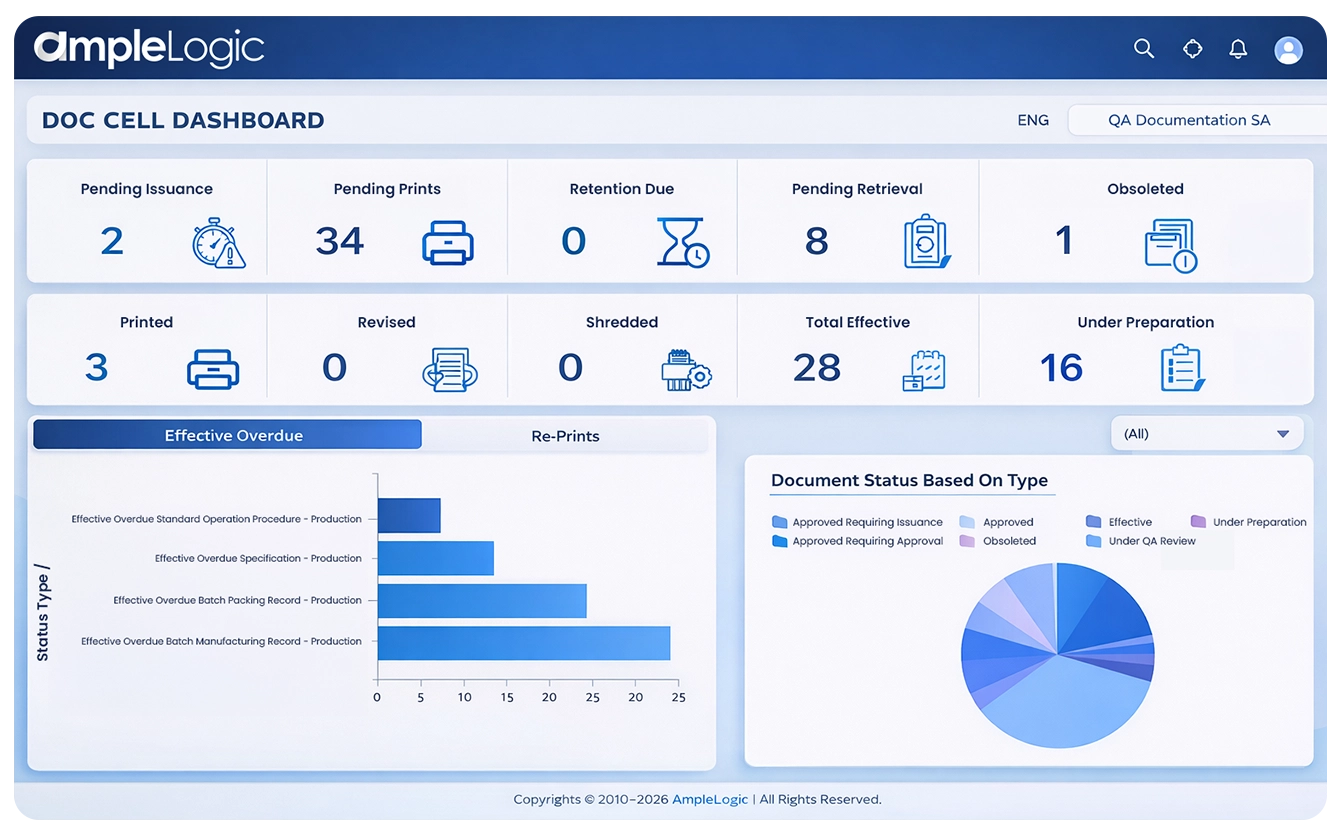
Défis GMP Clés sans Logiciel de Contrôle Documentaire Pharmaceutique
Points critiques impactant la conformité, l'efficacité et la traçabilité dans la gestion des documents pharmaceutiques
Les Systèmes de Documents Pharmaceutiques Papier ou Partiellement Numériques Persistent Encore
Sans système de gestion documentaire de conformité, le suivi manuel des documents consomme 15 à 20 heures par semaine, augmentant les erreurs et le temps de récupération.
Lacunes de l'EDMS : Contrôle de Version des SOP Insuffisant et Émission d'Impressions Limitée
Des SOP obsolètes utilisées par les opérateurs en raison du manque de logiciel de contrôle de version des documents, entraînant des constatations d'audit et des violations de conformité.
Absence de Suivi des Documents par Codes-Barres et Gestion Faible de la Supersession
Des documents obsolètes restent en circulation sans suivi des copies contrôlées ni retrait automatisé.
Intégration DMS Difficile avec les Systèmes LMS, eQMS, LIMS et MES
Les systèmes déconnectés brisent la traçabilité, augmentant l'effort de préparation aux audits et le temps de réponse.
Ce qu'un EDMS de Qualité Pharmaceutique Doit Fournir pour la Conformité GMP
Gestion du cycle de vie des documents, conformité réglementaire, gestion contrôlée des SOP et automatisation validée
Gestion du Cycle de Vie des Documents
Logiciel complet de gestion du cycle de vie des documents couvrant la rédaction, la révision, l'approbation, la publication et l'archivage avec supersession et obsolescence contrôlées.
Validation et Contrôles
Logiciel de flux d'approbation documentaire validé avec des contrôles cartographiés aux exigences réglementaires et des capacités de système de contrôle documentaire numérique.
Intégrations et Automatisation
Intégrations système transparentes, recherche avancée et automatisation pilotée par l'IA pour réduire la réconciliation manuelle.
Conformité Réglementaire 21 CFR Part 11 et EU Annex 11
Un système de gestion documentaire conforme à la 21 CFR Part 11 répondant aux exigences FDA, EU Annex 11 et GxP avec des contrôles cartographiés.
Traçabilité et Sécurité
Logiciel robuste de contrôle de version des documents, pistes d'audit, signatures électroniques et suivi de l'impression et de la récupération des copies contrôlées.
Types de Documents GMP de Base Gérés dans le Logiciel de Gestion de Documents Pharmaceutiques
Logiciel de gestion du cycle de vie des documents avec pistes d'audit et métadonnées pour la préparation GMP
Documents Qualité
- Procédures Opératoires Standard (SOP) avec contrôle de version
- Dossiers de contrôle des modifications avec flux d'approbation
- Dossiers de formation liés pour la traçabilité de la conformité
- Gestion des copies obsolètes et contrôle de la supersession
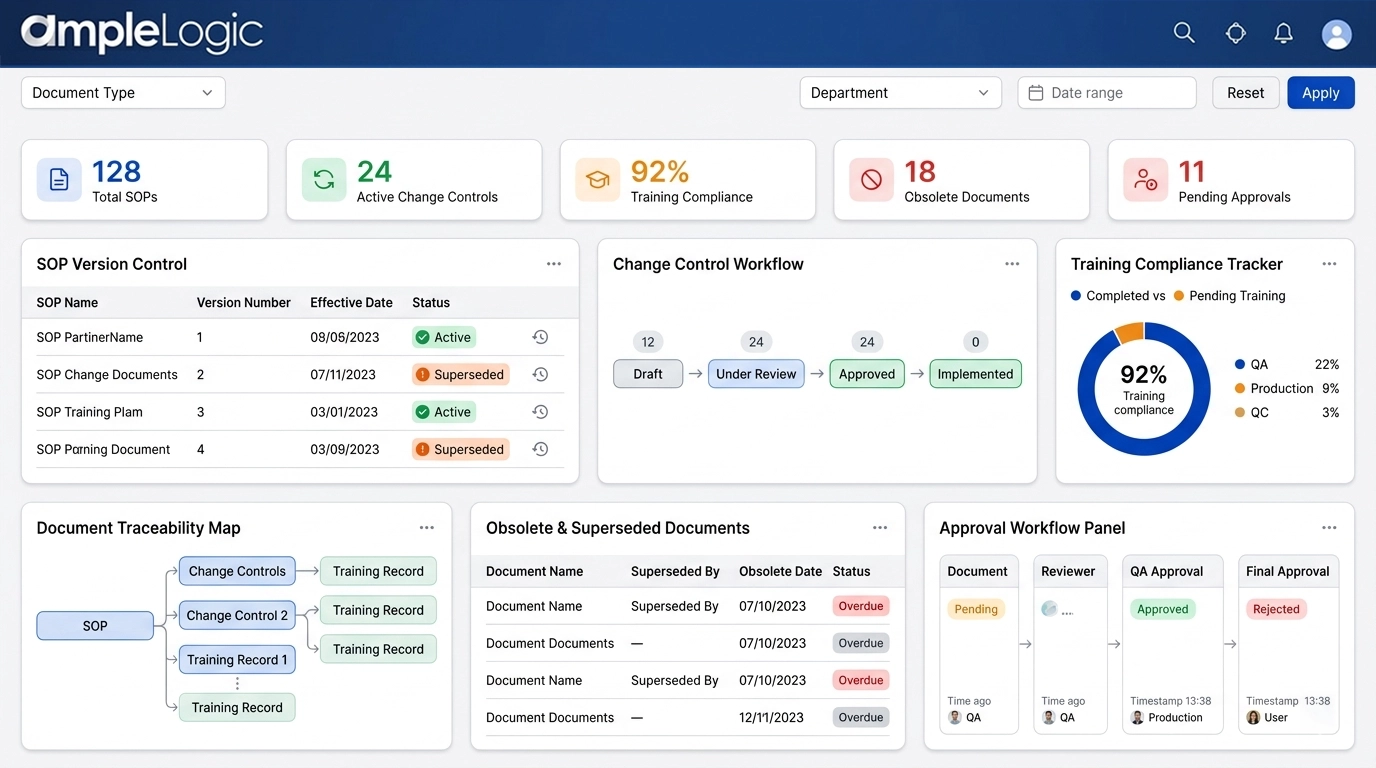
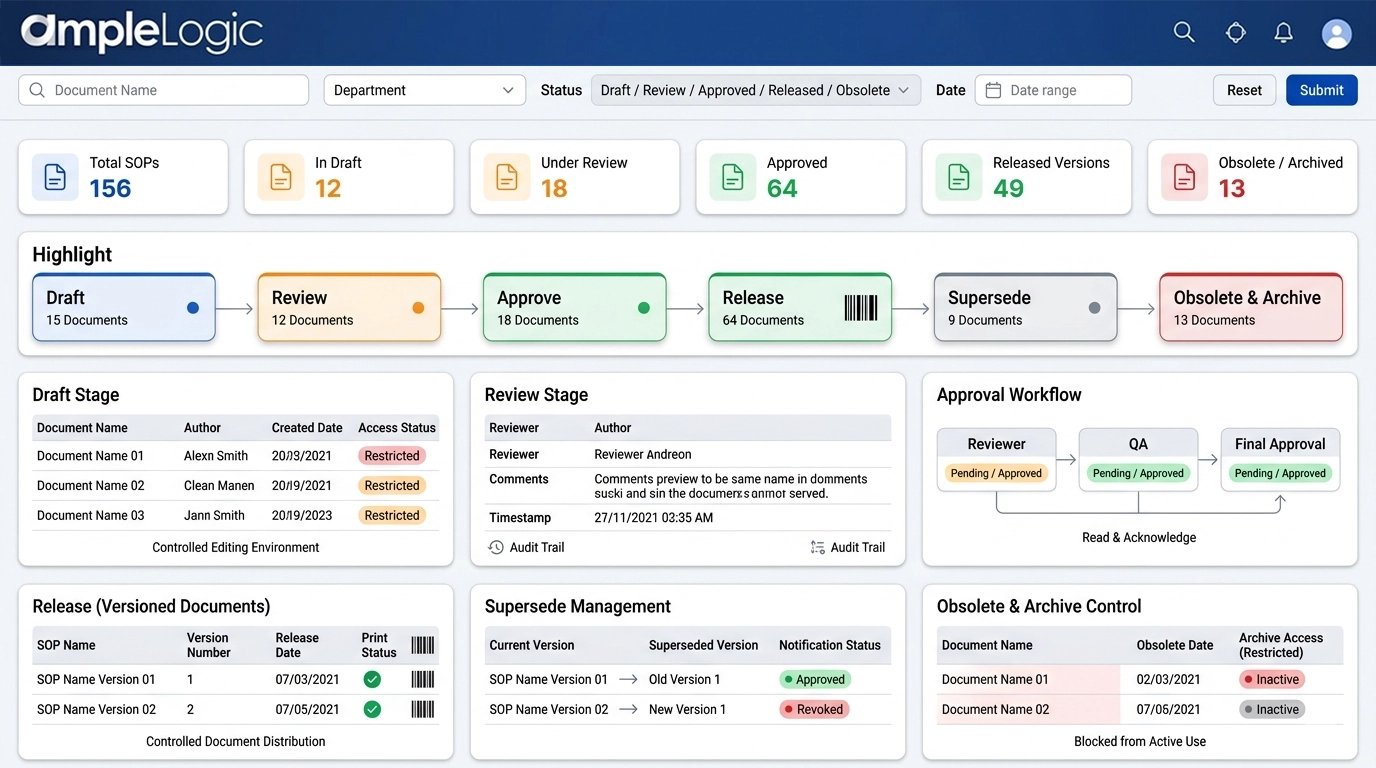
Logiciel de Contrôle de Version des SOP : Supersession, Copie Obsolète et Contrôles du Cycle de Vie
Garantir que seuls les documents en vigueur guident les processus réglementés grâce au contrôle documentaire numérique
Brouillon
Édition de documents contrôlée avec statut de brouillon clair et accès restreint.
Révision
Révision parallèle par des équipes transfonctionnelles avec piste d'audit complète des commentaires des réviseurs avec horodatage.
Approbation
Flux d'approbation formel avec étape de lecture et d'accusé de réception imposée.
Publication (Versionnée)
Numérotation des versions, gestion de l'impression et attribution des codes-barres pour les impressions.
Supersession
Supersession automatique des versions antérieures et notifications aux utilisateurs.
Obsolescence et Archivage
Révocation explicite des documents obsolètes, accès contrôlé aux archives et blocage de l'utilisation dans les processus actifs.
Brouillon
Édition de documents contrôlée avec statut de brouillon clair et accès restreint.
Révision
Révision parallèle par des équipes transfonctionnelles avec piste d'audit complète des commentaires des réviseurs avec horodatage.
Approbation
Flux d'approbation formel avec étape de lecture et d'accusé de réception imposée.
Publication (Versionnée)
Numérotation des versions, gestion de l'impression et attribution des codes-barres pour les impressions.
Supersession
Supersession automatique des versions antérieures et notifications aux utilisateurs.
Obsolescence et Archivage
Révocation explicite des documents obsolètes, accès contrôlé aux archives et blocage de l'utilisation dans les processus actifs.
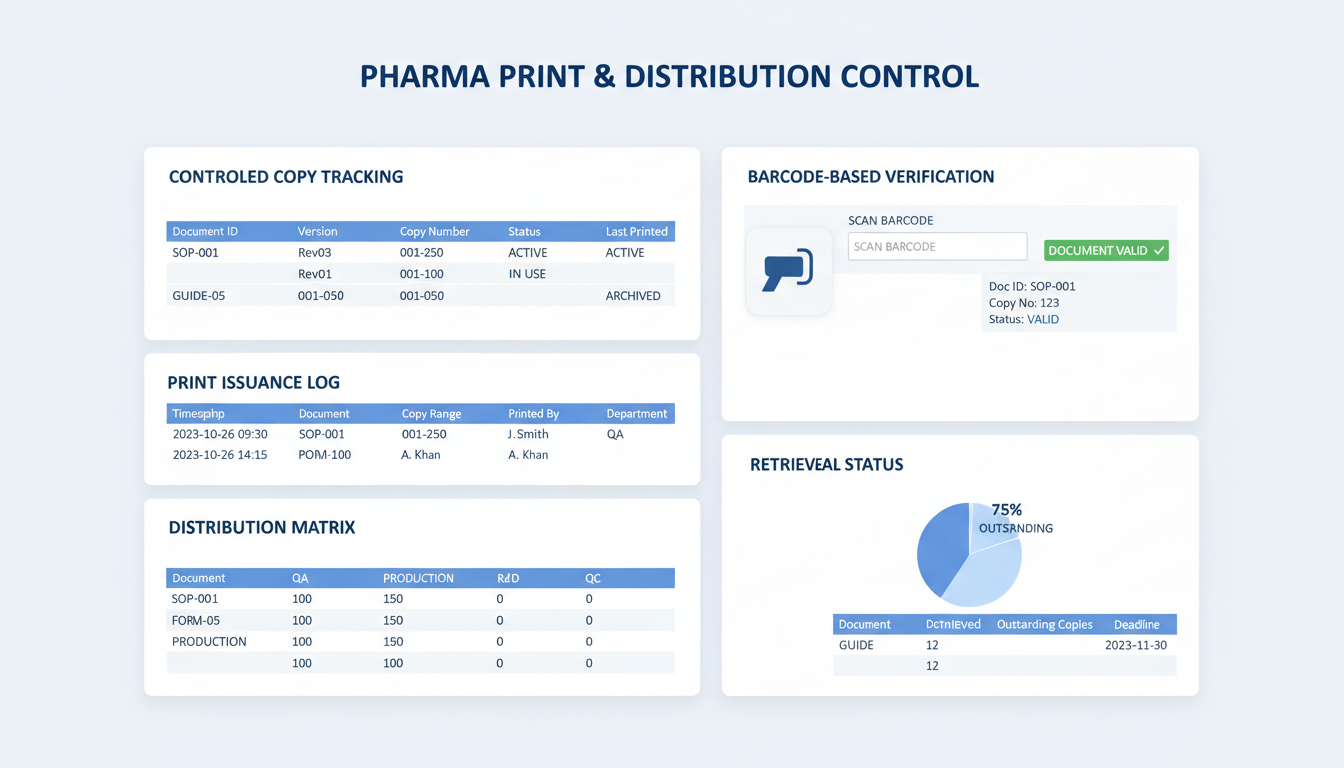
Émission d'Impressions, Distribution de Copies Contrôlées et Suivi de la Récupération
Garantir que seuls les documents actuels et autorisés parviennent en production — y compris les copies non contrôlées, de formation et les brouillons
Approbation
Finaliser le document avec les métadonnées de version et d'approbation via le logiciel de flux d'approbation documentaire.
Verrouillage de la Version
Geler la version approuvée ; empêcher les modifications et marquer les états de supersession grâce aux protections du système de contrôle documentaire numérique.
Émission d'Impressions
Accorder des droits d'impression par rôle/site, générer des filigranes comme copie contrôlée, copie non contrôlée, copie de formation et brouillon. Activer l'impression et la récupération des copies contrôlées sur les sites.
Distribution
Publier sur des listes contrôlées par site et par rôle avec des étiquettes codes-barres et accusé de réception à la remise.
Réconciliation et Piste d'Audit
Suivre les détails d'impression et réconcilier les copies papier émises avec les audits pour une traçabilité complète du système de contrôle documentaire pharmaceutique.
Contrôle et Vérification des Impressions
Combler l'écart entre les systèmes numériques et les copies physiques du terrain grâce au suivi par codes-barres
Génération Dynamique de Codes-Barres
Filigranage automatique et génération de codes-barres uniques pour chaque copie physique imprimée.
Vérification au Point d'Utilisation
Scan de codes-barres en temps réel sur le terrain de production pour vérifier le statut d'approbation et la version du document.
Audit Complet des Impressions
Suivi complet des copies physiques distribuées, y compris les journaux d'impression par utilisateur et les données de localisation.
OCR Intelligent et Recherche par IA pour Votre Système de Gestion de Documents de Conformité GxP
Rendez les documents réglementés consultables, révisables et accessibles dans votre système de contrôle documentaire numérique
OCR Alimenté par l'IA
Convertit les scans et images en texte consultable et modifiable.
Réduire la transcription manuelle et permettre une découverte plus rapide.
Recherche Intelligente
Fait remonter le contenu réglementé avec une pertinence contextuelle.
Améliorer la précision de récupération dans les archives de documents.
Recherche Vocale
Accélère la récupération et la révision mains libres.
Accès plus rapide lors des audits et des flux de travail d'équipe.
E-Discovery et Support aux Audits
Permet une révision plus rapide des documents, la récupération de preuves et les réponses aux audits.
Aide à la conformité, la traçabilité et les audits réglementés.
Accessibilité pour Toute l'Équipe
Fournit un accès cohérent aux documents contrôlés dans toutes les fonctions.
Permettre la traçabilité et la collaboration dans des environnements réglementés.
Intégrations DMS Conformes GMP avec eQMS, LMS, LIMS et MES
Connecté de manière transparente à votre écosystème de système de gestion documentaire GxP d'entreprise pour une traçabilité documentaire de bout en bout
LMS
Besoins en formation liés à l'introduction de nouvelles SOP et aux changements de version. Vérification de l'achèvement de la formation.
eQMS
Changement de version issu du contrôle des modifications, des constatations d'audit, des CAPA.
RIMS
Changement de version suite aux constatations réglementaires.
LIMS
Méthodes d'analyse et STP avec résultats et dossiers de laboratoire.
eLog Book
Référence au modèle de journal de bord.
Validation du Nettoyage
Accès aux SOP pour les procédures de nettoyage.
eBMR/MES
Gestion et accès aux documents BMR/BPR.
CAPS
Manuels d'équipements/SOP pour les procédures d'étalonnage.
SAP
Intégration avec la planification des ressources d'entreprise.
UMS
Intégration avec le système de gestion des utilisateurs.
Atouts de la Plateforme DMS Low-Code d'AmpleLogic et Valeur Ajoutée par l'IA
Flexibilité low-code, préparation à la conformité et automatisation contrôlée pour les sciences de la vie
Concepteur LCNC par Glisser-Déposer
Le constructeur visuel réduit le code personnalisé et accélère la livraison pour une composition rapide d'applications.
Gestion Documentaire Cloud pour la Pharma
Logiciel de gestion documentaire cloud pour la pharma avec des délais accélérés et un impact commercial rapide — ROI en aussi peu que 3 mois.
Gestion Documentaire pour l'Industrie Réglementée
Logiciel de gestion documentaire pour l'industrie réglementée conçu pour la documentation et les audits. Prêt pour USFDA, MHRA, ISO.
18+ Applications COTS
Applications préconstruites pour les flux de travail courants des sciences de la vie — prêtes à déployer immédiatement.
Plus de 100 Clients en Sciences de la Vie
La base de clients démontre une forte traction dans le secteur et une adoption validée de la plateforme.
Automatisation Alimentée par l'IA
L'IA aide à l'automatisation, l'extraction et l'assemblage d'applications pour accélérer la composition et le traitement.
ROI du Logiciel DMS : Bénéfices Commerciaux de la Gestion Documentaire Pharmaceutique Numérique
Conformité, rapidité, précision et qualité numérique évolutive
25%
Réduction des Constatations d'Audit
Pourcentage cible de réduction des constatations après déploiement.
30%
Amélioration du Délai de Libération
Réduction projetée du délai de libération des documents.
50%
Effort Manuel Économisé
Réduction estimée des heures de traitement manuel.
"Facile d'accès et de gestion. Travail sans papier et possibilité de conserver les dossiers du contrôle des modifications avec un accès facile depuis n'importe quel endroit. Moins chronophage."
Shweta Ramdas R.
Spécialiste Contrôle Documentaire
"Le logiciel est facile à utiliser et à mettre en œuvre au niveau opérateur. Les activités en ligne avec pistes d'audit rendent la conformité transparente."
Silpa K.
Assurance Qualité
"Flux de travail configurables, avantages de conformité et réduction de l'utilisation du papier dans toute l'organisation. Le support client est réactif et la mise en œuvre était simple."
Ramesh T.
Responsable Informatique Pharma
Gardez une longueur d'avance dans les sciences de la vie
Recevez les dernières mises à jour produit, actualités de conformité et analyses du secteur directement dans votre boîte mail.